
【题目】下列图象关系合理的是
A.  向pH=9的NaOH溶液中不断加水
向pH=9的NaOH溶液中不断加水
B.  在久置的NaOH溶液中加入盐酸
在久置的NaOH溶液中加入盐酸
C.  分别向稀盐酸中加入等质量的Fe和Mg
分别向稀盐酸中加入等质量的Fe和Mg
D.  在饱和的KNO3溶液中加入KNO3晶体
在饱和的KNO3溶液中加入KNO3晶体
【答案】B
【解析】
A.氢氧化钠溶液中加水稀释,溶液的pH会变小,但不会小于7,故A错误;
B.由于部分氢氧化钠与空气中的二氧化碳反应,因此变质的氢氧化钠中含有碳酸钠,而放入盐酸后先要与氢氧化钠反应生成氯化钠和水,故开始的一段时间内无气体产生,氢氧化钠反应完全后,盐酸会与碳酸钠反应生成二氧化碳直至反应结束气体质量不再变化,故B正确;
C.镁的金属活动性比铁强,故与稀盐酸反应时镁的反应速度要快一些(图象更陡一些),同质量的镁比铁生成的氢气多,故最终镁的曲线应该在铁的上面,故C错误;
D.向一定量饱和KNO3溶液中逐渐加入KNO3固体,溶液仍然饱和,硝酸钾的质量分数不变,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】工业溴主要利用中度卤水进行吹溴工艺生产。某化学小组的同学为了解从工业溴中提纯溴的方法,设计如下实验装置:

有关资料:Br2沸点为59℃,微溶于水,有毒性和强腐蚀性。
(1)图中盛装工业溴的仪器名称是______,烧杯A中热水浴的作用为______。
(2)按图连接好装置,检查装置气密性并装入试剂,然后________,再开始对A加热。C中液体产物的颜色为______。
(3)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是 _________。
A.乙醇 B.四氯化碳 C.纯碱溶液 D.裂化汽油
(4)Br2被过量Na2CO3溶液吸收的氧化产物为NaBrO3,则D中发生反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3+S=Na2S2O3。常温下溶液中析出晶体为Na2S2O35H2O。Na2S2O35H2O于4045℃熔化,48℃分解:Na2S2O3 易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线 如图所示。

I.现按如下方法制备Na2S2O35H2O:
将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按如下图示安装好装置。
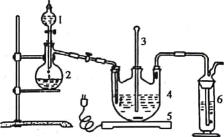
(1)仪器2的名称为__________,装置6中可加入________。
A. BaCl2溶液 B.浓 H2SO4 C.酸性KMnO4溶液 D. NaOH溶液
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二 氧化硫气体较均匀的通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,反应原理为:
①Na2CO3+SO2═Na2SO3+CO2 ②Na2S+SO2+H2O═Na2SO3+H2S
③2H2S+SO2═3S↓+2H2O ④Na2SO3+S![]() Na2S2O3
Na2S2O3
随着SO2气体的通入,看到溶液中有大量浅黄色固体析出,继续通SO2气体,反应约半小时。当溶液中pH接近或不小于7时,即可停止通气和加热。溶液pH要控制不小于7的理由是:______(用文字和相关离子方程式表示)。
Ⅱ.分离Na2S2O35H2O并测定含量:

(3)为减少产品的损失,操作①为_______,操作②是抽滤、洗涤、干燥,其中洗涤操作是用______(填试剂名称)作洗涤剂。
(4)蒸发浓缩滤液,直至溶液呈微黄色浑浊为止。蒸发时要控制温度不宜过高,其原因是_______________。
(5)制得的粗产品中往往含有少量杂质。为了测定粗产品中Na2S2O35H2O的含量,一般采用在酸性条件下用KMnO4标准液滴定的方法(假定杂质与酸性KMnO4溶液不反应)。 称取1.28g粗样品溶于水,用0.40mol/LKMnO4溶液(加入适量硫酸酸化)滴定,当溶液 中S2O32-全部被氧化时,消耗KMnO4溶液20.00mL。(5S2O32-+ 8MnO4-+14H+=8Mn2++l0SO42-+7H2O)
试回答:
①滴定终点时的颜色变化_______________。
②产品中Na2S2O35H2O的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g)在温度为T1、T2(T1<T2)时达到平衡,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g)在温度为T1、T2(T1<T2)时达到平衡,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

A. A、C两点的反应速率:A>C
B. B、C两点的气体的平均相对分子质量:B<C
C. A、C两点气体的颜色:A浅,C深
D. 保持容器体积不变,再充入NO2气体,NO2的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯亚砜(SOCl2)是一种无色易挥发液体,剧烈水解生成两种气体,常用作脱水剂,其熔点-105℃,沸点79℃,140℃以上时易分解。
(1)用硫黄(S)、液氯和三氧化硫为原料,在一定条件合成二氯亚砜,原子利用率达100%,则三者的物质的量比为______________________。
(2)甲同学设计如图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2(夹持及加热装置略)
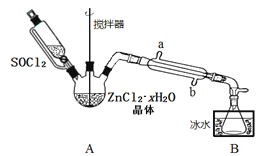
①SOCl2在该实验中的作用_________________________________;加热条件下,A装置中总的化学方程式为_________________________________。
②实验结束后,为检测ZnCl2·xH2O晶体是否完全脱水,甲同学设计实验方案如下,正确的实验顺序为___________(填序号)
a.干燥 b.洗涤; c加入足量硝酸酸化的硝酸银溶液,充分反应;
d称取蒸干后的固体m克溶于水;e.过滤; f称得固体为n克
若m/n=___________(保留小数点后两位),即可证明晶体已完全脱水。
(3)乙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丙同学认为该实验可能发生副反应使最后的产品不纯。
①可能发生的副反应的离子方程式_________________________________。
②丙同学设计了如下实验方案判断副反应的可能性:
i.取少量FeCl3·6H2O于试管中,加入足量SOCl2振荡使两种物质充分反应:
ii.往上述试管中加水溶解,取溶解后的溶液少许于两支试管,进行实验验证,完成表格内容。
供选试剂:AgNO3溶液、稀盐酸、稀HNO3、酸性KMnO4溶液、KSCN溶液、K3[Fe(CN)6]溶液、溴水)
方案 | 操作 | 现象 | 结论 |
方案一 | 往一支试管中滴加___________ | 若无明显现象 | 则发生了上述副反应 |
方案二 | 往另一支试管中滴加___________ | ___________ | 则没有发生上述副反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞巴匹特为新型抗溃疡药,它可保护胃肠黏膜免受各种致溃疡因子的危害,其合成路线如下:
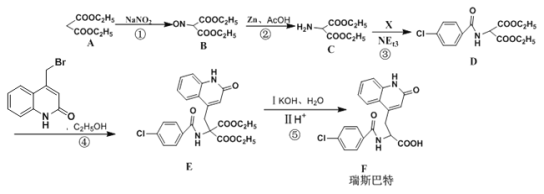
已知:Y的结构简式为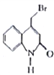 。
。
(1)A的化学名称为___________,化合物F的分子式为___________。
(2)化合物C中官能团的名称为___________,C与足量的NaOH溶液反应的化学方程式为___________。
(3)反应①~④中,属于取代反应的是___________(填序号)。
(4)C→D的转化中,生成的另一种产物为HCl,则X的结构简式为___________。
(5)已知Y中的溴原子被-OH取代得到Z,写出同时满足下列条件的Z的一种同分异构体的结构简式:___________
I.分子中含有一个苯环和一个五元环,且都是碳原子形成环;
I1.苯环上有两个取代基,且处于对位;
Ⅲ.能与 NaHCO3溶液发生反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A、B、C原子核内质子数之和为31,最外层电子数之和为17,这三种元素是()
A. N、P、ClB. P、O、SC. O、F、ClD. N、O、S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀和滤液,再用过量稀硝酸处理沉淀,最后减少到4.66g,并有气体放出。计算:
(1)求原混合液中Na2SO4的物质的量?__________________
(2)产生的气体在标准状况下的体积为多少?_________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com