
【题目】瑞巴匹特为新型抗溃疡药,它可保护胃肠黏膜免受各种致溃疡因子的危害,其合成路线如下:
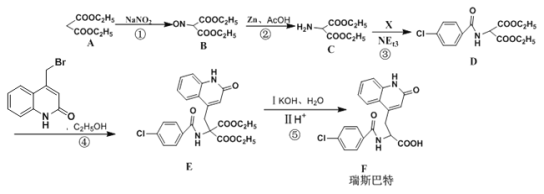
已知:Y的结构简式为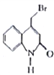 。
。
(1)A的化学名称为___________,化合物F的分子式为___________。
(2)化合物C中官能团的名称为___________,C与足量的NaOH溶液反应的化学方程式为___________。
(3)反应①~④中,属于取代反应的是___________(填序号)。
(4)C→D的转化中,生成的另一种产物为HCl,则X的结构简式为___________。
(5)已知Y中的溴原子被-OH取代得到Z,写出同时满足下列条件的Z的一种同分异构体的结构简式:___________
I.分子中含有一个苯环和一个五元环,且都是碳原子形成环;
I1.苯环上有两个取代基,且处于对位;
Ⅲ.能与 NaHCO3溶液发生反应。
【答案】1,3-丙二酸二乙酯 C19H15O4N2Cl 氨基、酯基 C2H5OOCCH(NH2)COOC2H5+2NaOH![]() NaOOCCH(NH2)COONa+2C2H5OH ①③④
NaOOCCH(NH2)COONa+2C2H5OH ①③④ ![]()
【解析】
(1)A由1分子1,3-丙二酸与2分子乙醇形成的酯;化合物F的分子式为C19H15O4N2Cl;
(2)由结构可知,C所含官能团有氨基、酯基;酯在碱性条件下水解生成相应的醇及羧酸盐;
(3)反应①A中一个H被-NO取代;反应②对比B、C结构,可知B转化为C的过程为去氧加氢,属于还原反应;反应③氨基中一个H被![]() 取代;反应④对比D、E的结构,可知D中次甲基中H原子被
取代;反应④对比D、E的结构,可知D中次甲基中H原子被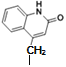 基团代替,属于取代反应。
基团代替,属于取代反应。
(4) 对比C、D的结构,可知C与X发生取代反应生成D与HCl,HCl中H原子源于C中氨基,Cl原子源于X,可以确定X为![]() ;
;
(5)Y的结构简式为: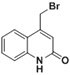 ,Y中的溴原子被-OH取代得到Z,则Z的结构简式为:
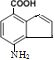
,Y中的溴原子被-OH取代得到Z,则Z的结构简式为: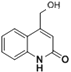 ,Z的同分异构体,分子中含有一个苯环和一个五元环,且都是碳原子形成环,说明N原子不在环上;能与 NaHCO3溶液发生反应,说明含有羧基;苯环上有两个取代基,应该是氨基和羧基,且处于对位; 则Z的结构简式可能为
,Z的同分异构体,分子中含有一个苯环和一个五元环,且都是碳原子形成环,说明N原子不在环上;能与 NaHCO3溶液发生反应,说明含有羧基;苯环上有两个取代基,应该是氨基和羧基,且处于对位; 则Z的结构简式可能为 。
。
(1)根据系统命名法,有机物![]() 的化学名称为1,3—丙二酸二乙酯,化合物F的分子式为C19H15O4N2Cl;
的化学名称为1,3—丙二酸二乙酯,化合物F的分子式为C19H15O4N2Cl;
故答案为:1,3-丙二酸二乙酯;C19H15O4N2Cl;
(2)化合物![]() 中官能团的名称为氨基、酯基;酯可在NaOH溶液中发生碱性水解,C(2—氨基—1,3—丙二酸二乙酯)与足量NaOH溶液反应的化学方程式为:C2H5OOCCH(NH2)COOC2H5+2NaOH
中官能团的名称为氨基、酯基;酯可在NaOH溶液中发生碱性水解,C(2—氨基—1,3—丙二酸二乙酯)与足量NaOH溶液反应的化学方程式为:C2H5OOCCH(NH2)COOC2H5+2NaOH![]() NaOOCCH(NH2)COONa+2C2H5OH;
NaOOCCH(NH2)COONa+2C2H5OH;
故答案为:氨基、酯基;C2H5OOCCH(NH2)COOC2H5+2NaOH![]() NaOOCCH(NH2)COONa+2C2H5OH;
NaOOCCH(NH2)COONa+2C2H5OH;
(3) 反应①A中一个H被-NO取代,属于取代反应;反应②对比B、C结构,可知B转化为C的过程为去氧加氢,属于还原反应;反应③氨基中一个H被![]() 取代,属于取代反应;反应④对比D、E的结构,可知D中次甲基中H原子被
取代,属于取代反应;反应④对比D、E的结构,可知D中次甲基中H原子被 基团代替,属于取代反应。所以反应①~④中,属于取代反应的是①③④;
基团代替,属于取代反应。所以反应①~④中,属于取代反应的是①③④;
故答案为:①③④;
(4) 对比C、D的结构,可知C与X发生取代反应生成D与HCl,根据产物的碳架结构并结合原子守恒,可知X的结构简式为![]() ;
;
故答案为:![]() ;
;
(5) Y的结构简式为: ,Y中的溴原子被-OH取代得到Z,则Z的结构简式为:
,Y中的溴原子被-OH取代得到Z,则Z的结构简式为: ,Z的同分异构体:分子中含有一个苯环和一个五元环,且都是碳原子形成环,说明N原子不在环上;能与 NaHCO3溶液发生反应,说明含有羧基;苯环上有两个取代基,应该是氨基和羧基,且处于对位;则Z的结构简式可能为
,Z的同分异构体:分子中含有一个苯环和一个五元环,且都是碳原子形成环,说明N原子不在环上;能与 NaHCO3溶液发生反应,说明含有羧基;苯环上有两个取代基,应该是氨基和羧基,且处于对位;则Z的结构简式可能为 。
。
故答案为: 。
。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在恒温恒压密闭容器M(如图Ⅰ)和恒温恒容密闭容器N(如图Ⅱ)中,两容器中均加入a molA和a molB,起始时两容器体积均为VL,发生如下反应并达到化学平衡状态:2A(?)+ B(?)![]() xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是
xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是

A. x=2
B. 若N中气体的密度如图Ⅲ所示,则A、B只有一种是气态
C. A为气体,B为非气体,则平衡时M、N中C的物质的量相等
D. 若A、B均为气体,平衡时M中A的转化率小于N中A的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色粉末,由BaCl2、K2SO4、CaCO3、NaOH、CuSO4中的一种或几种组成,为了探究它的成份,进行了如下实验:下列判断正确的是( )

A. BaCl2,CaCO3一定存在,NaOH可能存在
B. K2SO4、CuSO4一定不存在
C. K2SO4、NaOH、CaCO3、BaCl2一定存在,CuSO4可能存在
D. C为单一溶质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的基本化工原料,可制备乙酸乙酯,其转化关系如图.

已知:H2C=CH﹣OH不稳定
I ①的反应类型是___.请写出乙烯官能团名称_____, 由A生成B的化学方程式_____.
II 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。

已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点见下表:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用为_______;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式__________
(2)球形干燥管C的作用是______若反应前D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出________;再加入(此空从下列选项中选择)________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A 五氧化二磷 B 碱石灰
C 无水硫酸钠 D 生石灰
(4)从绿色化学的角度分析,使用浓硫酸制乙酸乙酯不足之处主要有________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象关系合理的是
A.  向pH=9的NaOH溶液中不断加水
向pH=9的NaOH溶液中不断加水
B.  在久置的NaOH溶液中加入盐酸
在久置的NaOH溶液中加入盐酸
C.  分别向稀盐酸中加入等质量的Fe和Mg
分别向稀盐酸中加入等质量的Fe和Mg
D.  在饱和的KNO3溶液中加入KNO3晶体
在饱和的KNO3溶液中加入KNO3晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,还含有少量SiO2。现以卤块为原料按如图所示流程进行生产,用于制备金属镁。

请回答下列问题:
(1)步骤①中,为了加快酸溶速率,除了适当增加稀盐酸的浓度外,还可以采取的措施是____________(任写一条)。
(2)步骤②得到的X是___(填化学式),能够分离得到沉淀的方法是_____
(3)写出步骤④的化学方程式:_______
(4)步骤①中溶解卤块的盐酸如果过量太多造成的影响是____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2(g)+O2(g)=2H2O(l) ΔH=-569.6kJ/mol,2H2O(g)=2H2(g)+O2(g) ΔH=+482.1 kJ/mol。现有1g液态H2O,蒸发时吸收的热量是 ( )
A. 2.43 kJ B. 4.86 kJ C. 43.8 kJ D. 87.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 将 Cl2 通入水中: Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 向 Fe2(SO4)3 溶液中加入过量铁粉: Fe3++Fe=2Fe2+
C. 将 SO2 通入双氧水中: SO2+H2O2=2H++SO42-
D. 向 Na2SiO3 溶液中滴加稀盐酸: Na2SiO3+2H+=H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图象能正确反映其对应操作中各量变化关系的是 ( )
A.  用一定质量的高锰酸钾加热制氧气
用一定质量的高锰酸钾加热制氧气
B.  向一定质量的石灰石中加入过量的稀盐酸
向一定质量的石灰石中加入过量的稀盐酸
C.  向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
D.  分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com