
| A、棕红色的NO2加压后颜色先变深后变浅 |
| B、氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
| C、黄绿色的氯水光照后颜色变浅 |
| D、合成氨工业使用高压以提高氨的产量 |


科目:高中化学 来源: 题型:
| A、可用浓硝酸除去铝制品表面的铜镀层 | ||
B、用催化法处理汽车尾气中的CO和NO:CO+NO
| ||
| C、浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体 | ||
| D、因为浓硫酸在常温下不可与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、下列仪器中①漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥滴定管;⑦燃 烧 匙,常用于物质分离的是①③⑤ |
| B、甲酸溶液滴到大理石台板上有气泡产生:2H++CaCO3═CO2↑+Ca2++H2O |
| C、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉溶解 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用25mL量筒量取12.36mL盐酸 |
| B、用托盘天平称取8.75克食盐 |
| C、用标准NaOH溶液滴定未知浓度的盐酸,用去NaOH溶液23.10mL |
| D、用pH试纸测得某溶液的PH为3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
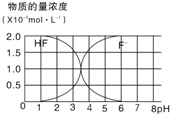 请按要求完成下列各小题:
请按要求完成下列各小题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡含离子键的化合物,一定含金属元素 |
| B、在化合物MgCl2中,两个氯离子之间也存在离子键 |
| C、离子化合物一定能导电 |
| D、原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“半成品碳”在硫酸溶液中加热可能发生的是消去反应 |
| B、“半成品碳”是碳元素的一种新单质 |
| C、蔗糖溶液与新制的氢氧化铜悬浊液混合加热有砖红色沉淀生成 |
| D、焦糖烯是一种新型的烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com