
【题目】阿伏加德罗常数值用NA表示。下列说法中不正确的是
A. 0.5 mol由F2与Ar组成的混合气体中含质子总数为9NA
B. 标准状况下,足量Na2O2与5.6 L CO2反应转移电子数目为0.25NA
C. 71g Cl2通入水中,HClO、ClO-、Cl-三种微粒数目之和为2NA
D. 常温下,1.5 L 1.0 mol L-1 CuSO4溶液中阳离子数目大于1.5NA
【答案】C
【解析】A、0.5mol均为F2时,总质子数为18×0.5mol=9mol,0.5mol均为Ar时,总质子数为18×0.5mol=9mol,所以不论二者以何种比例混合,总质子数一定是9mol,A正确。B、标准状况下,5.6L CO2物质的量为0.25mol,与足量Na2O2反应时消耗Na2O20.25mol,其中被氧化的-1价的氧原子占Na2O2总氧原子的一半为0.25mol,其化合价从-1价升高到0价,所以转移电子数![]() ,B正确。C、71g Cl2为1mol,含有Cl原子2mol,通入水中后,部分溶于水后以Cl2分子存在,部分与水反应生成HCl和HClO,HCl完全电离生成H+和Cl-,HClO部分电离生成H+和Cl-,所以HClO、ClO-、Cl-三种微粒数目之和小于2mol,C错误。D、CuSO4物质的量1.5mol,部分Cu2+水解Cu2++2H2O
,B正确。C、71g Cl2为1mol,含有Cl原子2mol,通入水中后,部分溶于水后以Cl2分子存在,部分与水反应生成HCl和HClO,HCl完全电离生成H+和Cl-,HClO部分电离生成H+和Cl-,所以HClO、ClO-、Cl-三种微粒数目之和小于2mol,C错误。D、CuSO4物质的量1.5mol,部分Cu2+水解Cu2++2H2O ![]() Cu(OH)2+2H+,水解过程中使得溶液中阳离子数目增大,所以溶液中阳离子数目大于1.5NA,D正确。正确答案C。
Cu(OH)2+2H+,水解过程中使得溶液中阳离子数目增大,所以溶液中阳离子数目大于1.5NA,D正确。正确答案C。


科目:高中化学 来源: 题型:
【题目】过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧.下列有关说法不正确的是( )
A.Na2O2与CO2反应时,Na2O2是氧化剂,CO2是还原剂
B.1mol过氧化钠中阴离子数目为1NA
C.过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性
D.过氧化钠与二氧化硫反应时可生成硫酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol·L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )

A. 在0~a范围内,只发生中和反应
B. a=0.3
C. ab段发生反应的离子方程式为CO32-+2H+=CO2↑+H2O
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下: 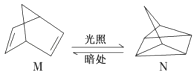
△H=+88.6kJ/mol,则M、N相比,较稳定的是 .
(2)已知CH3OH(l)的燃烧热△H=﹣238.6kJ/mol,CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2(g)△H=﹣a kJ/mol,则a238.6(填“>”“<”或“=”).
O2(g)═CO2(g)+2H2(g)△H=﹣a kJ/mol,则a238.6(填“>”“<”或“=”).
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2 , 当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式: .
(4)火箭和导弹表面的薄层是耐高温物质.将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=﹣1176kJ/mol,则反应过程中,每转移1mol电子放出的热量为 .
(5)汽车排出的尾气中含有CO和NO等气体.为了解决污染问题,在汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物CO和NO转化为无毒的大气循环物质.已知: N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
2C(s)+O2(g)═2CO(g)△H=﹣221.0kJ/mol
C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol
请写出污染物CO和NO转化为无毒的大气循环物质的热化学方程式是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取Al2O3两种工艺的流程如下:
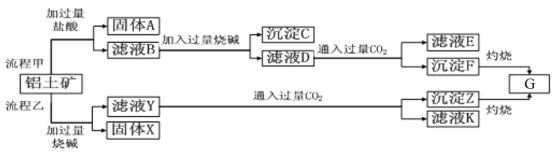
请回答下列问题:
(1)流程乙加入烧碱后和SiO2反应的离子方程式为________________________________。
(2)流程甲滤液D中通入过量CO2的化学方程式为_______________________________。
(3)验证滤液B中是否含有Fe3+的方法:_____________________________。
(4)写出滤液E中溶质的一种用途_________________________________。
(5)由物质G制取铝的化学方程式为__________________________。
(6)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X。已知每转移3mole-,有1.5mol化合物X生成,此反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氯化碘(沸点97.4℃),是一种红棕色易挥发的液体,不溶于水,溶于乙醇和乙酸。某校研究性学习小组的同学拟制备一氯化碘。回答下列问题:
(1)甲组同学拟利用干燥、纯净的氯气与碘反应制备一氯化碘,其装置如下:(已知碘与氯气的反应为放热反应)
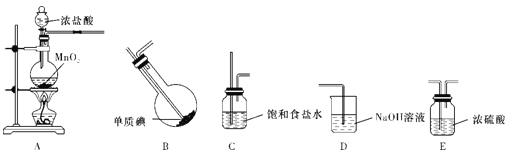
①各装置连接顺序为A→___________;A装置中发生反应的离子方程式为___________。
②B装置烧瓶需放在冷水中,其目的是:___________,D装置的作用是____________。
(2)乙组同学采用的是最新报道的制一氯化碘的方法。即在三颈烧瓶中加入粗碘和盐酸,控制温度约50℃,在不断搅拌下逐滴加入氯酸钠溶液,生成一氯化碘。则发生反应的化学方程式为___________________。
(3)设计简单实验证明:
①ICl的氧化性比I2强:________________________________________________。
②ICl与乙烯能发生反应:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.100molL﹣1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步: A.移取20mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写) .
(2)上述B步骤操作的目的是 .
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果(填“偏高“、“偏低”或“不变”).
(4)判断到达滴定终点的实验现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com