
【题目】为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是
A. KI(淀粉溶液) B. FeCl2溶液(KSCN)
C. Na2SO3溶液(BaCl2) D. HCHO溶液(石蕊试液)
科目:高中化学 来源: 题型:
【题目】汽油抗爆剂的添加剂通常使用1,2-二溴乙烷,常温下它是无色液体,密度2.18 g.cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:

(1)装置a中碎瓷片的作用是__________________________。
(2)安全瓶b可以防止倒吸,并可以检査实验进行时试管d是否发生堵塞,请写出发生堵塞时瓶b中的现象______________________。
(3)判断该制备反应己经结束的最简单的方法是________________________________。
(4)写出装置e中发生的反应的离子方程式_______________________________。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 _____________层(填“上”、“下”),若产物中有少量未反应的Br2,最好用_______________洗涤除去(填正确选项前的字母)。
a.水 b.亚硫酸钠溶液 c.碘化钠溶液 d.乙醇
(6)实验结束时若制得纯净的1,2-二溴乙烷18.8g,则至少消耗乙醇_______________g。
(7)某学生在做此实验时使用了一定量的液溴,当反应结束时,发现消耗乙醇的量比正常情况下超过许多。原因除了装置的气密性不好之外,还有可能的2个原因_______________、_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物是一类重要的物质。回答下列有关问题:
(l)某试管底部附着一层致密的铜,向其中滴加10 mL 稀硫酸时,无明显现象,再加入0.1g KNO3, 振荡,可观察到有气泡生成,除此外还可观察到的现象是__________,生成的气体是___(填化学式)。
(2)铜与浓硫酸加热反应,实验结束后观察到试管底部有黑色物质形成,溶液呈蓝色,通过检验知该黑色物质为Cu2S。写出浓硫酸与Cu反应生成Cu2S的化学方程式:___________。
(3)工业上利用合成气(主要成分为CO、CO2和H2)、空气,在铜基催化剂作用下,可合成甲醇。已知:25℃,101kPa下:
H2(g)+1/2O2(g)=H2O(g) △H=-242kJ/mol;
CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-676kJ/mol。
写出CO2和H2生成甲醇等气态产物的热化学方程式:________________。
(4)合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的碳的氧化物。铜液吸收CO的化学方程式为Cu(NH3)2Ac(aq)+CO(g)+NH3(g) ![]() [Cu(NH3)3CO]Ac(aq) △H
[Cu(NH3)3CO]Ac(aq) △H
① 如果要提高上述反应的反应速率,可以采取的措施是______(填字母)。
a.增压 b.增加NH3的浓度 c.增大Cu(NH3)2Ac浓度
d.降温 e.减小[Cu(NH3)3CO]Ac浓度
② 合成氨反应中,在不增减反应物或生成物的情况下,不断改变反应条件,反应速率与时间的关系如图所示:

t4~t5改变的条件可能是__________,H2转化率最高的时间段是________。若某温度下,3xmolH2和xmolN2反应,在1L的密闭容器中, H2的最高转化率为50%,则该温度下2NH3(g) ![]() 3H2(g)+N2(g)的平衡常数K=_____(保留两位小数)。
3H2(g)+N2(g)的平衡常数K=_____(保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程属于固氮的是( )
A. 氮气和镁反应生成氮化镁 B. 豆科作物根把含氮化合物转变为蛋白质
C. 植物从土壤中吸收含氮养料 D. 将氨气转化成各类铵态氮肥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列陈述I、II均正确并且有因果关系的是( )
选项 | 陈述I | 陈述II |
A | Fe2O3是红棕色粉末 | Fe2O3常做红色涂料 |
B | SiO2是两性氧化物 | SiO2可和HF反应 |
C | Al2O3难溶于水 | Al2O3可用作耐火材料 |
D | SO2有漂白性 | SO2可使溴水褪色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)因硬度大、熔点高、常温时耐酸碱腐蚀而被广泛应用。以钛铁矿(主要成分是FeTiO3,钛酸亚铁)为主要原料冶炼金属钛的工艺流程如图所示:

请回答下列问题:
(1)钛铁矿在酸浸前需进行粉碎处理,原因是 。
(2)钛铁矿和浓硫酸反应的产物之一是TiOSO4,反应中无气体生成。副产品甲是 。
(3)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是 。
(4)在溶液Ⅱ中加水并加热的目的是 。
(5)上述冶炼金属钛的过程中,可回收利用的物质是 。
(6)上述流程制得的金属钛中混有少量杂质,可加入 溶解除去。
(7)若钛铁矿中钛的含量为a%,整个流程钛的损耗率为b%,欲制造1 t金属钛,需要钛铁矿的质量为_____________t(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业上常用下列方法制备H2:
方法I:C(s)+2H2O(g) ![]() CO2(g)+2H2(g)
CO2(g)+2H2(g)
方法Ⅱ:CO(g)+H2O(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知
①C(s,石墨)+O2(g)=CO2(g) △H1=一394 kJ·mol一1
②2C(s,石墨)+O2(g)=2CO(g) △H2=一222 kJ·mol-1
③2H2(g)+O2(g)= 2H2O(g) △H3=一484 kJ·mol-1
试计算25℃时由方法Ⅱ制备1 000 g H2所放出的能量为______________。
(2)在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应C(s)+2H2O(g) ![]() CO2(g)+2H2(g)。其相关数据如下表所示:
CO2(g)+2H2(g)。其相关数据如下表所示:

①T1____T2(填“>”“=”或“<”);T1℃时,该反应的平衡常数K=______________。
②乙容器中,当反应进行到1.5 min时,H2O(g)的物质的量浓度范围是__________。
③在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是____________(填序号)。
A.V逆(CO2)=2V正(H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均摩尔质量保持不变
(3) 现有0.175 mol/L 醋酸钠溶液500 mL(已知醋酸的电离平衡常数K=1.75×10-5)。
①下列图像能说明醋酸钠的水解反应在t1时刻达到平衡的是________(填序号,下同)。
A.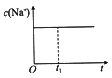 溶液中c(Na+)与反应 时间t的关系
溶液中c(Na+)与反应 时间t的关系
B. CH3COO一的水解速率与反应时间t的关系
CH3COO一的水解速率与反应时间t的关系
C . 溶液的pH与反应时间t的关系
溶液的pH与反应时间t的关系
D. K与反应时间t的关系
K与反应时间t的关系
②在醋酸钠溶液中加入下列少量物质,水解平衡向正反应方向移动的有_____________ 。
A.冰醋酸B.纯碱固体c.醋酸钙固体D.氯化铵固体
(4)在醋酸钠溶液中加入少量冰醋酸后,溶液中微粒浓度的关系式能成立的有________。
A.c(CH3COO一)+c(CH3COOH)>c(Na+)
B.c(Na+)> c(CH3COO一)>c(H+)>c(OH一)
C.c(CH3COO一)> c(Na+)> c(H+)>c(OH一)
D.c(CH3COO一)>c c(H+)>c(OH一)> c(Na+)
(5)欲配制0.175 mol/L醋酸钠溶液500 mL,可采用以下两种方案:
方案一:用托盘天平称取_________g无水醋酸钠,溶于适量水中,配成500 mL溶液。
方案二:用体积均为250 mL且浓度均为_____________的醋酸与氢氧化钠溶液混合而成(设混合后的体积等于混合前两者体积之和)。在室温下,0.175 mol/L醋酸钠溶液的pH约为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制造镁粉是将镁蒸气在气体中冷却.可作为冷却气体的是( )
①空气 ②CO2 ③Ar ④H2 ⑤N2.
A.①② B.②③ C.③④ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用 63%的浓 HNO3 (其密度为 1.4 g·mL -1)配制 240 mL 0.50 mol·L-1 稀 HNO3,若实验仪器有:
A.10 mL 量筒 B.50 mL 量筒 C.托盘天平 D.玻璃棒 E.100 mL 容量瓶 F.250 mL 容量瓶 G.500 mL 容量瓶 H.胶头滴管 I.200mL 烧杯
(1)此浓硝酸的物质的量浓度为_____mol·L -1。
(2)应量取 63%的浓硝酸_____mL,应选用_____(填仪器的字母编号)。
(3)实验时还需选用的仪器有 D、I、______(填序号)。
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)______。
①量取浓硝酸的量筒用蒸馏水洗涤 2~3 次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com