
【题目】核磁共振氢谱法是有机物测定的一种重要方法,有机物中有几种氢原子,核磁共振氢谱中就有几个峰,G是一种合成橡胶和树脂的重要原料,A是一种五元环状化合物,其核磁共振氢谱只有一个峰;F的核磁共振氢谱有3个峰,峰面积之比为2:2:3。已知:(其中R是烃基)
①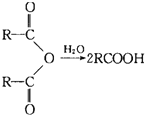 ②RCOOH
②RCOOH![]() RCH2OH
RCH2OH
有关物质的转化关系如图所示,请回答以下问题:
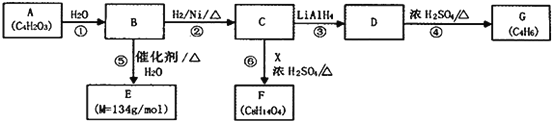
(1)C中所含官能团的名称是 ____________;④的反应类型是 _________反应。
(2)G的结构简式为 _____________。
(3)反应②的化学方程式为 _____________。
(4)若E在一定条件下发生缩聚反应生成高分子化合物,写出其中两种的结构简式: __________。
(5)反应⑥的化学方程式为 __________。
(6)有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,写出所有符合条件的Y的结构简式:_________。
【答案】羧基 消去 CH2=CHCH=CH2 HOOCCH=CHCOOH+H2![]() HOOCCH2CH2COOH;
HOOCCH2CH2COOH; 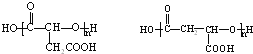 HOOCCH2CH2COOH+2C2H5OH
HOOCCH2CH2COOH+2C2H5OH![]() CH3CH2OOCCH2CH2COOCH2CH3+2H2O
CH3CH2OOCCH2CH2COOCH2CH3+2H2O 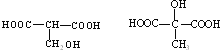
【解析】
A是一种五元环状化合物,其核磁共振氢谱只有一个峰,说明A中只含一种类型的H原子,A能水解生成B,B能和氢气发生加成反应生成C,说明C中含有碳碳双键,结合题给信息和A的分子式知,A的结构简式为: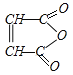 ,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2。
,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2。
根据上述分析可知A为: ,B为HOOCCH=CHCOOH,C为HOOCCH2CH2COOH,D为HOCH2CH2CH2CH2OH,E为:HOOCCH2CH(OH)COOH,F为CH3CH2OOCCH2CH2COOCH2CH3,G为CH2=CHCH=CH2,X是乙醇。
,B为HOOCCH=CHCOOH,C为HOOCCH2CH2COOH,D为HOCH2CH2CH2CH2OH,E为:HOOCCH2CH(OH)COOH,F为CH3CH2OOCCH2CH2COOCH2CH3,G为CH2=CHCH=CH2,X是乙醇。
(1)C的结构简式为:HOOCCH2CH2COOH,分子中含有羧基;反应④是D发生消去反应生成G;
(2)通过以上分析知,G的结构简式为:CH2=CHCH=CH2;
(3)B和氢气发生加成反应生成C,反应方程式为HOOCCH=CHCOOH+H2![]() HOOCCH2CH2COOH;
HOOCCH2CH2COOH;
(4)E的结构简式为:HOOCCH2CH(OH)COOH,E能发生缩聚反应,其生成物的结构简式为: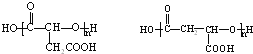 ;
;
(5)1、4-丁二酸和乙醇发生酯化反应,反应方程式为HOOCCH2CH2COOH+2C2H5OH![]() CH3CH2OOCCH2CH2COOCH2CH3+2H2O;
CH3CH2OOCCH2CH2COOCH2CH3+2H2O;
(6)有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,符合条件的有: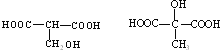 。
。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A. 高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B. 室温下,1 L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向25 mL 0.1 mol.L-1NaOH溶液中逐滴滴加0.2 mol.L-1的HN3(叠氮酸)溶液,pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7)。下列说法正确的是

A. 水电离出的c(H+):A点小于B点
B. 在B点,离子浓度大小为c(OH-)>c(H+)>c (Na+)>c(N3-)
C. 在C点,滴加的V(HN3)=12.5 mL
D. 在D点,c(Na+)=2c(HN3)+2 c(N3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物M是合成香精的重要原料。实验室由A和芳香烃E制备M的一种合成路线如下:
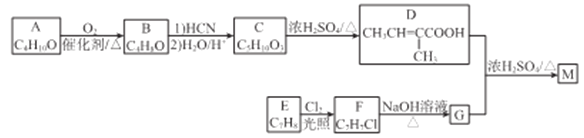
已知: (R1、R2表示烃基或H原子)
(R1、R2表示烃基或H原子)
请回答下列题:
(1)A的化学名称为_________,B的结构简式为________。
(2)C中官能团的名称为________。
(3)D分子中最多有___个原子共平面。
(4)E→F的反应类型为________。
(5)D+G→M的化学方程式为________。
(6)同时满足下列条件的D的同分异构体有___种(不考虑立体异构),其中核磁共振氢谱有3组峰的结构简式为________。
①能发生水解反应和银镜反应; ②不含环状结构
(7)参照上述合成路线和信息。以![]() 为原料(其他无机试剂任选),设计制备
为原料(其他无机试剂任选),设计制备 的合成路线_______________________。
的合成路线_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式_____________。
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用图中的曲线表示是________(填序号).

(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.则反应的离子方程式是 _________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示.请回答下列问题.
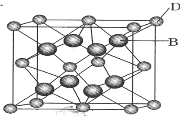
(1)E元素原子基态时的电子排布式为_________.
(2)A2F分子中F原子的杂化类型是_________
(3)CA3极易溶于水,其原因主要是_________,
(4)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为_________;1molC60分子中σ键的数目为_________.

(5)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜铟硒薄膜电池等.
①第一电离能:As_________Se(填“>”“<”或“=”).
②硫化锌的晶胞中(结构如图所示),硫离子的配位数是_________与S距离最近且等距离的S之间的距离为_________(密度为ρg/cm3)
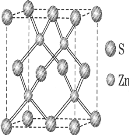
③二氧化硒分子的空间构型为_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在人类的生产和生活中有着广泛的应用,某化学兴趣小组利用图一装置探究氨气的有关性质。
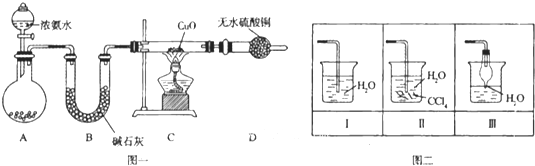
(1)装置A中烧瓶内试剂可选用 (填序号)。B的作用是
a.碱石灰 b.浓硫酸 c.生石灰 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 ,.该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,所得溶液的物质的量浓度为 mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应过程中不存在电子转移的是( )
A.Zn+2HCl=ZnCl2+H2↑
B.Ca(ClO)2+2HCl=CaCl2+2HClO
C.Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O
D.3Cl2+6KOH(浓)![]() 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是( )
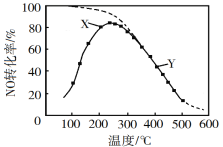
A.反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B.图中X点所示条件下,延长反应时间不能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K>2000
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com