



科目:高中化学 来源: 题型:
| A、HNO3是氧化剂,NO2是氧化产物 |
| B、还原剂与氧化剂的物质的量比是1:2 |
| C、若2mol Cu完全反应,则反应中共转移了NA个电子 |
| D、氧化产物和还原产物的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气的水溶液能导电,所以氯气属于电解质 |
| B、稀H2SO4溶液能导电,稀H2SO4是电解质 |
| C、由于NH3?H2O溶于水,而Ca(OH)2微溶于水,所以NH3?H2O是强电解质,Ca(OH)2是弱电解质 |
| D、硫酸钡难溶于水,但硫酸钡属于强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
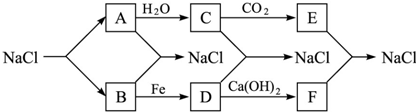
查看答案和解析>>
科目:高中化学 来源: 题型:
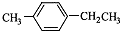 )是一种重要的有机原料,用该物质可合成其他物质.
)是一种重要的有机原料,用该物质可合成其他物质.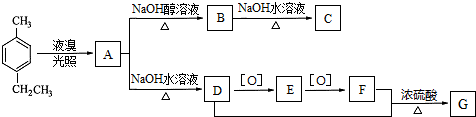
查看答案和解析>>
科目:高中化学 来源: 题型:
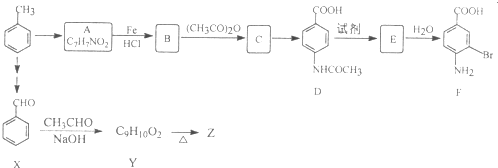
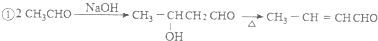
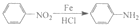 苯胺中氨基易被氧化.
苯胺中氨基易被氧化.查看答案和解析>>
科目:高中化学 来源: 题型:
| ①溶解 |
| ②加入NaOH |
| ③加入() |
| ④加入() |
| ⑤过滤 |
| ⑥加入() |
| ⑦() |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com