
【题目】某浅黄色固体XY和焦炭混合,加强热。发生如下反应:

先通入氮气。然后点燃Ⅰ、Ⅲ酒精灯,实验中观察到Ⅰ生成银白色金属,Ⅱ、Ⅳ中溶液变浑浊。Ⅲ中黑色粉未变红色粉末。下列推断不正确的是
A. 开始通入氮气的目的是排尽装置中的空气
B. XY与焦炭在高温下反应生成CO2和CO
C. X可能是钠,Y一定是氧元素
D. 用燃烧法处理Ⅳ排放的尾气
科目:高中化学 来源: 题型:
【题目】在铜锌原电池中,锌电极上发生的反应为Zn-2e-=Zn2+,则( )
A. 锌电极为负极 B. 锌电极为正极
C. 电子从铜电极流向锌电极 D. 反应中Zn被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷。若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
A.CH3CH2CH2CH2CH2OH B.(CH3)2COHCH2CH3
C.(CH3)2CHCH2CH2OH D.(CH3)3CCH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S转化是环保和资源利用的研究课题。將烧碱吸收H2S后的溶液加人如图装置,可以回收单质硫,甲为二甲醚(CH3OCH3)一空气燃料电池。
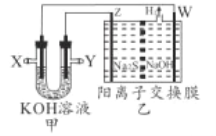
下列推断正确的是
A. Y极充入二甲醚 B. 电子由X![]() W
W![]() 溶液
溶液![]() Z
Z![]() Y
Y
C. Z极反应式为S2--2e-=S D. 电解后,乙装置右池中c(NaOH)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】形成酸雨的原理之一可简单表示如下:
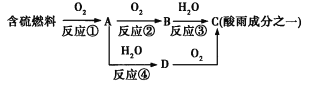
回答下列问题:
(1)酸雨的pH__________(填“ > ”、“ < ”或“ =”)5.6。
(2)D物质的化学式为__________。
(3)反应②的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬合金具有高硬度、耐腐蚀特性,广泛应用于精密仪器制造,由高碳铬铁合金废料制取铬的简单流程如下:
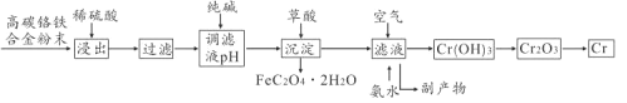
已知:Cr+H2SO4=CrSO4+H2↑
请回答下列问题:
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有_____ (写一条即可)
(已知: ![]() )
)
(2)用纯碱调节溶液酸度,若纯碱过量,则可能导致的后果是______,副产物中两种主要物质的化学式为_____________
(3)加入草酸发生反应的离子方程式为______;利用铝热反应冶炼铬。请写出该反应的化学方程式_________
(4)向滤液中通入空气,加入氨水后发生反应的化学方程式为_________
(5)利用如图装置,探究铬和铁的活泼性强弱。
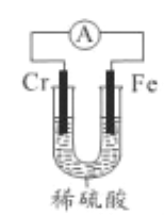
能证明铁比铬话泼的实验现象是______,工业上,在钢器具表面镀铬,用硫酸铬(CrSO4)溶液作电解液,阴极的电极反应式为___________。
(6)已知高碳铬铁度料中铁铭元素质量比为14:13.上述流程中铁元素转化草酸亚铁的利用率为80%。废料中提取金属铬的总转化率为95%,如果得到草酸亚铁品体(FeC2O4·2H2O)质量为18.00吨,则可以冶炼铬的质量为____吨(结果保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CH4催化还原NOx可以消除氮氧化物的污染。
已知CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1。若在标准状况下4.48 L CH4恰好能将一定量NO2还原成N2和H2O(g),则整个过程中放出的热量为( )
A. 173.4 kJ B. 232 kJ C. 368.8 kJ D. 114.8 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A. 达到化学平衡状态时,4v正(O2)=5v逆(NO)
B. 若单位时间内生成xmol NO的同时,消耗xmol NH3,则反应达到化学平衡状态
C. 达到化学平衡状态后,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率的关系为2v正(NH3)=3v正(H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com