
【题目】已知高能锂离子电池的总反应式为2Li+FeS=Fe+Li2S,LiPF6·SO(CH3)2为电解质,用该电池为电源电解含镍酸性废水并得到单质Ni的实验装置如图所示。下列说法错误的是
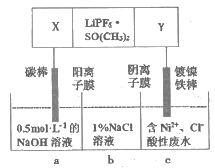
A. 电极Y应为Li
B. X极反应式为FeS+2Li++2e-=Fe+Li2S
C. 电解过程中,b中NaCl溶液的物质的量浓度将不断减小
D. 若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
【答案】C
【解析】
本题主要考查原电池与电解池串联问题。通过总反应可知,Li发生氧化反应,作负极,FeS发生还原反应,作正极;因c中由Ni2+生成单质Ni,即发生还原反应,故Y极为负极,X为正极。
A.由上述分析可知,Y为原电池负极,故Y为Li,选项A正确;
B.X极为正极,FeS发生还原反应,故电极反应式为: FeS+2Li+ +2e- =Fe+Li2S,选项B正确;
C.电解过程中,a为阳极区,发生氧化反应: 4OH--4e- =2H2O+O2↑, a中Na+通过阳离子交换膜进入b中;C中发生还原反应: Ni2+ +2e-=Ni,溶液中Cl-通过阴离子交换膜进入b中。故电解过程中, b中NaCl的物质的量浓度将不断增大,选项C错误;
D.若将阳离子交换膜去掉,因b中含有C1-,故阳极电极反应式为: 2C1--2e-=Cl2↑,故电解反应总方程式发生改变,选项D正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铝广泛应用于航空、建筑、汽车等行业,目前工业上采用电解氧化铝和冰晶石(Na3AlF6)混合物的方法制取铝。回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图
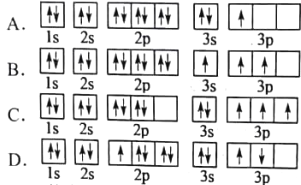
其中能量最低的是___________(填字母),电子由状态C到状态B所得原子光谱为___________光谱(填“发射”或“吸收”),状态D是铝的某种激发态,但该电子排布图有错误,主要是不符合____________________________________________。
(2)熔融状态的氯化铝可挥发出二聚分子Al2Cl6,其结构如图所示。
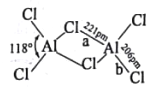
①a键的键能_________b键的键能(填“>”“<”或“=”),其理由是______________________。
②Al2Cl6中铝原子的杂化方式为___________;AlCl3的空间结构为 ___________________。
(3)冰晶石属于离子化合物,由Na+和AIF63-组成,在冰晶石的晶胞中,AlF63-占据的位置相当于氯化钠晶胞中Cl-的位置。
①冰晶石的化学式为___________,一个冰晶石晶胞中Na+的个数为___________。
②已知冰晶石的密度为2.95g/cm3,则冰品石晶胞的边长a=___________pm(列出算式即可,阿伏加德罗常数值为6.02×1023)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是:
A. 将铜丝插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe===2Fe2+
C. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种氧气吸收剂,为红棕色晶体,易被氧化,不溶于水和乙醚(易挥发的有机溶剂),微溶于乙醇,易溶于盐酸,其制备装置如下(已知:Cr3+水溶液颜色为绿色,Cr2+水溶液颜色为蓝色):

回答下列问题:
(1)装置甲中连通管a的作用是___________。
(2)向三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液:关闭K2打开K1,旋开分液漏斗的旋塞并控制好滴速;当观察到三颈烧瓶中溶液颜色由绿色完全转变为蓝色时,进行的实验操作为______________,从而将甲中溶液自动转移至装置乙中;当观察到装置乙中出现________________________时,说明反应基本完成,此时关闭分液漏斗的旋塞。
(3)装置乙中反应的离子方程式为_____________。
(4)将装置乙中混合物快速过滤、洗涤和干燥,称量得到mg[Cr(CH3COO)2]2·2H2O。其中洗涤的目的是去除可溶性杂质和水分,下列洗涤试剂正确的使用顺序是_____(填标号。
A.乙醚 B.去氧冷的蒸馏水 C.无水乙醇
(5)若实验所取用的CrCl3溶液中含溶质ng,则[Cr(CH3COO)2]2·2H2O(相对分子质量为376 )的产率是___________。
(6)该实验装置有一个明显的缺陷是________,解决此缺陷的措施为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列几组化合物,所含化学键类型不完全相同的是( )
A.NH3、H2O、CH3COOH
B.NH3、HNO3、CH3CH2OH
C.CH3COONH4、NH3、Na2O2
D.CaCl2、NaH、Na2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室需要配制500mL 0.10mol/L Na2CO3溶液.

(1)所需玻璃仪器有:玻璃棒、烧杯、100mL量筒、________、________
(2)实验时图中所示操作的先后顺序为________(填编号)
(3)在配制过程中,下列操作对所配溶液浓度有无影响?(填“偏高”、“偏低”或“无影响”)
①称量时误用“左码右物”________ ②转移溶液后没有洗涤烧杯和玻璃棒________
③向容量瓶加水定容时俯视液面________ ④摇匀后液面下降,再加水至刻度线________
(4)所需Na2CO3固体的质量为____g;若改用浓溶液稀释,需要量取2mol/L Na2CO3溶液________mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,对可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是( )
3C(g)的下列叙述中,能说明反应已达到平衡的是( )
A. C生成的速率与C分解的速率相等
B. 单位时间内消耗amolA,同时生成3amolC
C. 容器内的压强不再变化
D. 混合气体的物质的量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简单原子的原子结构可用下图形象地表示:

其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是
a.①②③互为同位素 b.①②③互为同素异形体 c.①②③具有相同的质量数
d.①②③是三种化学性质不同的粒子 e.①②③具有相同的质量 f.①②③是三种不同的原子
A. e、fB. b、cC. d、eD. a、f
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com