
【题目】二乙酸—1,4—环己二醇酯可通过下列路线合成:
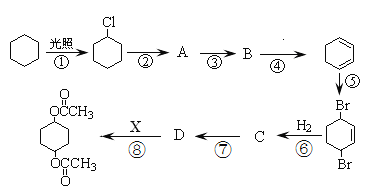
(1)化合物的结构简式:B___;D___。
(2)上述合成过程中没有涉及的反应类型是___。
A.加成 B.消去 C.取代 D.氧化 E.聚合 F.酯化
(3)反应④和反应⑧的反应条件:④___;⑧___。
(4)写出②的反应方程式___;写出⑤的反应方程式___。
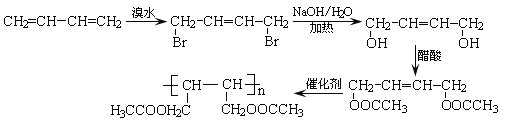
(5)请设计合理的方案以CH2=CH—CH=CH2(1,3—丁二烯)和醋酸为原料合成 (用合成路线流程图表示,并注明反应条件)___。
(用合成路线流程图表示,并注明反应条件)___。
提示:①合成过程中无机试剂任选;②合成路线流程图示例如:
CH3CH2OH![]() H2C=CH2
H2C=CH2
【答案】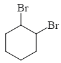
![]() DE NaOH的醇溶液,加热 乙酸、浓硫酸,加热
DE NaOH的醇溶液,加热 乙酸、浓硫酸,加热 ![]() +NaOH
+NaOH![]() +NaCl+H2O
+NaCl+H2O ![]() +Br2
+Br2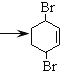
【解析】
环己烷在光照条件发生取代反应生成![]() ,由
,由![]() 制备
制备 ![]() ,可以先由
,可以先由![]() 发生消去反应生成A,则A应为
发生消去反应生成A,则A应为![]() ;A再与溴发生加成反应生成B为
;A再与溴发生加成反应生成B为 ;B再发生消去反应生成
;B再发生消去反应生成![]() ;
;![]() 与溴发生1,4加成生成
与溴发生1,4加成生成![]() ,之后与氢气发生加成反应生成C为
,之后与氢气发生加成反应生成C为![]() ;根据最终产物可推测D应为醇,X为CH3COOH,所以C到D为卤代烃的水解反应,D的结构简式为
;根据最终产物可推测D应为醇,X为CH3COOH,所以C到D为卤代烃的水解反应,D的结构简式为![]() 。
。
(1)根据分析可知B为 ,D为
,D为![]() ;
;
(2)反应①为取代反应,反应②、④为消去反应,反应⑥为加成反应,反应⑧为酯化反应,所以没有涉及氧化反应和聚合反应,故选DE;
(3)反应④为卤代烃的消去反应,反应条件为NaOH的醇溶液、加热;反应⑧为D与乙酸的酯化反应,反应条件为乙酸、浓硫酸,加热;
(4)反应②为氯代烃的消去反应,化学方程式为![]() +NaOH
+NaOH![]() +NaCl+H2O;
+NaCl+H2O;
反应⑤为![]() 与溴发生1,4加成,化学方程是式为img src="http://thumb.zyjl.cn/questionBank/Upload/2020/07/21/23/187b9b2b/SYS202007212347590152116663_DA/SYS202007212347590152116663_DA.005.png" width="45" height="45" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />+Br2
与溴发生1,4加成,化学方程是式为img src="http://thumb.zyjl.cn/questionBank/Upload/2020/07/21/23/187b9b2b/SYS202007212347590152116663_DA/SYS202007212347590152116663_DA.005.png" width="45" height="45" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />+Br2 ;
;
(5)该高聚物可以由![]() 发生聚和反应生成,而该物质可以由
发生聚和反应生成,而该物质可以由![]() 和CH3COOH发生酯化反应生成,
和CH3COOH发生酯化反应生成,![]() 可以由
可以由![]() 水解生成,
水解生成,![]() 可以由CH2=CH—CH=CH2与溴发生1,4加成生成,所以合成路线为
可以由CH2=CH—CH=CH2与溴发生1,4加成生成,所以合成路线为 。
。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】如图是可逆反应![]() 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
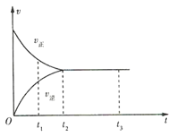
A.t1时,反应只向正方向进行B.t2时,反应未达到限度
C.t2~t3,反应已停止D.t2~t3,各物质的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
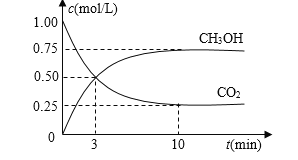
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____mol/(L·min)。
②该反应的平衡常数表达式为K=_________。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案_______(填“是”、“否”)可行,理由是:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为![]() 。下列说法正确的是
。下列说法正确的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1![]()
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2![]()
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 锶(Sr)原子序数为 38,在周期表中的位置为_____关于锶及其化合物的说法中不正确的是_________
a. 锶能与冷水剧烈反应
b. 锶的失电子能力比钙强
c. Sr(OH)2 的碱性比 Ca(OH)2 弱
d. 氧化锶是碱性氧化物
II.高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,61℃时晶体开始失去结晶水,100℃时失去全部结晶水。用工业碳酸锶粉末(含少量 Ba、Fe 的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。
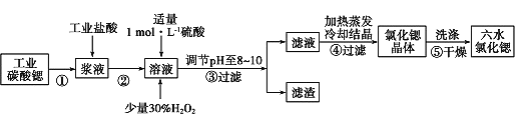
请回答:
(1)已知常温下,NaCl 溶液、BaCl2 溶液呈中性,而 MgCl2 、CuCl2 溶液呈酸性。常温下,SrCl2 溶液 pH_____7(填“大于”、“等于”或“小于”);
(2)步骤③所得滤渣的主要成分是_________(填化学式),调节溶液 pH 至 8~10,宜选用的试剂为_____。
a.稀硫酸 b.氢氧化锶粉末 c.氢氧化钠 d.氧化锶粉末
(3)步骤⑤中,洗涤氯化锶晶体最好选用_____。
a.水 b.稀硫酸 c.氢氧化钠溶液 d.氯化锶饱和溶液
(4)工业上用热风吹干六水氯化锶,选择的适宜温度范围是_____(填字母)。
a.50~60℃ b.70~80℃ c.80~100℃ d.100℃以上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=13的两种碱溶液M、N各1mL,分别加水稀释到1000mL,其pH与溶液体积(V/mL)的关系如图所示,下列说法正确的是( )
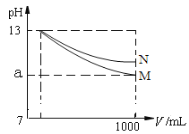
A.M、N两种碱溶液的物质的量浓度一定相等
B.稀释后,M溶液的碱性比N溶液强
C.若10<a<13,则M、N都是弱碱
D.若a=10,则M是强碱,N不一定是弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺![]() 的性质与氨相似,
的性质与氨相似,![]() 也是一元弱碱,
也是一元弱碱,![]() 时电离常数
时电离常数![]() 。现用
。现用![]() 的稀硫酸滴定
的稀硫酸滴定![]() 的甲胺溶液,溶液中
的甲胺溶液,溶液中![]() 的负对数pOH与所加稀硫酸的体积
的负对数pOH与所加稀硫酸的体积![]() 的关系如图所示,下列说法正确的是( )
的关系如图所示,下列说法正确的是( )
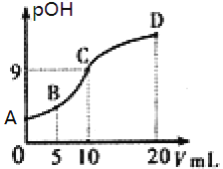
A.B点溶液中存在![]()
B.甲胺在水中的电离方程式为:![]()
C.A、B、C三点溶液中,由水电离出来的![]() :
:![]()
D.C点所在溶液中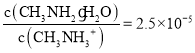
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】80℃时,1L 密闭容器中充入0.20 mol N2O4,发生反应N2O4![]() 2NO2 △H = + Q kJ·mol﹣1(Q>0),获得如下数据:
2NO2 △H = + Q kJ·mol﹣1(Q>0),获得如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L﹣1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
下列判断正确的是
A. 升高温度该反应的平衡常数K减小
B. 20~40s 内,v(N2O4)= 0.004 mol·L-1·s-1
C. 100s时再通入0.40 mol N2O4,达新平衡时N2O4的转化率增大
D. 反应达平衡时,吸收的热量为0.15Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() 在一定条件下与
在一定条件下与![]() 反应转化为甲醇
反应转化为甲醇![]() 是变废为宝的好方法,一定条件下,每转化
是变废为宝的好方法,一定条件下,每转化![]() 放出的热量为
放出的热量为![]() ,
,![]() 转化为甲醇过程中浓度随时间的变化曲线如图所示
转化为甲醇过程中浓度随时间的变化曲线如图所示![]() 已知反应物和生成物在此条件下均为气体
已知反应物和生成物在此条件下均为气体![]() ,下列叙述中正确的是
,下列叙述中正确的是

A.在进行到3分钟时,![]() 和
和![]() 所表达的反应速率值相等,均为
所表达的反应速率值相等,均为![]()
B.此反应的热化学方程式为:![]()
C.此条件下反应的平衡常数为![]()
D.降低温度,此反应的平衡常数可能为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com