
ЁОЬтФПЁПГЃЮТЯТЃЌгУ0.10 molЁЄL-1NaOH ШмвКЗжБ№ЕЮЖЈ20.00mL ХЈЖШОљЮЊ0.10 molЁЄL-1CH3COOHШмвККЭHCNШмвКЫљЕУЕЮЖЈЧњЯпШчгвЭМЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ

A. ЕуЂкКЭЕуЂлЫљЪОШмвКжаЖМгаЃКc(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B. ЕуЂйКЭЕуЂкЫљЪОШмвКжаЃКc(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
C. ЕуЂлКЭЕуЂмЫљЪОШмвКжаЃКc(Na+)ЃОc(OH-)ЃОc(CH3COO-)ЃОc(H+)
D. ЕуЂйКЭЕуЂкЫљЪОШмвКжаЃКc(CH3COO-)ЃМc(CN-)
ЁОД№АИЁПB
ЁОНтЮіЁПA. ЕуЂкКЭЕуЂлЫљЪОШмвКжаЕчКЩЪиКуЃКc(CH3COO-)+c(OH-)=c(Na+)+c(H+)ЃЌЕуЂкЫљЪОШмвКжаЃЌCH3COOHЕФ1/2зЊЛЏЮЊCH3COONaЃЌгЩгкpH<7ЃЌЫљвдCH3COOHЕФЕчРыГЬЖШДѓгкCH3COONaЕФЫЎНтГЬЖШЃЌc(CH3COO-)>c(Na+)>c(CH3COOH)ЃЌвђДЫЃЌc(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+)ЃЌЕуЂлЫљЪОШмвКжаЃЌpH=7ЃЌc(OH-)=c(H+)ЃЌЫљвдc(CH3COO-)=c(Na+)ЃЌc(Na+)>c(CH3COOH)ЃЌвђДЫЃЌc(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+)ЃЌЙЪAДэЮѓЃЛB. ЕуЂйКЭЕуЂкЫљЪОШмвКжаЃКc(CH3COO-)+c(CH3COOH)=c(CN-)+c(HCN)ЃЌМДc(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)ЃЌЙЪBе§ШЗЃЛC. ЕуЂлЫљЪОШмвКжаc(OH-)=c(H+)ЃЌЕуЂмЫљЪОШмвКжаCH3COONaЫЎНтГЬЖШКмаЁЃЌЫљвд c(OH-)<c(CH3COO-)ЃЌЙЪCДэЮѓЃЛ D. ЕуЂйКЭЕуЂкЫљЪОШмвКжаЃКc(CH3COO-)+c(CH3COOH)=c(CN-)+c(HCN)ЃЌЖјЧввЛАыЫсзЊЛЏЮЊбЮЃЌЕуЂйЫљЪОШмвКpH>7ЫЕУїCN-ЕФЫЎНтГЬЖШДѓгкHCNЕФЕФЕчРыГЬЖШЃЌc(HCN)>c(CN-)ЃЌЕуЂкЫљЪОШмвКpH<7ЃЌЫЕУїCH3COOHЕФЕчРыГЬЖШДѓгкCH3COONaЕФЫЎНтГЬЖШЃЌЫљвдc(CH3COO-)>c(CH3COOH)ЃЌвђДЫЃЌc(CH3COO-)>c(CN-)ЃЌЙЪDДэЮѓЁЃЙЪбЁBЁЃ


 УћаЃПЮЬУЯЕСаД№АИ
УћаЃПЮЬУЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
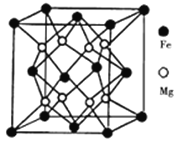
ЁОЬтФПЁПУОЁЂЬњЁЂЭЕШдкЙЄХЉвЕЩњВњжагазХЙуЗКЕФгІгУЁЃЛиД№ЯТСаЮЪЬт:
ЃЈ1ЃЉЭдЊЫиЮЛгкдЊЫижмЦкБэжаЕФ___ЧјЃЌЦфЛљЬЌдзгЕФМлЕчзгХХВМЭМЮЊ_________ЁЃ
ЃЈ2ЃЉЭљСђЫсЭШмвКжаМгШыЙ§СПАБЫЎЃЌПЩаЮГЩ[Cu(NH3)4]SO4ШмвКЃЌИУШмвКПЩгУгкШмНтЯЫЮЌЫиЁЃ
Ђй[Cu(NH3)4]SO4жавѕРызгЕФСЂЬхЙЙаЭЪЧ_______ЁЃ
Ђкдк[Cu(NH3)4]SO4жаЃЌХфРызгЫљКЌгаЕФЛЏбЇМќЮЊ________ЃЌЬсЙЉЙТЕчзгЖдЕФГЩМќдзгЪЧ_______ЁЃ
Ђл çѐдЊЫиЭтЃЌ[Cu(NH3)4]SO4жаЫљКЌдЊЫиЕФЕчИКадгЩаЁЕНДѓЕФЫГађЮЊ_______ЁЃ
ЂмNF3гыNH3ЕФПеМфЙЙаЭЯрЭЌЃЌжааФдзгЕФЙьЕРдгЛЏРраЭОљЮЊ_____ЁЃЕЋNF3ВЛвзгыCu2+аЮГЩЛЏбЇМќЃЌЦфдвђЪЧ____________ЁЃ
ЃЈ3ЃЉЬњУОКЯН№ЪЧФПЧАвбЗЂЯжЕФДЂЧтУмЖШзюИпЕФДЂЧтВФСЯжЎвЛЃЌЦфОЇАћНсЙЙШчЭМЫљЪОЁЃдђЬњУОКЯН№ЕФЛЏбЇЪНЮЊ________ЃЌШєИУОЇАћЕФВЮЪ§ЮЊdnm,дђИУКЯН№ЕФУмЖШЮЊ____ g/cm3(ВЛБиЛЏМђЃЌгУNAБэЪОАЂЗќМгЕТТоГЃЪ§)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУ1L1molLЉ1NaOHШмвКЮќЪе0.6molCO2 ЃЌ ЫљЕУШмвКжаNa2CO3КЭNaHCO3ЕФЮяжЪЕФСПжЎБШдМЮЊЃЈ ЃЉ
A.2ЃК3
B.1ЃК2
C.2ЃК1
D.3ЃК2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбаОПадбЇЯАаЁзщЭЈЙ§ЯТСаЗДгІдРэжЦБИSO2ВЂНјаааджЪЬНОПЁЃЗДгІдРэЮЊЃКNa2SO3(ЙЬ)+H2SO4(ХЈ)ЃН Na2SO4 + SO2Ёќ+ H2O

ЃЈ1ЃЉИљОнЩЯЪідРэжЦБИВЂЪеМЏИЩдяSO2ЕФЪЕбщзАжУСЌНгЫГађЮЊ________________ЁЃ(ЬюНгЭЗађКХ)
ЃЈ2ЃЉDжаЪЂзАЕФЪдМСЮЊ_________________ЁЃ
ЃЈ3ЃЉМзЭЌбЇгУзЂЩфЦїЮќШЁДПОЛЕФSO2ВЂНсКЯзАжУGНјааSO2ЕФаджЪЪЕбщЃЌШєXЪЧNa2SШмвКЃЌЦфФПЕФЪЧМьбщSO2ЕФ_____________ЃЌПЩЙлВьЕНЕФЯжЯѓ_________ ЁЃ
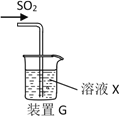
ЃЈ4ЃЉЪЕбщ1ЃКввЭЌбЇНЋШмвКXЛЛЮЊХЈЖШОљЮЊ0.1mol/L Fe(NO3)3КЭBaCl2ЕФЛьКЯШмвКЃЈвбОГ§ШЅШмНтбѕЃЉЃЌЭЈШыЩйСПSO2КѓЙлВьЕНЩеБВњЩњАзЩЋГСЕэЃЌввЭЌбЇШЯЮЊАзЩЋГСЕэЮЊBaSO4ЃЌЮЊЬНОПАзЩЋГСЕэЕФГЩвђЃЌЫћМЬајНјааШчЯТЪЕбщбщжЄЃКЃЈвбжЊЃК0.1mol/L Fe(NO3) 3ЕФpH=2ЃЉ
ЪЕбщ | Вйзї | ЯжЯѓ | НсТлКЭНтЪЭ |
2 | НЋSO2ЭЈШы0.1mol/L ____КЭBaCl2ЛьКЯвК | ВњЩњАзЩЋГСЕэ | Fe3+ФмбѕЛЏH2SO3 |
3 | НЋSO2ЭЈШы_______ КЭ BaCl2ЛьКЯвК | ВњЩњАзЩЋГСЕэ | ЫсадЬѕМўNO3-ФмНЋH2SO3бѕЛЏЮЊSO42- |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагаЙибцЩЋЗДгІЕФЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉ
A.ЙлВьK2SO4ЕФбцЩЋгІЭИЙ§РЖЩЋЕФюмВЃСЇ
B.NaгыNaClдкзЦЩеЪБЛ№бцбеЩЋЯрЭЌ
C.ПЩвдгУбцЩЋЗДгІРДЧјБ№NaClКЭKCl
D.бцЩЋЗДгІвЛЖЈЗЂЩњЛЏбЇБфЛЏ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПДгКЃЫЎЕУЕНЕФДжЪГбЮЫЎжаГЃКЌCa2+ЁЂMg2+ЁЂSO42ЁЊ![]() ЃЌашвЊЗжРыЬсДПЁЃЯжгаКЌЩйСПCaCl2ЁЂMgSO4ЕФДжЪГбЮЫЎЃЌдкГ§ШЅаќИЁЮяКЭФрЩГжЎКѓЃЌвЊгУ4жжЪдМСЃКЂйбЮЫсЁЂЂкNa2CO3ЁЂЂлNaOHЁЂЂмBaCl2РДГ§ШЅЪГбЮЫЎжаЕФCa2+ЁЂMg2+ЁЂSO42ЁЊ
ЃЌашвЊЗжРыЬсДПЁЃЯжгаКЌЩйСПCaCl2ЁЂMgSO4ЕФДжЪГбЮЫЎЃЌдкГ§ШЅаќИЁЮяКЭФрЩГжЎКѓЃЌвЊгУ4жжЪдМСЃКЂйбЮЫсЁЂЂкNa2CO3ЁЂЂлNaOHЁЂЂмBaCl2РДГ§ШЅЪГбЮЫЎжаЕФCa2+ЁЂMg2+ЁЂSO42ЁЊ![]() ЁЃЬсДПЪБЕФВйзїВНжшКЭМгШыЪдМСЕФЧщПіШчЭМЁЃ
ЁЃЬсДПЪБЕФВйзїВНжшКЭМгШыЪдМСЕФЧщПіШчЭМЁЃ

ЭМжаaЁЂbЁЂcЁЂdЗжБ№БэЪОЩЯЪі4жжЪдМСжаЕФвЛжжЃЌЧыЛиД№ЃК
ЃЈ1ЃЉГСЕэAЕФУћГЦЪЧ________ЁЃ
ЃЈ2ЃЉЪдМСdЪЧ________ЃЛХаЖЯЪдМСdвбОзуСПЕФЗНЗЈЪЧ____________________ЁЃ
ЃЈ3ЃЉМгШыbЁЂcКѓШмвКжаЗЂЩњЕФЛЏбЇЗДгІЕФЛЏбЇЗНГЬЪНга__________________________(ШЮаДСНИі)ЁЃ
ЃЈ4ЃЉЯжгаЯТСавЧЦїЃЌЙ§ТЫГіГСЕэAЁЂBЁЂCЪББиаыгУЕНЕФЪЧ____(ЬюађКХ)ЃЌвЧЦїЂлЕФУћГЦЪЧ______ЁЃ

ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
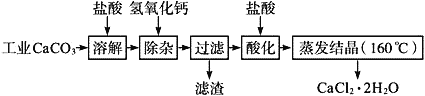
ЁОЬтФПЁПвНгУТШЛЏИЦПЩгУгкЩњВњВЙИЦЁЂПЙЙ§УєКЭЯћбзЕШЃЌвдЙЄвЕЬМЫсИЦЃЈКЌЩйСПNa+ЁЂAl3+ЁЂFe3+ЕШдгжЪ)ЩњВњвНвЉМЖЖўЫЎКЯТШЛЏИЦ(CaCl2ЁЂ2H2OЕФжЪСПЗжЪ§ЮЊ97.0%ЁЋ103.0%)ЕФжївЊСїГЬШчЯТЃК
вбжЊЃК
ЧтбѕЛЏЮя | FeЃЈOHЃЉ3 | AlЃЈOHЃЉ3 | AlЃЈOHЃЉ3 | |
ПЊЪМГСЕэЪБЕФpH | 2.3 | 4.0 | ПЊЪМШмНтЪБЕФpH | 7.8 |
ЭъШЋГСЕэЪБЕФpH | 3.7 | 5.2 | ЭъШЋШмНтЪБЕФpH | 10.8 |
ЃЈ1ЃЉCaCO3гыбЮЫсЗДгІЕФРызгЗНГЬЪН___________ЁЃ
ЃЈ2ЃЉЁАГ§дгЁБВйзїЪЧМгШыЧтбѕЛЏИЦЃЌЕїНкШмвКЕФpHЗЖЮЇЮЊ________ЃЌФПЕФЪЧГ§ШЅШмвКжаЕФЩйСПAl3+ЁЂFe2+ЁЃ
ЃЈ3ЃЉЙ§ТЫЪБашгУЕФБШВЃСЇЦїга__________ЁЃ
ЃЈ4ЃЉЁАЫсЛЏЁБВйзїЪЧМгШыбЮЫсЃЌЕїНкШмвКЕФpHдМЮЊ4.0ЃЌЦфФПЕФгаЃКЂйЗРжЙЧтбѕЛЏИЦЮќЪеПеЦјжаЕФЖўбѕЛЏЬМЃЛЂкЗРжЙCa2+дкеєЗЂЪБЫЎНтЃЛЂл_______ЁЃ
ЃЈ5ЃЉеєЗЂНсОЇвЊБЃГждк160ЁцЕФдвђЪЧ__________ЁЃ
ЃЈ6ЃЉВтЖЈбљЦЗжаCl-КЌСПЕФЗНЗЈЪЧЃКГЦШЁ0.750 0 gCaCl2ЁЄ2H2OбљЦЗЃЌШмНтЃЌдк250 mLШнСПЦПжаЖЈШнЃЛСПШЁ25.00 mLД§ВтШмвКгкзЖаЮЦПжаЃЛгУ0.050 00 mol/L AgNO3ШмвКЕЮЖЈжСжеЕуЃЈгУK2Cr2O2ЃЉЃЌЯћКФAgNO3ШмвКЬхЛ§ЕФЦНОљжЕЮЊ20.39 mLЁЃ
ЂйЩЯЪіВтЖЈЙ§ГЬжаашгУШмвКШѓЯДЕФвЧЦїга________ЁЃ
ЂкМЦЫуЩЯЪібљЦЗжаCaCl2ЁЄ2H2OЕФжЪСПЗжЪ§ЮЊ_______ЁЃЃЈБЃСєЫФЮЛгааЇЪ§зжЃЉ
ЂлШєгУЩЯЪіЗНЗЈВтЖЈЕФбљЦЗжаCaCl2ЁЄ2H2OЕФжЪСПЗжЪ§ЦЋИп(ВтЖЈЙ§ГЬжаВњЩњЕФЮѓВюПЩКіТд)ЃЌЦфПЩФмдвђга________ЃЛ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСЂЗНЭщ(C8H8)ЭтЙлЮЊгаЙтдѓЕФОЇЬхЁЃЦфАЫИіЬМдзгЖдГЦЕиХХСадкСЂЗНЬхЕФАЫИіНЧЩЯЁЃвдЯТЯрЙиЫЕЗЈДэЮѓЕФЪЧ
A. СЂЗНЭщдкПеЦјжаПЩШМЃЌШМЩегаКкбЬВњЩњ
B. СЂЗНЭщвЛбѕДњЮя1жжЁЂЖўТШДњЮяга3жжЁЂШ§ТШДњЮявВга3жж
C. СЂЗНЭщЪЧБН(C6H6)ЕФЭЌЯЕЮяЁЂвВЪЧБНввЯЉ(C6H5-CH=CH2)ЕФЭЌЗжвьЙЙЬх
D. АЫЯѕЛљСЂЗНЭщЭъШЋЗжНтПЩФмжЛВњЩњЖўбѕЛЏЬМКЭЕЊЦј
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAдЊЫиЕФвѕРызгЁЂBдЊЫиЕФвѕРызгКЭCдЊЫиЕФбєРызгОпгаЯрЭЌЕФЕчзгВуНсЙЙЁЃвбжЊAЕФдзгађЪ§ДѓгкBЕФдзгађЪ§ЁЃдђAЁЂBЁЂCШ§жждЊЫиЕФРызгАыОЖДѓаЁЫГађЪЧ(ЁЁЁЁ)
A.A>B>CB.B>A>CC.C>A>BD.C>B>A
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com