
【题目】室温下,0.1 mol·L-1某一元酸(HA)溶液中![]() =1×10-10,下列叙述正确的是
=1×10-10,下列叙述正确的是
A.溶液中水电离出的c(H+)=10-10 mol·L-1
B.溶液中c(H+)+c(A-)=0.1 mol·L-1
C.与0.05 mol·L-1 NaOH溶液等体积混合,所得混合溶液中水的电离得到促进
D.上述溶液中加入一定量NaA晶体或加水稀释,溶液的c(OH-)均增大
【答案】D
【解析】
试题分析:A、溶液中c(OH-)/c(H+)=1×10-10,Kw=c(H+)c(OH-)=1×10-14,两式中的氢离子浓度是溶液中酸电离出的,氢氧根离子浓度是水电离出的,联立解得c(H+)=0.01mol/L,确定为弱酸溶液,所以溶液中c(OH-)=10-12mol/L,即水电离出的氢离子浓度为10-12mol/L;A错误;B、0.1molL-1某一元酸(HA)溶液中存在电离平衡,所以根据物料守恒可知c(A-)+c(HA)=0.1molL-1,所以c(H+)+c(A-)=0.1molL-1是错误的,B错误;C、0.1molL-1某一元酸(HA)溶液与0.05molL-1NaOH溶液等体积混合后反应盐酸过量,所得混合溶液中水的电离仍然被抑制,C错误;D、通过计算可知酸为弱酸存在 电离平衡HA![]() H++A-,加水稀释促进电离,氢离子浓度减小,加入一定量NaA晶体,溶解生成的A-离子抑制了酸的电离,氢离子浓度减小,根据温度一定时溶液中氢离子浓度与氢氧根离子浓度乘积为常数,加入水和加入一定量NaA晶体,使氢离子浓度减小,氢氧根离子浓度增大,D正确;答案选D。
H++A-,加水稀释促进电离,氢离子浓度减小,加入一定量NaA晶体,溶解生成的A-离子抑制了酸的电离,氢离子浓度减小,根据温度一定时溶液中氢离子浓度与氢氧根离子浓度乘积为常数,加入水和加入一定量NaA晶体,使氢离子浓度减小,氢氧根离子浓度增大,D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】【2016广东模拟】一定条件下,乙烷发生分解反应:C2H6C2H4+H2.一段时间后,各物质的浓度保持不变,这说明( )
A.反应完全停止 B.反应达到平衡状态
C.反应物消耗完全 D.正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017孝义市模拟】下列储存药品的方法中,正确的是( )
A.液溴保存在带橡胶塞的玻璃瓶中
B.新制氯水保存在棕色广口瓶中
C.金属锂保存在石蜡油中
D.硅酸钠溶液保存在带磨口玻璃塞的玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3,两步反应的能量变化示意图如下:

下列说法合理的是( )
A.该反应的催化剂是NO2
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在碱性溶液中能大量共存,且溶液为无色透明的是( )
A.K+ MnO4﹣ Cl﹣ SO42﹣
B.Na+ Ba2+ NO3﹣ Cl﹣
C.Na+ SO42﹣ Cu2+ Cl﹣
D.Na+ H+ NO3﹣ SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A.增大反应物浓度,平衡正向移动,反应物的转化率一定增大
B.正、逆反应速率改变时,平衡一定发生移动
C.对于任何可逆反应,使用催化剂只改变反应速率,不影响平衡
D.增大体系压强,化学反应速率加快,化学平衡一定正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015北京理综化学】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
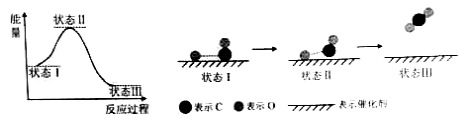
下列说法中正确的是 ( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ →状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下关于甲烷的说法中错误的是( )
A.甲烷分子具有正四面体结构
B.甲烷化学性质比较稳定,不被任何氧化剂氧化
C.甲烷分子中具有极性键
D.甲烷分子中四个C﹣H键是完全等价的键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com