
����Ŀ�������Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A.�����ȼ����Ϊ890.3KJ?mol��1 �� �����ȼ���ȵ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=��890.3 kJ?mol��1
B.500�桢30 MPa �£���0.1 mol N2 �� 0.3 mol H2 �����ܱ������г�ַ�Ӧ����NH3��g��������3.86 KJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g�� ![]() ? 2NH3��g����H=��38.6 KJ?mol��1
? 2NH3��g����H=��38.6 KJ?mol��1
C.��֪1 gҺ̬�º�����Һ̬�������ⷴӦ���ɵ�����ˮ����ʱ�ų�20.05 kJ���������º������ⷴӦ���Ȼ�ѧ����ʽΪ��N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=��641.6 KJ?mol��1
D.CO��g����ȼ������283.0 KJ?mol��1 �� ��2CO2��g���T2CO��g��+O2��g�� ��Ӧ�ġ�H=+283.0 KJ?mol��1
���𰸡�C
���������⣺A������ȼ������1mol������ȫȼ�������ȶ�������ų����������Ȼ�ѧ����ʽ��ˮ�����壬��ȷ���Ȼ�ѧ����ʽΪ������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ�� CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=��890.3 kJmol��1 �� ��A����
B����ͬ�����µ�ͬһ���淴Ӧ�����淴Ӧ��Ӧ����ֵ��ȣ������෴��0.1 mol N2 �� 0.3 mol H2 �����ܱ������г�ַ�Ӧ����NH3��g��������3.86 KJ�����ɵİ��������ʵ���С��1mol������2mol�����ֽ⣬���յ���������38.6kJ����B����
C.1 gҺ̬�µ����ʵ���Ϊ ![]() =
= ![]() mol����1molҺ̬����ȫ��Ӧ�ų�������Ϊ20.05 kJ��
mol����1molҺ̬����ȫ��Ӧ�ų�������Ϊ20.05 kJ�� ![]() =641.6kJ���÷�Ӧ�Ļ�ѧ����ʽΪN2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=��641.6 kJmol��1 �� ��C��ȷ��
=641.6kJ���÷�Ӧ�Ļ�ѧ����ʽΪN2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=��641.6 kJmol��1 �� ��C��ȷ��
D��ȼ������ָ25��101KPʱ��1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų�����������Ӧ���뷽��ʽ�ļ����������ȣ�CO��g����ȼ�����ǩ�283.0kJ/mol����2CO��g��+O2��g��=2CO2��g����Ӧ�ġ�H=��2��283.0kJ/mol����2CO2��g���T2CO��g��+O2��g�� ��Ӧ�ġ�H=+2��283.0 KJmol��1 �� ��D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������뽺���ص���
A.�ü�������䵰������Һʱ������һ��������ͨ·
B.���м���ʯ���ƵÿɿڵĶ���
C.CuSO4��Һ����ɫ
D.���ˮ����μ���FeCl3������Һ���õ����ɫ���ķ�ɢϵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A.ClO3���Ŀռ乹��Ϊƽ��������
B.��Ȳ�����е�����̼ԭ�Ӳ���sp2�ӻ���ʽ
C.CS2ΪV�εļ��Է���
D.SiF4��SO32��������ԭ�Ӿ�Ϊsp3�ӻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С����H2O2�ֽ�Ϊ�����о�Ũ�ȡ���������Һ����ԶԷ�Ӧ���ʵ�Ӱ�죬�ڳ����°������·������ʵ�顣
ʵ���� | ��Ӧ�� | ���� |
�� | 10 mL 2% H2O2��Һ | �� |
�� | 10 mL 5% H2O2��Һ | �� |
�� | 10 mL 5% H2O2��Һ | 1 mL 0.1 mol L-1 FeCl3��Һ |
�� | 10 mL 5% H2O2��Һ+����HCl��Һ | 1 mL 0.1 mol L-1 FeCl3��Һ |
�� | 10 mL 5% H2O2��Һ+����NaOH��Һ | 1 mL 0.1 mol L-1 FeCl3��Һ |
��1�������ܼӿ컯ѧ��Ӧ���ʵ�ԭ������
��2��ʵ��ٺ͢ڵ�Ŀ������ʵ��ʱ���ڽϳ�ʱ��û�й۲쵽������������ó����ۡ�������ʾ��ͨ��������H2O2�ȶ������ֽ⡣Ϊ�˴ﵽʵ��Ŀ�ģ����ԭʵ�鷽���ĸĽ�����
��3��д��ʵ��۵Ļ�ѧ��Ӧ����ʽ����
��4��ʵ��ۡ��ܡ����У�������������������ʱ��仯�Ĺ�ϵ��ͼ��������ͼ�ܹ��ó���ʵ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ijѧ����0.1000mol/L NaOH��Һ�ζ�δ֪Ũ�ȵ�������Һ��������ɷֽ�Ϊ���¼�����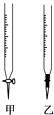
A�����ζ����Ƿ�©ˮ
B��������ˮϴ�ɾ��ζ���
C��ȡ�¼�ʽ�ζ����ñ���NaOH��Һ��ϴ����Һע���ʽ�ζ��ܡ�0���̶�����2��3cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ������0���̶Ȼ�0���̶�����
D���ô��ⶨ����Һ��ϴ��ʽ�ζ���
E������ʽ�ζ���ȡϡ����20.00mL��ע����ƿ�У������̪
F������ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶�
G����ȡ��ƿ�����ظ�����һ��
���������գ�
��1������F��Ӧ��ѡ��ͼ�� �ζ��ܣ����ţ���
��2���ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲� ��
A���ζ�����Һ��ı仯 B����ƿ����Һ��ɫ�ı仯
�ζ��յ���Һ��ɫ�ı仯�� ����ָʾ����Ϊ��������ɫ�ı仯�� ��
��3���ζ���������ʾ��
�ζ����� | ����Һ���/mL | ����Һ�����/mL | ||
�ζ�ǰ�̶� | �ζ���̶� | |||
�� | 20 | 1.02 | 21.03 | |
�� | 20 | 2.00 | 25.00 | |
�� | 20 | 0.60 | 20.59 | |
�ζ������ϴ���ǵ� ��ʵ�飬����������Ŀ���ԭ���� ��
A����ʽ�ζ�����װҺǰδ�ñ�NaOH��Һ��ϴ2��3��
B���ζ���ʼǰ��ʽ�ζ��ܼ��첿�������ݣ��ڵζ��յ����ʱδ��������
C���ζ���ʼǰ��ʽ�ζ��ܼ��첿��û�����ݣ��ڵζ��յ����ʱ���ּ��첿��������
D���ﵽ�ζ��յ�ʱ��������Һ��Һ����͵����
E���ζ������У���ƿҡ����̫���ң�������ЩҺ�ηɽ�����
��4���������Ũ��Ϊmol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ���칹�������л�����������Ҫԭ��֮һ�����л�Ϊͬ���칹���һ�黯�����ǣ� ��
A.���������
B.�Ҵ�������
C.��������춡��
D.����ϩ����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̲�ʵ�������ո��л�ѧʵ��Ļ����������⻯ѧ��ѧ��ʵ��ԭ����ʵ�鷽����ʵ��˼·�����ѧ��ʵ�������Ļ���;��:
(1)ʵ��1:ȡһ������ƣ��ڲ���Ƭ������ֽ���ɱ����ú�ͺ���С����ȥһ�˵���Ƥ���۲��Ƶ���ɫ�����ʵ���л����õ���һ��������_________��
(2)ʵ��2:��һ��ʢ��ˮ��С�ձ�����뼸�η�̪��Һ��Ȼ���һС����Ͷ��С�ձ����ѷ�Ӧ���������Ӧ��������ո�������--�Ƶ��ܶȱ�ˮС��������--��Ӧ��������������������������______________��
(3)ʵ��3��������ǯ��סһС����ɰֽ��ϸ��ĥ���������ھƾ����ϼ������ۻ��������ۻ������������䡣���й�������ʵ������Ľ�����ȷ����_________
A.�����¶�̫�Ͳ���ʹ��ȼ�� B.���ڿ������ܺܿ��γ�����Ĥ
C.���������۵�ȳ����۵�� D.��ĥɰֽ���ܳ�ȥ���������Ĥ
(4)ʵ��4:������ˮ����ʢ��Na2O2������Թ��У������ô����ǵ�ľ�������Թܿڣ�����
���ɵ������壬��Ӧ�����Һ�м����̪��Һ�����Կ���__________��
(5)ʵ��5:�ڲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ����,��������ԭ��Ӧ����������__________���÷�Ӧÿ����1mol����ת�Ƶ��ӵ����ʵ���Ϊ_________��
(6)ʵ��6:���Թ���ע���������Ʊ���FeSO4��Һ���ý�ͷ�ι���ȡNaOH��Һ�����ιܼ�˲����Թ�����Һ�ײ�����������NaOH��Һ�����Կ�����ʼʱ����һ�ְ�ɫ����״��������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ������������Ҳ�仯��ԭ����(�û�ѧ����ʽ��ʾ):______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������;������ȡ������������ͭ��
��ͭ��ϡ���ᷴӦ��
��ͭ��Ũ���ᷴӦ��
��ͭ����������Ӧ��������ͭ������ͭ�ٸ����ᷴӦ��������������ȷ����
A. ����;��������ͭ���������
B. ����;����������������ʵ�������>��>��
C. ;�������Ʊ��������������ɫ��ѧ������
D. ;�����б�������ͭ�뱻��ԭ����������ʵ���֮����3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����Ȼ���е�ѭ������ͼ����˵������ȷ���ǣ� ��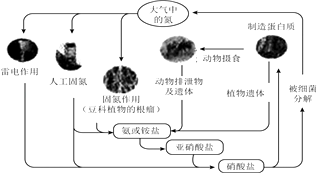
A.��Ԫ�ؾ�������
B.��ҵ�ϳɰ������˹��̵�
C.��������ͺ����л�����ת��
D.̼���⡢������Ԫ��Ҳ�μ��˵�ѭ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com