
【题目】A、B、C、D均是短周期元素,A和B同周期, B和C同族,A元素族序数是周期数的三倍,B原子最外层电子数是内层电子数的二倍,B与A能生成化合物BA2,C与A生成化合物CA2, A的阴离子与D的阳离子电子层结构相同,都与氖原子的电子层结构相同,D 的单质与A 的单质在不同条件下反应,可生成D2A或D2A2。请回答
(1)写出元素符号A:_______,B:_______,C:________。
(2)D2A的电子式___________,
(3)D2A2的化学式__________,灼烧该化合物火焰呈_________色。
(4)C在元素周期表中的位置是_________,其原子结构示意图为_________________。
(5)比较A、B简单氢化物的沸点________;原因_____________________________。
【答案】O C Si ![]() Na2O2 黄色 第三周期IVA族
Na2O2 黄色 第三周期IVA族 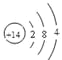 H2O > CH4 水分子间形成氢键,加大了分子间作用力
H2O > CH4 水分子间形成氢键,加大了分子间作用力
【解析】
A、B、C、D均是短周期元素,A元素族序数是周期数的三倍,A只能处于第二周期,族序数为Ⅵ,故A为O元素;A和B同周期,B原子最外层电子数是内层电子数的二倍,最外层电子数为4,则B为C元素;B和C同族,则C为Si;A的阴离子与D的阳离子电子层结构相同,都与氖原子的电子层结构相同,D的单质与A的单质在不同条件下反应,可生成D2A或D2A2,则D为Na,据此解答。
(1)由上述分析可知,A为O,B为C,C为Si,故答案为:O;C;Si;
(2)D2A为Na2O,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)D2A2的化学式为Na2O2,灼烧该化合物火焰呈黄色,故答案为:Na2O2;黄色;
(4)C为Si,元素周期表中的位置是第三周期IVA族,原子结构示意图为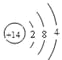 ,故答案为:第三周期IVA族;
,故答案为:第三周期IVA族; ;
;
(5)A为O元素,B为C元素,A、B简单氢化物分别为H2O、CH4,由于水分子间形成氢键,加大了分子间作用力,所以沸点H2O>CH4,故答案为:H2O>CH4;水分子间形成氢键,加大了分子间作用力。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】工业上用Na2SO3溶液处理硫酸厂的废气SO2得 NaHSO3溶液,然后用惰性电极电解 NaHSO3废水(原理如图所示)使吸收液再生,两膜中间的Na+和HSO3-可通过离子交换膜。下列叙述正确的是

A. 通电后中间隔室的HSO3-离子通过C膜向左侧迁移,左侧电极室溶液pH增大
B. 图中A连接电源的正极,B连接电源的负极
C. 阳极反应为HSO3-+H2O-2e-=SO42-+3H+,阳极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的Na2SO3生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )
A. 单位时间内生成n molA2同时生成n molAB
B. 容器内的总物质的量不随时间变化
C. 单位时间内生成2n molAB的同时生成n molB2
D. 单位时间内生成n molA2的同时生成n molB2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活密切相关,从化学的角度分析,下列有关说法不正确的是( )
A.用“84”消毒液对茶具、餐具和洁具进行清洗消毒
B.雾霾属于胶体,它区别于溶液等其它分散系的本质原因是能发生丁达尔现象
C.用石膏或盐卤点制豆腐与胶体性质有关
D.自来水厂用氯气对原水进行杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中进行反应C(s)+H2O(g)![]() CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是

A. 5min时该反应的K值一定小于12 min时的K值
B. 0~5min内,v (H2)=0.05mol/(Lmin)
C. 10 min时,改变的外界条件可能是减小压强
D. 该反应混合气体的平均相对分子质量:5min时小于12 min 时的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 800 | 0.20 | 0. 30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法错误的是
A. 实验①中,若5min时测得n(M) =0.05mol,则0至5min时间内,用N表示的平均反应速率v(N) =0.01 mol/( L·min)
B. 实验②中,该反应的平衡常数K= 1.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.06
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。减少CO2排放是一项重要课题。
(1)以CO2为原料制取碳(C)的太阳能工艺如图所示。

①过程1中每生成1molFeO转移电子数为_______________。
②过程2中发生反应的化学方程式为___________________________。
(2)碳酸二甲酯(CH3OCOOCH3,简称DMC)是一种应用前景广泛的新材料,用甲醇、CO、CO2在常压、70~120℃和催化剂条件下合成DMC。
已知:①CO的燃烧热为△H =﹣283.0 kJ·mol-1
②H2O(l)= H2O(g) △H = + 44.0 kJ·mol-1
③2CH3OH(g)+CO2(g)![]() CH3OCOOCH3 (g)+ H2O(g) △H =﹣15.5 kJ·mol-1
CH3OCOOCH3 (g)+ H2O(g) △H =﹣15.5 kJ·mol-1
则2CH3OH(g)+CO(g)+1/2O2(g)![]() CH3OCOOCH3 (g)+ H2O(l) △H =_______________。
CH3OCOOCH3 (g)+ H2O(l) △H =_______________。
(3)在密闭容器中按n(CH3OH):n(CO2)=2:1投料直接合成DMC,一定条件下,平衡时CO2的转化率如图所示,则:

①v(A)、v(B)、v(C)由快到慢的顺序为____________________;
②K(A)、K(B)、K(C)由大到小的顺序为___________________;
③下列能说明在此条件下反应达到平衡状态的是__________。
A.2v正(CH3OH)= v逆(CO2) B.CH3OH与CO2的物质的量之比保持不变
C.容器内气体的密度保持不变 D.各组分的物质的量分数保持不变
(4)CO2经催化加氢可以生成低碳烃,主要有以下两个竞争反应:
反应Ⅰ:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
反应II:2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
为分析催化剂对反应的选择性,在1 L密闭容器中充入1 molCO2和2 mol H2,测得有关物质的物质的量随温度变化如图所示。

①该催化剂在较低温度时主要选择________(填“反应Ⅰ”或“反应II”)。520℃时,反应II的平衡常数K=___________(只列算式不计算)。
②用惰性电极电解强酸性的二氧化碳水溶液可得到乙烯,其原理如图所示。b电极上的电极反应式为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属铝及氧化铝说法不正确的是( )
A.铝合金具有密度小、高强度及较好的可塑性,可用于制飞机骨架等。
B.铝在自然界中有游离态和化合态两种形式
C.由于表面存在致密的氧化铝,因此金属铝在空气中有良好的抗腐蚀性。
D.氧化铝是一种高硬度、高熔沸点的化合物,红宝石、蓝宝石的主要成分是氧化铝。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com