
【题目】PVAc是一种具有热塑性的树脂,可合成重要高分子材料M,合成路线如下:
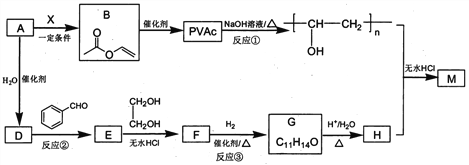
己知:R、Rˊ、Rˊˊ为H原子或烃基
I. R'CHO+ R"CH2CHO![]()
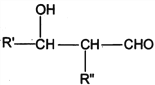
![]()
![]()
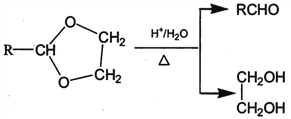
II. RCHO+![]()
![]()
(1)标准状况下,4.48L气态烃A的质量是5.2g,则A的结构简式为___________________。
(2)己知A→B为加成反应,则X的结构简式为_______;B中官能团的名称是_________。
(3)反应①的化学方程式为______________________。
(4)E能使溴的四氯化碳溶液褪色,反应②的反应试剂和条件是_______________________。
(5)反应③的化学方程式为____________________________。
(6)在E→F→G→H的转化过程中,乙二醇的作用是__________________________。
(7)己知M的链节中除苯环外,还含有六元环状结构,则M的结构简式为_________________。
【答案】 HC≡CH CH3COOH 酯基、碳碳双键 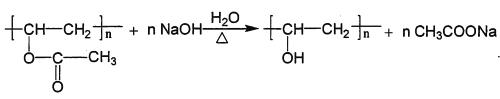 稀NaOH溶液/△
稀NaOH溶液/△ 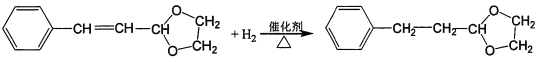 保护醛基不被H2还原
保护醛基不被H2还原 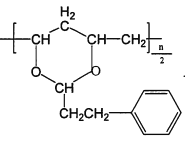
【解析】(1)标准状况下,4.48L气态烃A的物质的量为0.2mol, 质量是5.2g,摩尔质量为26g/mol,所以A为乙炔,结构简式为HC≡CH;正确答案:HC≡CH。
(2)根据B分子结构可知,乙炔和乙酸发生加成反应,X的结构简式为. CH3COOH;B中官能团的名称是酯基、碳碳双键;正确答案:CH3COOH;酯基、碳碳双键。
(3)有机物B发生加聚反应生成PVAc,PVAc在碱性环境下发生水解生成羧酸盐和高分子醇,化学方程式为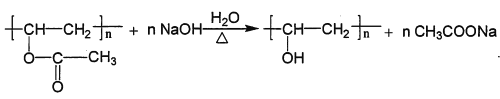 ;正确答案:
;正确答案:
(4)乙炔水化制乙醛,乙醛和苯甲醛发生加成、消去反应生成有机物E,因此反应②的反应试剂和条件是是稀NaOH溶液/△ ;正确答案:稀NaOH溶液/△ 。
(5)根据信息II,可知芳香烯醛与乙二醇在氯化氢环境下发生反应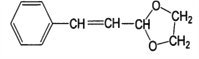 ,与氢气发生加成反应生成
,与氢气发生加成反应生成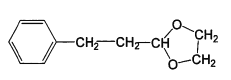 ;化学方程式为
;化学方程式为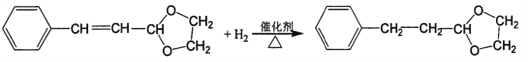 ;正确答案:
;正确答案: 。
。
6)从流程图可以看出,醛基能够与氢气发生加成反应,所以乙二醇的作用是保护醛基不被H2还原;正确答案:保护醛基不被H2还原。
(7)高分子醇中2个 -CH(OH)-CH2-与苯丙醛发生反应,生成六元环状结构的高分子环醚,则M的结构简式为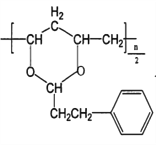 ;正确答案:
;正确答案: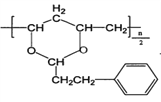 。
。


科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是
选项 | 反应类型 | 反应条件 |
A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京航空航天大学教授偶然中发现米虫吃塑料,受此启发进行了系列实验,证实黄粉虫的肠道微生物可降解聚苯乙烯(PS),蜡虫可降解聚乙烯(PE)。聚苯乙烯在虫肠内降解的示意图如下,下列说法正确的是
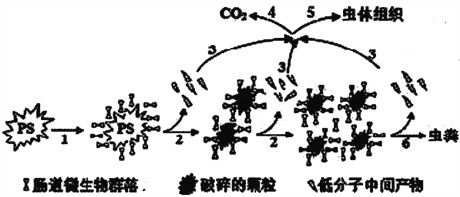
A. 在虫肠内微生物作用下,聚苯乙烯断裂碳碳双键
B. 在虫肠内微生物作用下,聚苯乙烯直接降解为CO2分子
C. 在虫肠内微生物作用下,聚苯乙烯发生降解,分子量降低
D. 聚乙烯与聚苯乙烯是同系物,具有烯烃的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2CO3溶液存在水解平衡:CO![]() +H2O
+H2O![]() HCO
HCO![]() +OH-。下列说法正确的是( )
+OH-。下列说法正确的是( )
A. 稀释溶液,水解平衡常数增大
B. 加入少量NH4Cl固体,平衡朝正反应方向移动
C. 升高温度,![]() 减小
减小
D. 加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱除工业尾气中的二氧化硫气体对物质的充分利用和环境保护有重要意义。
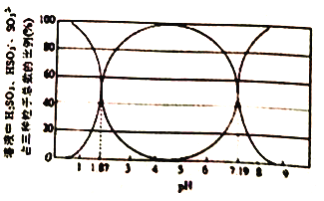
(1)某温度下,二氧化硫溶于水后所得溶液中H2SO3、HSO3-和SO32-占三种粒子总数的比例随pH 的变化如图所示。则在pH 为3时,溶液中H2SO3、HSO3-和SO32-的浓度最大的为_____。该温度下H2SO3 的电离平衡常数Ka1=_________。
(2)利用尿素[CO(NH2)2]水解的溶液可以吸收空气中含有的SO2。已知尿素水解放热,常温下水解反应较慢,水解的反应方程式如下:CO(NH2)2+H2O![]() H2NCOONH4 (氨基甲酸铵)。
H2NCOONH4 (氨基甲酸铵)。
①当该反应处于平衡状态时,下列措施中有利于提高尿素水解程度的是____(填字母)。
a.升高反应温度 b.延长反应时间
c.增大尿素的浓度 d.向装置中充入SO2和空气混合物
②氨基甲酸铵会与空气中的SO2和O2反应:2 H2NCOONH4 (aq)+2SO2(g)+2O2(g)+H2O![]() 2(NH4)2SO4(aq )+2CO2(g),判断该反应达到平衡状态的标志是_______(填字母)。
2(NH4)2SO4(aq )+2CO2(g),判断该反应达到平衡状态的标志是_______(填字母)。
a.SO2和CO2浓度相等 b. SO2百分含量保持不变
c.容器中气体的压强不变 d.CO2的生成速率与SO2的消耗速率相等
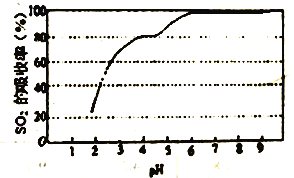
③尿素溶液吸收SO2的吸收率随溶液的pH变化如图所示。尿素溶液吸收空气中的SO2后溶液的pH 会降低,为提高SO2 的吸收率和充分回收产物,应控制溶液pH 为_____。
(3)工业上也常用氨水吸收SO2 。25℃时将SO2通入氨水中,当产物恰好为NH4HSO3时,溶液为_____ (填酸性、中性或碱性)。当c(OH-)降至1.0×10-7mol/L时,溶液中的c(SO32-)/c(HSO3-)=__________。己知25℃,NH3·H2O 的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学就在你身边
(1)汽车尾气是城市空气污染来源之一,汽车尾气中含有CO和NO等有害物质。通过特殊的催化装置,可以使CO与NO相互反应生成无害且稳定的气体N2和CO2,反应的化学方程式是_____________。若反应生成1molN2,转移的电子数目为_______________。(NA表示阿伏加德罗常数的值)
(2)Cl2+2NaOH=NaCl+NaClO+H2O是工业上制84消毒液的原理,把上述化学方程式改为离子方程式,并用双线桥法标明电子转移的方向和数目。_________________
(3)在一定的温度和压强下,1体积X2 (气)跟3体积Y2 (气)化合生成2体积化合物,则该化合物的化学式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于离子化合物的叙述正确的是( )
A.离子化合物中都含有离子键
B.离子化合物中的阳离子只能是金属离子
C.离子化合物一定可以导电
D.溶于水可以导电的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 铜在自然界中主要以单质的形式存在
B. 工业上常用电解饱和食盐水的方法制备金属钠
C. 工业上常用焦炭在高温下直接将氧化铁还原炼铁
D. 在海水中加入石灰乳可得氢氧化镁沉淀,这是从海水中富集镁的基本方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com