
【题目】(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下面的适当位置。

①________②________③________④________
(2)图中所示的物质分类方法名称是______________________。
科目:高中化学 来源: 题型:
【题目】制烧碱所用的盐水需进行两次的精制。
(1)第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、SO42-等离子,过程如下:
I.向粗盐水中加入过量X,过滤。
II.向所得滤液中加入过量Y,过滤。
III.滤液用盐酸调节pH,获得一次精制盐水。
请回答下列问题:
①X是__________。
②Y是___________,加入Y的主要目的_______________。
③经检测,II中过滤所得的沉淀中还含有Mg2(OH)2CO3,生成该沉淀的离子方程式是________。
(2)第二次精制要除去一次精制盐水中微量的IO3-、NH4+、Ca2+、Mg2+,流程示意图如下:
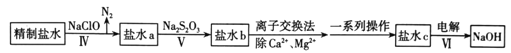
①IV中除去的离子是____________(填化学式),判断的理由是_______。
②V中得到的溶液颜色呈棕黄色,由此说明Na2S2O3将IO3-还原为______(填化学式),同时Na2S2O3被氧化为SO42-。此反应中体现了Na2S2O3的_________性。假设Na2S2O3已完全反应,则证明盐水b中含有SO42-的方法是__________,观察到的现象是____________。
③有同学提出,该流程中的过程IV可直接加入NaOH溶液除去NH4+和Mg2+,你认为是否可行?_______(填“是”或“否”,提示NH3极易溶于水),理由是_______(答一点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如下图所示。

(1)根据上图信息可以看出,下列哪种气体污染物不是由机动车行驶造成的_________,
a.SO2 b.NOx c.VOCs d. NH3
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式_______。

(3)SO2是气体污染物的主要成分之一。作为一种化学性质活泼的物质,它能发生多种反应,请按照下表提示,从不同角度梳理SO2不同类的化学性质,将化学方程式填在下表中。
SO2性质梳理 | 化学方程式 | |
物质类别 | 酸性氧化物 | ①SO2 +H2O |
②SO2 + CaO = CaSO3 | ||
③_______________________ | ||
S元素 价态 | S为+4价 | ①_______________________ |
② SO2 + 2H2S = 3S + 2H2O | ||
(4)科学家经过研究发现中国霾呈中性,其主要原因如图所示:

请判断A的化学式并说明判断理由:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项中所示的物质间转化均能实现的是
A. NaOH(aq) ![]() Cu(OH)2悬浊液
Cu(OH)2悬浊液![]() Cu2O
Cu2O
B. NH3![]() NO
NO![]() HNO3
HNO3
C. MgC12(aq)![]() 无水MgC12
无水MgC12![]() Mg
Mg
D. CaCl2(aq)![]() CaCO3
CaCO3![]() CaO
CaO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见有机物A、B、C、D、E、F间的转化关系如下图所示(以下变化中,某些反应条件及产物未标明)。B是天然有机高分子化合物,C、D可发生银镜反应,在相同条件下,F蒸气密度是氦气的22倍。
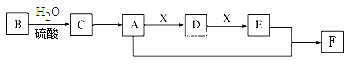
(1)B的分子式为_________________ ;F的结构简式为__________________。
(2)E中官能团的名称___________________________。
(3)A的同分异构体的结构简式_____________________。
(4)A→D反应的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
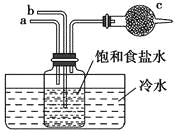
A. a通入CO2,然后b通入NH3,c中放碱石灰
B. b通入NH3,然后a通入CO2,c中放碱石灰
C. a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D. b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的恒容密闭容器中充入6 mol CO2和8 mol H2,发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH =-49.0kJ·mol-1
CH3OH(g)+H2O(g) ΔH =-49.0kJ·mol-1
测得n(H2)随时间变化如曲线Ⅰ所示。下列说法正确的是
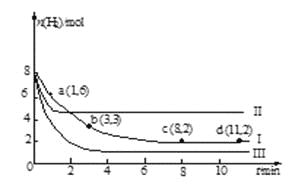
A. 该反应在0~8 min内CO2的平均反应速率是0.375mol·L-1·min-1
B. 若起始时向上述容器中充入3 mol CO2和4 mol H2,则平衡时H2的体积分数大于20%
C. 若起始时向上述容器中充入4 mol CO2、2 mol H2、2 mol CH3OH和1mol H2O(g),则此时反应向正反应方向进行
D. 改变条件得到曲线Ⅱ、Ⅲ,则曲线Ⅱ、Ⅲ改变的条件分别是升高温度、充入氦气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiAlH4是重要的储氢材料,其组成类似于Na3AlF6。常见的供氢原理如下面两个方程式所示:①2LiAlH4![]() 2LiH+2Al+3H2↑,②LiAlH4+2H2O=LiAlO2+4H2↑。下列说法正确的是
2LiH+2Al+3H2↑,②LiAlH4+2H2O=LiAlO2+4H2↑。下列说法正确的是
A. 若反应①中生成3.36L氢气,则一定有2.7g铝生成
B. 氢化锂也是一种储氢材料,供氢原理为LiH+H2O=LiOH+H2↑
C. 生成等质量的氢气,反应①②转移电子数之比为4:3
D. LiAlH4是共价化合物,LiH是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物G可用来制备抗凝血药,可通过下列路线合成。

请回答:
(1)C+E→F的反应类型是____。
(2)F中含有的官能团名称为____。
(3)在A→B的反应中,检验A是否反应完全的试剂为_____。
(4)写出G和过量NaOH溶液共热时反应的化学方程式_____。
(5)化合物E的同分异构体很多,符合下列条件的结构共____种。
①能与氯化铁溶液发生显色;②能发生银镜反应;③能发生水解反应
其中,核磁共振氢谱为5组峰,且峰面积比为2∶2∶2∶1∶1的结构简式为___。
(6)E的同分异构体很多,所有同分异构体在下列某种表征仪器中显示的信号(或数据)完全相同,该仪器是___(填标号)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(7)已知酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯(![]() )是一种重要的有机合成中间体。请根据已有知识并结合相关信息,试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。____
)是一种重要的有机合成中间体。请根据已有知识并结合相关信息,试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任选)。____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com