
【题目】常见有机物A、B、C、D、E、F间的转化关系如下图所示(以下变化中,某些反应条件及产物未标明)。B是天然有机高分子化合物,C、D可发生银镜反应,在相同条件下,F蒸气密度是氦气的22倍。
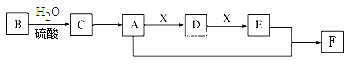
(1)B的分子式为_________________ ;F的结构简式为__________________。
(2)E中官能团的名称___________________________。
(3)A的同分异构体的结构简式_____________________。
(4)A→D反应的化学方程式:______________________。
【答案】(C6H10O5)n CH3COOCH2CH3 羧基 CH3OCH3 2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
在相同条件下,G蒸气密度是氦气的22倍,可以计算出F的相对分子质量为88。因为B是天然有机高分子化合物,根据B转化为C的条件可知B发生了水解反应,再结合C、D可发生银镜反应(说明C和D分子中有醛基),可以推断B可能是淀粉或纤维素,C为葡萄糖;再联系G的相对分子质量,可以确定A为乙醇,D为乙醛,E为乙酸,F为乙酸乙酯。
(1)B的分子式为(C6H10O5)n ;F的结构简式为CH3COOCH2CH3。
(2)E中官能团的名称羧基。
(3)A的同分异构体为二甲醚,二甲醚的结构简式为CH3OCH3 。
(4)A→D反应的化学方程式:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2C12)是工业上常用的硫化剂。常温下是一种液体,沸点137℃,易与水反应。实验室可通过硫与少量氯气在110140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。
(1)选取以下装置制取少量S2Cl2:

①仪器m的名称为_____________。
②装置连接顺序:A→________________________________→E→D。
③A中发生反应的离子方程式为 _________________________。
④装置F的作用是____________________。
⑤D中的最佳试剂是__________(填标号)。
a.碱石灰 b.浓硫酸 c.无水氯化钙
⑥为了提高S2Cl2的纯度,关键的是控制好温度和_______________________。
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合物的SO2的体积分数。

①W溶液可以是下列溶液中的__________(填标号);
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为__________(含V、m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学用语表示Na2CO3+2Cl2===2NaCl+Cl2O+CO2中的相关微粒,其中正确的是( )
A. Na+的结构示意图:![]()
B. Cl2O的结构式:Cl—O—Cl
C. 中子数比质子数多3的氯原子:3517Cl
D. CO2的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。某厂为了变废为宝,将工业废水(含5.00×10-3 mol·L-1的Cr2O72-)处理得到磁性材料Cr0.5Fe1.5FeO4,设计了如下实验流程:
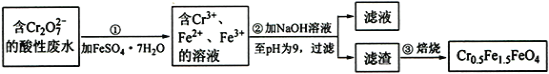
(1)第①步反应的离子方程式是_____。
(2)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有_____。
(3)为保证磁性材料的质量,应控制第①步反应后所得溶液中Fe3+与Fe2+的比例为___。在第②步过程中,须持续通入N2,原因是____________。
(4)将FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是_____。
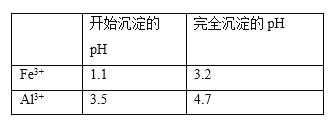
(5)以工业碳酸钙(含有少量A12O3、Fe3O4杂质)生产二水合氯化钙(CaC12·2H2O)的方法为:将工业碳酸钙溶于盐酸,________得到CaC12·2H2O。(在横线上补全实验步骤,实验中需用到的试剂和仪器有:盐酸,双氧水,氢氧化钙,冰水,pH计)。有关离子开始沉淀及沉淀完全时的pH见下表
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3和NaHCO3是两种常见的钠盐.
(1)用洁净的铂丝蘸取Na2CO3粉末置于酒精灯火焰上灼烧,火焰呈_____色.
(2)等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同条件下产生CO2的体积V(Na2CO3)_____V(NaHCO3)(填“大于”,“小于”或“等于”)
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为_____.
(4)实验室中需2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量是_____.
A. 1000mL; 212g B.950mL;543.4g C.任意规格; 572g D.500mL; 106g
(5)若出现如下情况,其中将引起所配溶液浓度偏高的是_____(填下列编号);
A.容量瓶实验前用蒸馏水洗干净,但未烘干
B.定容观察液面时俯视
C.未冷却至室温就开始定容
D.加蒸馏水时不慎超过了刻度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将碳酸钙、稀盐酸、铁、氧气四种物质填写到下面的适当位置。

①________②________③________④________
(2)图中所示的物质分类方法名称是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由短周期元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
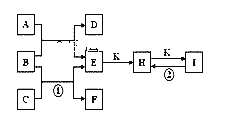
请回答下列问题:
(1)物质A的化学式为________;物质D的名称________;
(2)化合物I的化学式为_____________________;
(3)反应①的化学方程式为_______________________________________;
反应②的化学方程式为_______________________________________;
A与B反应的化学方程式________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3 molO2加入到V L的反应器中,在高温下放电,经t1 s建立了平衡体系:3O2![]() 2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
A. 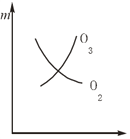 B.
B. 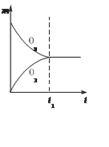
C. 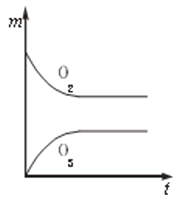 D.
D. 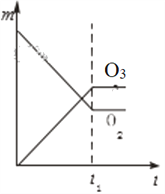
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是
A. 向含等物质的量的![]() 的溶液中缓慢通入氯气:
的溶液中缓慢通入氯气:![]()
B. 向含等物质的量的![]() 的溶液中缓慢加入锌粉:
的溶液中缓慢加入锌粉:![]()
C. 在含等物质的量的![]() 的混合溶液中缓慢通入CO2:
的混合溶液中缓慢通入CO2:![]() 、
、![]()
D. 在含等物质的量的![]() 的溶液中逐滴加入盐酸:
的溶液中逐滴加入盐酸:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com