
【题目】有机物Q是有机合成的重要中间体,制备Q的一种合成路线如下(部分反应条件和试剂略去)。
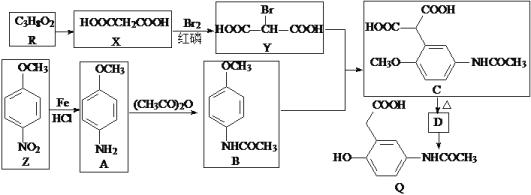
回答下列问题:
(1)Y中不含氧的官能团名称为__________,R的名称为_________________________。
(2)加热C脱去CO2生成D,D的结构简式为____________________________。
(3)B+Y→C的反应类型是_______________,Q的分子式为____________________。
(4)A→B的化学方程式为______________________________________________。
(5)同时满足下列条件的Z的同分异构体有_____________种(不包括立体异构)。①能与氯化铁溶液发生显色反应;②能与碳酸氢钠反应;③含―NH2; ④苯环上有处于对位的取代基
(6)已知:―NH2具有强还原性。参照上述合成路线,以![]() 为原料(无 机试剂任选),设计制备
为原料(无 机试剂任选),设计制备![]() 的合成路线:__________。(格式:CH2=CH2
的合成路线:__________。(格式:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH)
CH3CH2OH)
【答案】溴原子 1,3-丙二醇 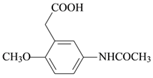 取代反应 C10H11O4N
取代反应 C10H11O4N 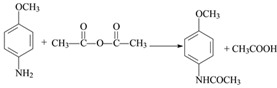 6
6 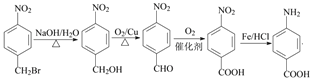
【解析】
由R的分子式、X的结构简式,可推知R为HOCH2CH2CH2OH;加热C脱去CO2生成D,即C中侧链-CH(COOH)2转化为-CH2COOH而得到D,因此D为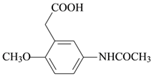 ,结合官能团的结构和性质分析解答(1)~(5)。
,结合官能团的结构和性质分析解答(1)~(5)。
(6)由于-NH2具有强还原性,应先引入羧基,再还原硝基得到氨基,因此应先制备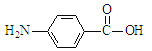 结合羟基的引入方法分析解答。
结合羟基的引入方法分析解答。
(1)Y(![]() )中含有的官能团有-COOH、-Br,其中不含氧的官能团为溴原子;由R的分子式、X的结构简式,可推知R为HOCH2CH2CH2OH,名称为:1,3-丙二醇,故答案为:溴原子;1,3-丙二醇;
)中含有的官能团有-COOH、-Br,其中不含氧的官能团为溴原子;由R的分子式、X的结构简式,可推知R为HOCH2CH2CH2OH,名称为:1,3-丙二醇,故答案为:溴原子;1,3-丙二醇;
(2)加热C脱去CO2生成D,即C中侧链-CH(COOH)2转化为-CH2COOH而得到D,故D的结构简式为: ,故答案为:
,故答案为: ;
;
(3)对比B、Y、C的结构,可知B中苯环上-OCH3邻位的H原子被换成了-CH(COOH)2生成C,属于取代反应。Q(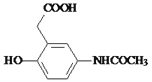 )的分子式为:C10H11O4N,故答案为:取代反应;C10H11O4N;
)的分子式为:C10H11O4N,故答案为:取代反应;C10H11O4N;
(4)对比A、B结构,可知A→B是A的氨基中氢原子被![]() 取代生成B,同时还生成CH3COOH,反应的方程式为:
取代生成B,同时还生成CH3COOH,反应的方程式为: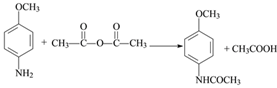 ,故答案为:
,故答案为: ;
;
(5)Z为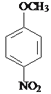 ,Z的同分异构体满足:①能与氯化铁溶液发生显色反应,说明含有酚羟基;②能与碳酸氢钠反应,说明含有-COOH;③含-NH2,④苯环上有处于对位的取代基,该同分异构体中含有3个取代基:-OH、-NH2、-COOH,处于对位的2个取代基有3种组合,另外一个取代基均含有2种位置,故符合条件的共有3×2=6种,故答案为:6;
,Z的同分异构体满足:①能与氯化铁溶液发生显色反应,说明含有酚羟基;②能与碳酸氢钠反应,说明含有-COOH;③含-NH2,④苯环上有处于对位的取代基,该同分异构体中含有3个取代基:-OH、-NH2、-COOH,处于对位的2个取代基有3种组合,另外一个取代基均含有2种位置,故符合条件的共有3×2=6种,故答案为:6;
(6)以![]() 为原料制备
为原料制备![]() 。氨基可以有硝基还原得到,由于-NH2具有强还原性,应先引入羧基,因此应先制备
。氨基可以有硝基还原得到,由于-NH2具有强还原性,应先引入羧基,因此应先制备 ,再还原硝基得到氨基,
,再还原硝基得到氨基,在碱性条件下溴原子水解可以引入羟基,再氧化可以引入-COOH,最后与Fe/HCl作用,还原得到氨基,合成路线流程图为:
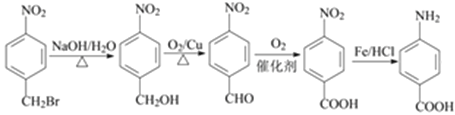 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:
为阿伏加德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:![]() 。下列说法正确的是( )
。下列说法正确的是( )
A.如果氯气管道漏气,则会看到有大量白雾生成
B.反应中每形成![]() 键,转移电子数为
键,转移电子数为![]()
C.![]() 的
的![]() 溶液中,
溶液中,![]() 的数目小于
的数目小于![]()
D.该反应中,氧化剂与还原剂的物质的量之比为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富马酸亚铁(C4H2O4Fe)是常用的治疗贫血的药物。可由富马酸与FeSO4反应制备。
(1)制备FeSO4溶液的实验步骤如下:
步骤1.称取4.0g碎铁屑,放入烧杯中,加入10%Na2CO3溶液,煮沸、水洗至中性。
步骤2.向清洗后的碎铁屑中加入3mol/L H2SO4溶液20mL,盖上表面皿,放在水浴中加热。不时向烧杯中滴加少量蒸馏水,控制溶液的pH不大于1。
步骤3.待反应速度明显减慢后,趁热过滤得FeSO4溶液。
①步骤1的实验目的是____。
②步骤2“不时向烧杯中滴加少量蒸馏水”的目的是____;“控制溶液的pH不大于1”的目的是____。
(2)制取富马酸亚铁的实验步骤及步骤(Ⅱ)的实验装置如下:
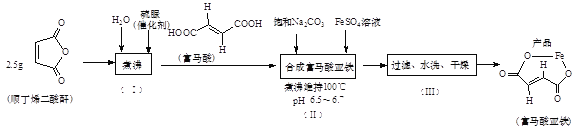
①步骤(Ⅰ)所得产品(富马酸)为_______-丁烯二酸(填“顺”或“反”)。
②富马酸与足量Na2CO3溶液反应的方程式为_________。
③图中仪器X的名称是_________,使用该仪器的目的是__________。
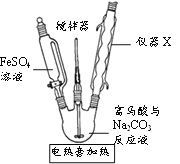
(3)测定(2)产品中铁的质量分数的步骤为:准确称取产品ag, 加入新煮沸过的3mol/LH2SO4溶液15mL,待样品完全溶解后,再加入新煮沸过的冷水50mL和4滴邻二氮菲-亚铁指示剂,立即用cmol/L (NH4)2Ce(SO4)3标准溶液滴定(Ce4++Fe2+=Ce3++Fe3+),滴定到终点时消耗标准液VmL。
①(NH4)2Ce(SO4)3标准溶液适宜盛放在_______(填“酸式”或“碱式”)滴定管中。
②该实验中能否用KMnO4标准溶液代替(NH4)2Ce(SO4)3标准溶液滴定Fe2+,说明理由_____。
③产品中铁的质量分数为________(用含a、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() (x)
(x)![]() (y)
(y)![]() (z)的分子式均为C8H8,下列说法正确的是
(z)的分子式均为C8H8,下列说法正确的是
A. x、y、z均能使Br2的CCl4溶液褪色
B. x的同分异构体只有y和z
C. x、y、z的二氯代物均只有三种
D. x、y、z中只有y中所有原子可以处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据物质结构有关性质和特点,回答下列问题:
(1)Ti基态原子核外电子排布式为____________,碳原子的价电子轨道表示式为________。
(2)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积____________(填“膨胀”或“收缩”)。
(3)写出一种与NH4+互为等电子体物质的化学式____________。
(4)SO2的空间构型为___________________。
(5)丙烯腈(CH2=CH—CN)分子中σ键和π键的个数比为____,分子中碳原子轨道杂化类型是______。
(6)FeCl3熔点282℃,而FeCl2熔点674℃,二者熔点差异的原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取SO2并验证SO2某些性质的装置图。若观察到装置④中的有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答:
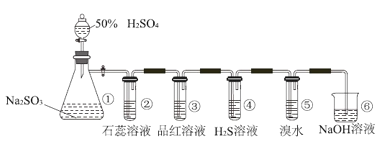
(1)①中发生反应的离子方程式为_____。
(2)③的实验现象是_____,证明SO2有_____性。
(3)④中SO2做_____剂。
(4)⑤中反应生成两种强酸,该反应的离子方程式是_____。
(5)⑥的作用是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业为人类解决粮食问题做出了巨大贡献.一定条件下,在密闭容器中进行合成氨反应:N2(g)+3H2(g)2NH3(g),当正、逆反应速率相等且不等于零时,下列说法不正确的是( )
A. N2、H2完全转化为NH3 B. N2、H2、NH3在容器中共存
C. 反应已达到化学平衡状态 D. N2、H2、NH3的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:①NaOH+HCl=NaCl+H2O, ②Fe+H2SO4=FeSO4+H2↑。
回答下列问题:
(1)两反应中属于氧化还原反应的是_____(填序号,下同),能设计成原电池的是___。
(2)Fe—Cu原电池的装置如图所示。
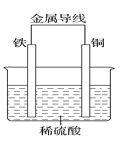
①铁作_____(填“正极”或“负极”),溶液中H+向____(填“铁”或“铜”)电极方向移动。
②正极的现象是________,负极的电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组制备高铁酸钾![]() 并探究其性质。
并探究其性质。
资料:![]() 为紫色固体,微溶于
为紫色固体,微溶于![]() 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生![]() ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1)制备![]() (夹持装置略)
(夹持装置略)
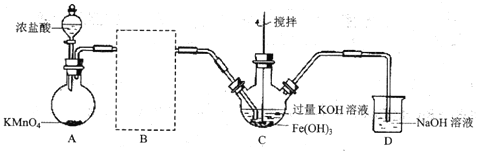
①A为氯气发生装置。A中反应的离子方程式为_________(锰被还原为![]() )。
)。
②请在B方框内将除杂装置补充完整,并标明所用试剂__________。
③![]() 中得到紫色固体和溶液。
中得到紫色固体和溶液。![]() 中主要反应的化学方程式为___________。
中主要反应的化学方程式为___________。
(2)探究![]() 的性质
的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有![]() 。为证明是否
。为证明是否![]() 氧化了
氧化了![]() 而产生
而产生![]() ,设计以下方案:
,设计以下方案:
方案Ⅰ | 取少量a,滴加 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将 |
由方案Ⅰ中溶液变红可知a中含有的离子为____,但该离子的产生不能判断一定是![]() 将
将![]() 氧化,该离子还可能由_______产生(用离子方程式表示)。
氧化,该离子还可能由_______产生(用离子方程式表示)。
②根据![]() 的制备实验得出:氧化性
的制备实验得出:氧化性___________
![]() (填“>”或“<”),而方案Ⅱ实验表明,
(填“>”或“<”),而方案Ⅱ实验表明,![]() 和
和![]() 的氧化性强弱关系相反,原因是________________。
的氧化性强弱关系相反,原因是________________。
③资料表明,酸性溶液中的氧化性![]() ,验证实验如下:将溶液
,验证实验如下:将溶液![]() 滴入
滴入![]() 和足量
和足量![]() 的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性![]() 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:_______________。
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com