
【题目】关于KOH溶液和Fe(OH)3胶体描述正确的是
A. 两者的分散质都属于碱
B. 两者均为有色不透明的分散系
C. 两者分散质的直径都介于10-9~10-7m之间
D. 一束光线分别通过时,两者都会出现明显的光带
科目:高中化学 来源: 题型:
【题目】下面这个实验为“套管实验”,实验装置如下图,请观察实验装置。分析实验原理,并回答下列问题:
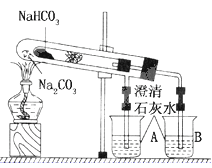
(1)整个实验过程中,能观察到①烧杯A中的现象:②烧杯B中的现象______________;
(2)实验结束时的操作是______________
(3)写出实验过程中发生反应的化学方程式______________;
(4)该实验可证明稳定性:NaHCO3 Na2CO3(填大于,小于或等于),证明稳定性比较时,能否将NaHCO3、Na2CO3的位置互换 (填能或不能)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于容积为2 L的密闭容器中,发生反应:4A(g)十B(g)=2C(g)反应进行到4 s末,测得C为0.2 mol。则该反应速率v(C)为
A.0.025 mol/(L·s) B.0.012 5 mol/(L·s)
C.0.05 mol/(L·s) D.0.1 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。请你根据所学知识回答下列问题:
(1)上述反应中 是氧化剂,该反应中氧化产物与还原产物的物质量之比为 。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是: 。
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液 mL才能与2.24 L氯气(标准状况)恰好完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式并用双线桥法表示出电子转移情况: 。
(5)现需490 mL 2.0 mol·L-1NaOH溶液:
①所需称量的氢氧化钠固体的质量是 。
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、 。
③在配制溶液的过程中,下列操作可能造成结果偏高的是 。
A.定容时俯视 |
B.容量瓶不干燥,含有少量蒸馏水 |
C.溶解所用烧杯未洗涤 |
D.NaOH溶解后,未冷却即进行实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3.84 g Fe和Fe2O3的混合物溶于100 mL某浓度的盐酸中,恰好使混合物溶解,生成0.03 mol H2,向反应后的溶液中加入KSCN检验,溶液无明显现象,设HCl无挥发,反应后溶液的体积不变。(已知:氧化性Fe3+>H+,还原性Fe>Cl-)
(1)求标准状况下生成氢气的体积?
(2)求反应后Cl-的物质的量浓度?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
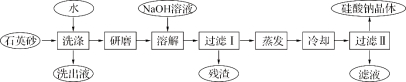
(1)要将洗出液中的溶质析出,采用的方法是 (填“蒸发”、“降温”)结晶;操作时用到的硅酸盐仪器有酒精灯(再填2个仪器) 。
(2)残渣的主要成分为: 。
(3)上述流程中加入NaOH溶液,反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:
①2H2(g)+O2(g)=2H2O(g) ΔH1;
②2H2(g)+O2(g)=2H2O(l) ΔH2
在相同条件下:2H2O(g)=2H2O(l)的焓变为
A.ΔH1-ΔH2 B.ΔH2-ΔH1 C.ΔH1+ΔH2 D.2ΔH1-2ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸与下列物质作用时,既表现氧化性,又表现酸性的是( ) ①炽热的木炭②H2S气体③Cu④FeO⑤NH3⑥蔗糖⑦CuSO45H2O⑧铁、铝.
A.③④
B.①②⑤⑧
C.①②③④⑦
D.⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com