
某芳香族化合物的分子式为C8H6O2,它的分子(除苯环外不含其它环)中不可能有
A.两个羟基 B.两个醛基 C.一个羧基 D.一个醛基
科目:高中化学 来源:2014-2015陕西岐山县高一上学期期末质量检测化学试卷(解析版) 题型:选择题
除去Na2CO3 固体中少量NaHCO3的最佳方法是
A.加入适量盐酸 B.加入NaOH溶液
C.加热 D.配成溶液后通入CO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省弥勒市高三市统测一模理综化学试卷(解析版) 题型:选择题
有一种瓦斯分析仪能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。下列有关叙述正确的是

A.电极a的反应式为:CH4+4O2--8e-=CO2+2H2O
B.电极b是正极,O2-由电极a流向电极b
C.瓦斯分析仪工作时,电池内电路中电子由电极a流向电极b
D.当固体电解质中有1 mol O2-通过时,电子转移4 mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省丹东五校协作体高三上学期期末考试理综化学试卷(解析版) 题型:选择题
化学与科学、技术、社会、环境密切相关,下列有关说法正确的是
A.锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去
B.日本福岛核电站爆炸时释放的两种放射性核素13153I与13755Cs的中子数相等
C.铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝
D.海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:选择题
由氧化铜和氧化铁组成的混合物a g,加入2 mol·L-1的稀硫酸溶液50 mL,恰好完全溶解,若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为
A. 1.6a g B.(a-1.6) g C.(a-3.2) g D.无法计算
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:填空题
(12分)过碳酸钠(2Na2CO3·3H2O2)俗称固体双氧水,是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的制备流程如下:
(注:BC-1、BC-2均为稳定剂,其中BC-1是由异丙醇和三乙醇胺按一定比例混合而成)
(1)结晶过程中加入氯化钠、搅拌,作用是 。
(2)加入BC-2稳定剂与工业纯碱中含有的Fe3+ 杂质生成稳定的配合物的目的是 。
(3)洗涤抽滤产品,应选用合适的洗涤试剂是 (填写序号)。
A.饱和氯化钠溶液 B.水 C.异丙醇 D.碳酸钠饱和溶液
(4)工业上常以活性氧的质量分数[ω(活性氧)=16 n(H2O2) / m(样品) ×100﹪]来衡量过碳酸钠产品的优劣,ω≥13﹪为优等品。现将0.2000g某厂家生产的过碳酸钠样品(所含杂质不参与后面的反应)溶于水配成溶液,加入适量稀硫酸酸化,再加入足量KI,摇匀后静置于暗处,充分反应后加入少量淀粉试剂,用0.1000mol/LNa2S2O3溶液滴定到终点,消耗Na2S2O3溶液33.00mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI),通过计算判断样品是否为优等品(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.在轮船表面涂刷富锌油漆,能有效防止船体在海水中被腐蚀
B.0.1 mol·L-1氨水加水稀释后,溶液中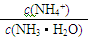 的值减小
的值减小
C.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
D.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省苏州市高三上学期期末调研测试化学试卷(解析版) 题型:选择题
300℃时,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应X(g) +Y(g) 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.当v逆(X)=2v正(Z),可以说明反应达平衡
B.反应前2 min的平均速率v(Z)=4.0×103 mol·L1·min1
C.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
D.该反应在350℃时的平衡常数小于1.44
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省南阳市高三上学期期末理综化学试卷(解析版) 题型:填空题
(16分)下图是部分短周期元素的常见化合价与原子序数的关系图:

(1)画出A的原子结构示意简图________________________;
(2)A的某氢化物分子式为A2H6,将含630mol电子的A2H6在氧气中完全燃烧生成稳定氧化物放出的热量为QkJ,请写出表示A2H6燃烧热的热化学方程式:_______________;
(3)用电子式表示D2G的形成过程__________________;其所含化学键类型为__________________;
(4)C2-、D+、G2-离子半径大小顺序是_____>______>______(用离子符号回答);
(5)C、G元素所形成的氢化物稳定性为_________>________(填化学式),原因是:_________________;
(6)某同学设计实验证明A、B、F的非金属性强弱关系,装置如图.

①溶液a和b分别为_______________,_______________;
②溶液c中发生反应的离子方程式为_________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com