
(12分)过碳酸钠(2Na2CO3·3H2O2)俗称固体双氧水,是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的制备流程如下:
(注:BC-1、BC-2均为稳定剂,其中BC-1是由异丙醇和三乙醇胺按一定比例混合而成)
(1)结晶过程中加入氯化钠、搅拌,作用是 。
(2)加入BC-2稳定剂与工业纯碱中含有的Fe3+ 杂质生成稳定的配合物的目的是 。
(3)洗涤抽滤产品,应选用合适的洗涤试剂是 (填写序号)。
A.饱和氯化钠溶液 B.水 C.异丙醇 D.碳酸钠饱和溶液
(4)工业上常以活性氧的质量分数[ω(活性氧)=16 n(H2O2) / m(样品) ×100﹪]来衡量过碳酸钠产品的优劣,ω≥13﹪为优等品。现将0.2000g某厂家生产的过碳酸钠样品(所含杂质不参与后面的反应)溶于水配成溶液,加入适量稀硫酸酸化,再加入足量KI,摇匀后静置于暗处,充分反应后加入少量淀粉试剂,用0.1000mol/LNa2S2O3溶液滴定到终点,消耗Na2S2O3溶液33.00mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI),通过计算判断样品是否为优等品(写出计算过程)。
(1)降低过碳酸钠的溶解度,有利于过碳酸钠晶体析出(2分)
(2)防止Fe3+杂质离子催化H2O2分解(2分) (3)C(2分)
(4)根据题目可知发生的化学反应为:H2O2+ 2KI+H2SO4=2H2O+I2+K2SO4(1分)
由关系式H2O2~I2 ~ Na2S2O3可得出:(1分)
n(H2O2)=1.65×10-3mol (2分)
ω(活性氧)=16n(H2O2)/ m(样品)×100﹪=16×1.65×10-3 mol÷0.2000g×100﹪
=13.2﹪(1分)
样品是优等品 (1分)
【解析】
试题分析:(1)结晶过程中加入氯化钠、搅拌,可以增大溶液中钠离子浓度,降低过碳酸钠的溶解度,有利于过碳酸钠晶体析出。
(2)由于双氧水在铁离子的催化作用下易分解生成水和氧气,则加入BC-2稳定剂与工业纯碱中含有的Fe3+ 杂质生成稳定的配合物的目的是防止Fe3+杂质离子催化H2O2分解。
(3)过碳酸钠在有机溶剂中溶解度很小,为防止产品溶解而损失,洗涤抽滤产品时应选用的洗涤试剂是异丙醇,答案选C。
(4)根据题目可知发生的化学反应为
H2O2+ 2KI+H2SO4=2H2O+I2+K2SO4
由关系式H2O2~I2 ~ Na2S2O3可得出
n(H2O2)=1.65×10-3mol
ω(活性氧)=16n(H2O2)/ m(样品)×100﹪
=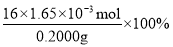
=13.2﹪
因此样品是优等品
考点:考查物质制备实验方案设计与探究


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:2014-2015陕西岐山县高一上学期期末质量检测化学试卷(解析版) 题型:选择题
现在CO和CO2 两种气体,它们所含氧原子的物质的量均为1 mol ,则 CO 与CO2的分子数之比为
A.1 :1 B.1 :2 C.2 :1 D.3 :2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省弥勒市高三市统测一模理综化学试卷(解析版) 题型:选择题
下列对图象描述正确的是

A.图①表示体积和pH值均相同的稀硫酸和醋酸,与足量的镁反应生成H2量的关系
B.图②表示向NaOH溶液中滴加稀盐酸,溶液导电性变化的关系
C.图③表示2SO2(g)+O2(g) 2SO3(g)反应过程中,SO2和O2反应速率大小关系
2SO3(g)反应过程中,SO2和O2反应速率大小关系
D.图④表示向氨水中滴加稀硫酸时,溶液的pH大小变化关系
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:实验题
(16分)Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取20 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取4 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。

③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________,检验是否存在该杂质的方法是____________________________。该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:_____________________________。
Ⅱ.测定产率
将所得产品配成500ml溶液,取该溶液20ml,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。反应原理为2S2O32-+I2===S4O62-+2I-
(5)滴定至终点时,溶液颜色的变化:____________________。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为______mL,则该实验的产率为_____。(保留三位有效数据)

Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:选择题
某芳香族化合物的分子式为C8H6O2,它的分子(除苯环外不含其它环)中不可能有
A.两个羟基 B.两个醛基 C.一个羧基 D.一个醛基
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)<sp(AgI) |
B | 向苯酚浊液中加入Na2CO3溶液 | 溶液变澄清 | 酸性:苯酚>HCO3— |
C | 向蓝色石蕊试纸上滴加新制氯水 | 试纸边缘呈红色色,中间为白色 | 氯水既有酸性又有还原性 |
D | 淀粉与稀硫酸混和一段时间后,滴加银氨溶液并水浴 | 无银镜出现 | 淀粉没有水解 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.铜溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O
B.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I 2+6OH-
C.向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D.向新制Cu(OH)2悬浊液中加入乙醛溶液并加热:CH3CHO+2Cu(OH)2+OH- CH3COO-+Cu2O↓+3H2O
CH3COO-+Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省苏州市高三上学期期末调研测试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的ΔH<0
B.镀锌铁制品镀层破损后,铁制品比受损前更容易生锈,而镀锡铁则相反
C.加热0.1 mol·L-1FeCl3溶液, Fe3+的水解程度增大、溶液的pH减小
D.向0.1 mol·L-1CH3COOH溶液中加水,则c(H+)与c(CH3COOH)的比值减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省南阳市高三上学期期末理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.向次氯酸钙溶液中通入少量CO2:2ClO-+H2O+CO2=CO32—+2HClO
B.向明矾溶液中加入足量Ba(OH)2溶液:Al3++2SO42—+4OH-+2Ba2+=2BaSO4↓+[Al(OH)4]-
C.向FeCl3溶液中加入足量单质锌:Zn+2Fe3+=Zn2++2Fe2+
D.向NaHSO4中滴加Ba(OH)2溶液至中性:H++SO42—+OH-+Ba2+=BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com