
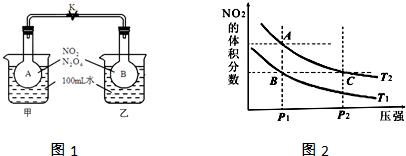
���� ��1�������¶ȶԻ�ѧƽ���Ӱ�죺�¶����ߣ���ѧ��Ӧ���ʼӿ죬ƽ���������ȷ����ƶ��жϣ�
��2������$\overline{M}=\frac{m}{n}$���ͼ�����T1��T2�¶ȵĸߵͿɵã�
��3���ٸ��ݻ�ѧƽ�ⳣ��������д��
�ڶԸ÷�Ӧ���¶����ߣ�ƽ�������ƶ���K��С��
��� �⣺��1������Bƿ������ˮ�У��¶Ƚϸߣ��÷�Ӧ�Ǹ����ȷ�Ӧ���¶����������淴Ӧ�����ƶ��������ɶ��������ķ�����ɫ����¶ȸߵķ�Ӧ���ʽϿ죻
�ʴ�Ϊ��B������
��2��A��B����ѹǿ��ͬ���¶Ȳ�ͬ��A������������������˵����Ӧ�����ƶ���T2��T1���÷�Ӧ����������������䣬�����ƶ������������ʵ���������$\overline{M}=\frac{m}{n}$����ƽ����Է���������С��
�ʴ�Ϊ������
��3����2NO2��g��?N2O4��g����ƽ�ⳣ������ʽK=$\frac{c��{N}_{2}{O}_{4}��}{{c}^{2}��N{O}_{2}��}$��
�ʴ�Ϊ��$\frac{c��{N}_{2}{O}_{4}��}{{c}^{2}��N{O}_{2}��}$��
���ɣ�2��֪��T2��T1���¶����ߣ��÷�Ӧ�����ƶ���K��С���ʴ�Ϊ������
���� ���⿼�鿴Ӱ�컯ѧƽ������ء���ѧƽ�ⳣ������ʽ����д��������ѧ���Ի���֪ʶ�Ĺ��̣�ע���ͼ��ķ����ǹؼ����ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢۢ� | C�� | �٢� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 һ�������£������Ϊ3L���ܱ������У�CO��H2��Ӧ���ɼ״���CH3OH��������ΪCu2O/ZnO����CO��g��+2H2��g��?CH3OH��g����������и��⣺
һ�������£������Ϊ3L���ܱ������У�CO��H2��Ӧ���ɼ״���CH3OH��������ΪCu2O/ZnO����CO��g��+2H2��g��?CH3OH��g����������и��⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
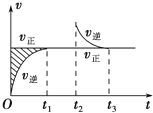 �����ܱ������������淴Ӧ��Z������+W������?X��g��+Y����������H����t1ʱ�̷�Ӧ�ﵽƽ�⣬��t2ʱ����С���������t3ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ���ǣ�������
�����ܱ������������淴Ӧ��Z������+W������?X��g��+Y����������H����t1ʱ�̷�Ӧ�ﵽƽ�⣬��t2ʱ����С���������t3ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ���ǣ�������| A�� | Z��W�ڸ���������һ����Ϊ��̬ | |
| B�� | t1��t2ʱ�����t3ʱ�̺���ʱ��η�Ӧ��ϵ�������ƽ��Ħ��������������� | |
| C�� | ���ڸ��¶��´˷�Ӧƽ�ⳣ������ʽΪK=c��X������t1��t2ʱ�����t3ʱ�̺��XŨ�Ȳ���� | |
| D�� | ���÷�Ӧֻ��ij�¶�T0�����Է����У���÷�Ӧ��ƽ�ⳣ��K���¶����߶����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
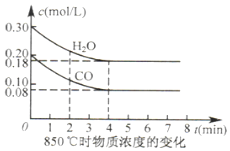 ����β�����������������ԭ��֮һ��
����β�����������������ԭ��֮һ��| ��ʼ���ʵ��� | �� | �� | �� |
| n��H2O��/mol | 0.10 | 0.20 | 0.20 |
| n��CO��/mol | 0.10 | 0.10 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
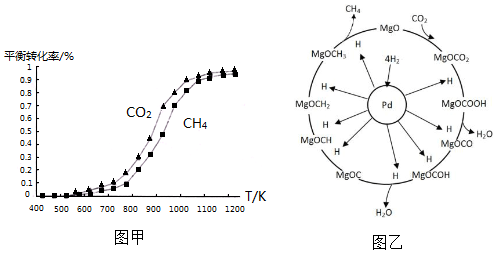 ��ͬ�¶���CO2��ƽ��ת���ʴ��ڣ�����ڡ���С�ڡ���CH4��ƽ��ת���ʣ���ԭ����CO2��������������Ӧ��
��ͬ�¶���CO2��ƽ��ת���ʴ��ڣ�����ڡ���С�ڡ���CH4��ƽ��ת���ʣ���ԭ����CO2��������������Ӧ�� CH4+2H2O��
CH4+2H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50mL 1 mol•L-1 NaCl��Һ | B�� | 100mL2 mol•L-1 AlCl3��Һ | ||
| C�� | 100mL1 mol•L-1 NH4Cl��Һ | D�� | 150mL2 mol•L-1 KCl��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com