
在一定温度下,将气体X和Y各1.6mol充入10L恒容密闭容器中,发生如下反应:

在反应过程中,X的物质的量与时间的关系如下表所示:
t/min | 0 | 2 | 4 | 6 | 8 | …… | 16 | 18 |
n(X)/mol | 1.600 | 1.200 | 1.100 | 1.075 | …… | …… | 1.000 | 1.000 |
下列说法不正确的是
A.4~6min时间段内Z的平均反应速率为2.5×10-3mol/(L·min)
B.此温度下该反应的平衡常数K=1.44
C.达平衡后,升高温度, 减小,则正反应
减小,则正反应
D.若保持其他条件不变,再充入1.6mol Z,达新平衡后Z的体积分数不变
C
【解析】
试题分析:A、4~6min时间段内X的物质的量减少1.1-1.075=0.025mol,所以Z的物质的量增加0.05mol,所以用Z表示的反应速率是0.05mol/10L/2min=0.0025 mol/(L·min),正确;B、16min时,反应达到平衡状态,此时X的物质的量浓度是1.000mol/10L=0.1mol/L,则Y的平衡浓度也是0.1mol/L,Z的平衡浓度是(1.6/10mol/L-0.1mol/L) ×2=0.12mol/L,所以该反应在该温度的平衡常数是0.122/0.12=1.44,正确;C、达平衡后,升高温度, 减小,说明平衡逆向移动,则正向是放热反应,所以△H<0,错误;D、若保持其他条件不变,再充入1.6molZ,因为生成物只有Z,所以相当于增大压强,而增大压强对该反应的平衡无影响,平衡不移动,Z的体积分数不变,正确,答案选C。
减小,说明平衡逆向移动,则正向是放热反应,所以△H<0,错误;D、若保持其他条件不变,再充入1.6molZ,因为生成物只有Z,所以相当于增大压强,而增大压强对该反应的平衡无影响,平衡不移动,Z的体积分数不变,正确,答案选C。
考点:考查对化学平衡的分析,平衡常数、反应速率的计算,平衡移动的判断
考点分析: 考点1:化学反应速率 考点2:化学平衡状态及移动 试题属性

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年山西省高二12月月考化学试卷(解析版) 题型:选择题
下列四组原电池,其中放电后,电解质溶液质量增加,且在正极有单质生成的是
A.Cu、Ag、AgNO3溶液 B.Zn、Cu、稀H2SO4
C.Fe、Zn、ZnSO4溶液 D.Fe、C、Fe2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高一上学期第三次月考化学试卷(解析版) 题型:选择题
仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图1、图2)就能实现相应实验目的是

查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高二上学期第三次月考化学试卷(解析版) 题型:选择题
对于合成氨工业来说,下列叙述中正确的是
A.使用催化剂和施加高压,都能提高反应速率,都对化学平衡状态无影响
B.使用催化剂和施加高压,都能提高反应速率,只有压强对化学平衡状态有影响
C.采用循环操作,能提高NH3的平衡浓度
D.采用循环操作,能加快反应速率
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第一学期期末练习化学试卷(解析版) 题型:推断题
(15分)化合物X是一种环境激素,存在如下转化关系:

(六元环状化合物)
化合物A能与FeCl3溶液发生显色反应,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取代物只有两种。B的核磁共振氢谱有三组峰,峰面积比6:1:1,且能与碳酸氢钠溶液反应。F(DMAEMA)在日化行业中常用于制备润湿剂、分散剂、树脂添加剂等。
已知:
RCOOR'+ R”18OH RCO18OR+R'OH( R、R’、R”代表烃基)根据以上信息回答:
RCO18OR+R'OH( R、R’、R”代表烃基)根据以上信息回答:
(1)B的官能团名称是 ,A C的反应类型是 。
C的反应类型是 。
(2)写出B在一定条件发生缩聚反应的方程式 。
(3)写出B G反应的化学方程式 。
G反应的化学方程式 。
(4)同时满足下列条件的D的同分异构体有____种(包括顺反异构),写出其中一种的结构简式 。
a.属于酯类
b.能发生银镜反应
c.不含环状结构
(5) ,写出E
,写出E F反应的化学方程式 。
F反应的化学方程式 。
(6)下列叙述正确的是 (填字母)。
a.化合物E不能与 发生加成反应
发生加成反应
b.化合物A可以和NaHCO3溶液反应
c.X与NaOH溶液反应,理论上1 mol X最多消耗6 mol NaOH
(7)X的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第一学期期末练习化学试卷(解析版) 题型:选择题
海洋约占地球表面积的71%,对其进行开发利用的部分流程如下图所示。下列说法不正确的是

A.可用BaCl2溶液除去粗盐中的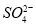
B.从苦卤中提取 的离子方程式为2Br-+ Cl2 === 2C1-十Br2
的离子方程式为2Br-+ Cl2 === 2C1-十Br2
C.试剂1可以选用Ca(OH)2
D.工业上,电解熔融Mg(OH)2冶炼金属镁
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第一学期期末练习化学试卷(解析版) 题型:选择题
下列有关物质应用的说法不正确的是
A.液氨常用作制冷剂 B.次氯酸钠是漂白液的有效成份
C.氧化钠可用于呼吸面具 D.小苏打是面包发酵粉的主要成分
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省泰安市高二上学期期末统考高二化学试卷(解析版) 题型:选择题
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O=4Al(OH)3。下列说法不正确的是
A.正极反应式为O2+2H2O+4e一=4OH—
B.以网状的铂为正极,可增大与氧气的接触面积
C.电池工作时,电流由铝电极沿导线流向铂电极
D.该电池通常只需更换铝板就可继续使用
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省忻州市高一上学期期末考试化学试卷(解析版) 题型:选择题
某CaCl2样品可能混有FeCl3、MgCl2、NaCl、Na2CO3中的一种或两种,取11.1克样品溶解,得无色溶液,再加入足量AgNO3溶液,得27.7克沉淀,由此可知样品中所含杂质的正确结论是
A.一定无Na2CO3,一定有MgCl2 B.一定无Na2CO3,一定有NaCl
C.一定有MgCl2,可能有NaCl D.一定有FeCl3,可能有NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com