
【题目】下列说法错误的是
A. ![]() 、
、![]() 、
、![]() 、H+和H2是氢元素的五种不同粒子
、H+和H2是氢元素的五种不同粒子
B. 石墨和金刚石互为同位素,化学性质相似
C. ![]() 和
和![]() 是不同的核素
是不同的核素
D. 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
【答案】B
【解析】分析:A.微粒指的是原子、分子和离子,1H、2H、3H是氢元素的三种不同原子为氢元素的同位素,H+是氢元素的离子,H2是氢元素的分子;
B.同位素是质子数相同、中子数不同的原子;
C.核素指的是具有一定数目质子和一定数目中子的原子;
D.质子数等于核外电子数,最外层电子数决定元素的化学性质。
详解:A.1H、2H、3H是氢元素的三种不同原子,H+表示氢离子,H2表示氢气分子,是氢元素的五种不同粒子,A正确;
B.石墨和金刚石是同种元素形成的不同种单质,互为同素异形体,不是同位素,B错误,
C.1H和3H质子数相同,质量数不同,属于不同的核素,C正确;
D.质子数等于核外电子数,最外层电子数决定元素的化学性质,这两种原子质子数,最外层电子数相同,化学性质相同,质量数不同物理性质不同,D正确;答案选B。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的反应:2SO2(g) + O2(g) ![]() 2SO3(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
2SO3(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
A.SO2完全转化为SO3 B.各物质浓度均不再改变
C.SO2和SO3的浓度一定相等 D.正、逆反应速率相等且等于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关如图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )
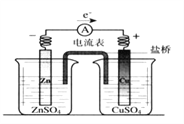
A. 铜片上有气泡逸出
B. 取出盐桥后,电流计依然发生偏转
C. 反应中,盐桥中的K+会移向CuSO4溶液
D. 反应前后铜片质量不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O72-(橙色)+ H2O![]() 2H++ 2CrO42-(黄色)
2H++ 2CrO42-(黄色)
①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。
②向2 mL 0.1 mol·L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+ = 2Cr3+(绿色) + 6Fe3+ + 7H2O。
下列分析正确的是
A. 实验①和②均能证明K2Cr2O7溶液中存在上述平衡
B. 实验②能说明氧化性:Cr2O72-> Fe3+
C. CrO42-和Fe2+在酸性溶液中可以大量共存
D. 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是______________
(2)C、B可按原子个数比1:1形成离子化合物乙的电子式___________
(3)C、D、E三种元素的离子半径由小到大的顺序是____________(用元素符号填写)。
(4)E单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是:____________________
(5)简述比较D与E金属性强弱的实验方法:_______________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。工业上,利用乙烯水化法制乙醇:CH2=CH2+H2O![]() CH3CH2OH。下列有关说法正确的是
CH3CH2OH。下列有关说法正确的是
A. 1mol乙烯和1mol乙醇分别完全燃烧,消耗O2的分子数均为3NA
B. 1mol H2O和H2F+的混合物中所含质子数为10NA
C. 乙醇催化氧化生成1mol乙醛时转移电子数为NA
D. 46g乙醇中所含共价键的数目为7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如图所示。下列说法中正确的是

A. W的最高价氧化物对应的水化物是强酸
B. Y的原子半径在同周期主族元素中最大
C. W的非金属性比Z的弱
D. Z的气态氢化物的稳定性在同主族元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.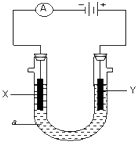
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和KCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,Y电极反应式是、发生反应.在X极附近观察到的现象是电极反应式是检验Y电极反应产物的方法是
(2)若X、Y都是银电极,a是稀硝酸银溶液,开始实验,X极的电极反应式是 .
Y电极的电极反应式是 , 电解前后硝酸银溶液的浓度(变大、变小或不变)若某电极质量增重108克,则在电路中有mol的电子发生转移.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( ) 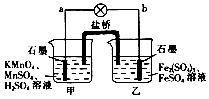
A.b电极上发生还原反应
B.甲烧杯中溶液的pH逐渐减小
C.电池工作时,盐桥中的SO42﹣移向甲烧杯
D.外电路的电流方向是从a到b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com