
【题目】钼是一种过渡金属元素,常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。钼酸钠晶体(Na2MoO4·2H2O)常用于制造阻燃剂和无公害型冷水系统的金属抑制剂。下图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图:
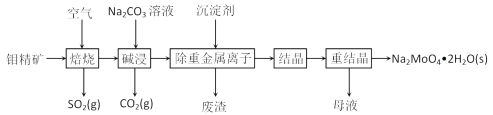
(1)提高焙烧效率的方法有:_____________(写一种)高温下发生焙烧反应的产物为MoO3,请写出该反应的化学方程式 ___________________________________。氧化产物是________________。
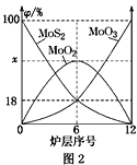
(2)焙烧钼精矿所用的装置是多层焙烧炉,图2为各炉层固体物料的物质的量的百分数(φ)。则x=________。
(3)若在实验室中模拟焙烧操作,需要用到的硅酸盐材料仪器的名称是___________________。
(4)“碱浸”时含钼化合物发生的主要反应的离子方程式为 ______________________。
(5)测得“除重金属离子”中部分离子的浓度:c(MoO42-)=0.20molL1,c(SO42-)=0.01molL1。“结晶”前应先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当BaMoO4开始沉淀时,此时SO42-的浓度_____________。〔已知Ksp(BaSO4)=1×1010,Ksp(BaMoO4)=2.0×108〕
【答案】粉碎固体 2MoS2+7O2![]() 2MoO3+4SO2 MoO3、SO2 64 坩埚 MoO3+CO32-=MoO42-+CO2↑ 0.001mol/L
2MoO3+4SO2 MoO3、SO2 64 坩埚 MoO3+CO32-=MoO42-+CO2↑ 0.001mol/L
【解析】
根据流程:钼精矿(主要成分是MoS2,含少量PbS等)通入空气焙烧,MoS2转化为MoO3,反应为:2MoS2+7O2 ![]() 2MoO3+4SO2,同时2PbS+3O2
2MoO3+4SO2,同时2PbS+3O2 ![]() 2PbS+2SO2,加入碳酸钠碱浸,反应为:MoO3+Na2CO3=Na2MoO4+CO2↑,溶液还含有铅离子,加入沉淀剂Na2S,将铅离子以PbS的形式除去,废渣为PbS,溶液主要为Na2MoO4溶液,将溶液结晶、重结晶得到Na2MoO42H2O,据此分析作答。
2PbS+2SO2,加入碳酸钠碱浸,反应为:MoO3+Na2CO3=Na2MoO4+CO2↑,溶液还含有铅离子,加入沉淀剂Na2S,将铅离子以PbS的形式除去,废渣为PbS,溶液主要为Na2MoO4溶液,将溶液结晶、重结晶得到Na2MoO42H2O,据此分析作答。
(1) 粉碎固体颗粒或者通入过量的空气可以提高矿石的利用率;根据流程“焙烧”时反应的化学方程式为:2MoS2+7O2![]() 2MoO3+4SO2,其中MoS2的Mo、S元素化合价均升高,发生氧化反应,故氧化产物为MoO3和 SO2;
2MoO3+4SO2,其中MoS2的Mo、S元素化合价均升高,发生氧化反应,故氧化产物为MoO3和 SO2;
(2) 由图2可知,6层中存在的固体物质分别为MoS2、MoO3、MoO2,图象分析MoS2、MoO3的物质的量百分比均为18%,根据Mo元素守恒,则MoO2 的物质的量百分比为64%,则x为64;
(3) 由钼酸得到MoO3所用到的硅酸盐材料仪器的名称是瓷坩埚;
(4) Na2CO3的加入与焙烧后的产物即MoO3作用生成CO2↑,而生产的最终产物是钼酸钠晶体,且在后面加入的沉淀剂是为了除去杂质铅的,也就是说钼酸钠在后续过程中没有发生变化,所以反应的化学方程式为 MoO3+Na2CO3=Na2MoO4+CO2↑,则反应的离子方程式为MoO3+CO32-=MoO42-+CO2↑;
(5)已知 c(MoO42-)=0.20molL1,且Ksp(BaMoO4)=2.0×108,则当BaMoO4开始沉淀时,c(Ba2+)= =
=![]() molL1=1.0×107molL1,此时溶液中c(SO42-)=
molL1=1.0×107molL1,此时溶液中c(SO42-)= =
=![]() molL1=1.0×103molL1。
molL1=1.0×103molL1。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】锂亚硫酰氯(Li/SOCl2)电池是实际应用电池系列中比能量最高的一种电池,剖视图如图所示,一种非水的LiAlCl4的SOCl2溶液为电解液。亚硫酸氯既是电解质,又是正极活性物质,其中碳电极区的电极反应式为2SOCl2+4e-=4Cl-+S+SO2↑,该电池工作时,下列说法错误的是( )

A. 锂电极区发生的电极反应:Li-e-=Li+
B. 放电时发生的总反应:4Li+2SOCl2=4LiCl+SO2↑+S
C. 锂电极上的电势比碳电极上的低
D. 若采用水溶液代替SOCl2溶液,电池总反应和效率均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铝钠![]() 是有机合成中的重要还原剂,其合成路线如图所示。
是有机合成中的重要还原剂,其合成路线如图所示。
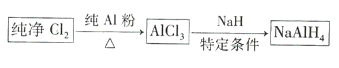
某实验小组利用如图所示的装置制备无水![]() 。
。
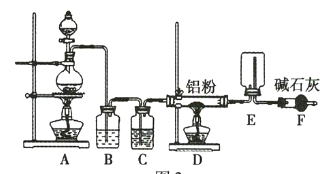
(1)装置F的作用是 _____________________________ 。
(2)![]() 与NaH反应时,需将
与NaH反应时,需将![]() 溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是 _____________________________
溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是 _____________________________
(3)利用氢化铝钠遇水反应生成的氢气的体积测定氢化铝钠样品的纯度。
①其反应的化学方程式为 _____________________________
②设计如图四种装置测定氢化铝钠样品的纯度(假设杂质不参与反应)。
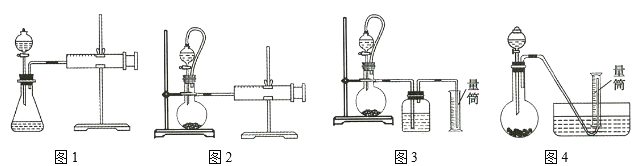
从简约性、准确性角度考虑,最适宜的装置是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,几种难溶电解质的溶度积(Ksp):
化学式 | Mg(OH)2 | MgF2 | Fe(OH)3 | AgCl | Cu(OH)2 | Ag2CrO4 |
溶度积 | 5.6×10-12 | 7.4×10-11 | 4 .0×10-38 | 1.8×10-10 | 2.2×10-20 | 2.0×10-12 |
下列说法不正确的是( )
A. 在Mg(OH)2 的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
B. 在Mg(OH)2 的悬浊液中加入NaF 溶液液后,Mg(OH)2 不可能转化为MgF2
C. CuCl2溶液中混入了一定量的FeCl3溶液,可以通过向溶液中加入CuO的方法,调整溶液的pH,除去Fe3+杂质
D. 向浓度均为1×10-3mol/L 的KCl 和K2CrO4混合液中滴加1×10-3mo/LAgNO3溶液,Cl-先形成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、N的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y的次外层电子数是其电子总数的1/4,离子化合物ZX2是一种储氢材料,W与Y属于同一主族,NY2是医学上常用的水消毒剂、漂白剂。下列叙述正确的是 ( )
A.Y和W分别与X形成的简单化合物的热稳定性:X2 Y > X2W
B.离子半径由大到小的顺序为Y2-< Z2+< N-< W2-
C.ZX2和NY2中含有化学键一致,且微粒个数之比均为1 : 2
D.含氧酸的酸性N > W,可证明非金属性:N > W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6 是一种优良的绝缘气体,分子结构中只有S─F键。已知:1 mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1 mol F─F 、S─F键需吸收的能量分别为160 kJ、330 kJ。则1 mol 固体硫单质参加:S(s)+3F2(g)=SF6(g)反应,完全生成SF6(g)的热效应为( )
A. 吸收430 kJ B. 释放450 kJ
C. 释放1220 kJ D. 释放1780 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3OH是重要的化工原料,工业上用CO与H2在催化剂作用下合成CH3OH,其反应为:CO(g)+2H2(g)CH3OH(g)。按n(CO):n(H2)=1:2,向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是

A. p1<p2
B. 该反应的ΔH>0
C. 平衡常数:K(A)=K(B)
D. 在C点时,CO转化率为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】秋冬季我国北方大部分地区出现严重雾霾天气,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等,城市雾霾中还含有铜等重金属元素。
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、![]() 等二次污染物。
等二次污染物。
①基态N原子的电子排布式___________;C、N和O的第一电离能由大到小的顺序为___________
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________,写出一种与氨硼烷互为等电子体的分子________(填化学式)。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间存在的作用力有________(填序号)。
a.离子键 b.共价键 c.配位键 d.范德华力
②NH4NO3中阴离子的空间构型为________,阳离子的中心原子轨道采用________杂化。

(3)某种镁铝合金可作为储钠材料,该合金晶胞结构如图所示,晶胞棱长为anm,该合金的化学式为____________,晶体中每个镁原子周围距离最近的铝原子数目为___________,该晶体的密度为__________________g/cm3(阿伏伽德罗常数的数值用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为某有机化合物的结构简式:
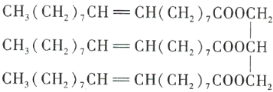
请回答下列问题。
(1)该有机化合物含有的官能团有_______________(填名称)。
(2)该有机化合物的类别是_______________(填字母序号,下同)。
A.烯烃 B.酯 C.油脂 D.羧酸
(3)将该有机化合物加入水中,则该有机化合物_______________。
A.与水互溶 B.不溶于水,水在上层 C.不溶于水,水在下层
(4)该物质是否有固定熔点、沸点?_______________(填“是”或“否”)
(5)能与该有机化合物反应的物质有_______________。
A.![]() 溶液 B.碘水 C.乙醇 D.乙酸 E.
溶液 B.碘水 C.乙醇 D.乙酸 E.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com