
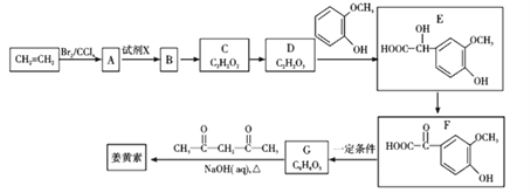
【题目】2018年8月3日我国确诊首例非洲猪瘟疫情。目前某有效药物的主要成分——姜黄素(分子式为C12H20O6)的一种合成路线如图所示:
已知:
①![]()
![]() CH3CHO+CO2↑
CH3CHO+CO2↑
②CH3CHO+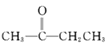
![]()
![]() +H2O
+H2O
回答下列问题:
(1)A的名称为_________;试剂X为_________。
(2)D中含有的官能团名称为_________。
(3)反应D→E的化学方程式为______________________________,其反应类型是________。
(4)下列有关G(C8H8O3)的叙述不正确的是_________(填正确答案编号)。
a.能与NaHCO3溶液反应 b.能与浓溴水发生取代反应
c.能与FeCl3溶液发生显色反应 d.l mol G最多能与3 mol H2发生加成反应
(5)姜黄素的结构简式为_________。
(6)G(C8H8O3)的同分异构体中,写出同时符合下列条件的结构简式为_________。
①苯环上的一取代物只有2种;
②核磁共振氢谱中有4组吸收峰;
③l mol该物质与烧碱溶液反应,最多消耗3 mol NaOH。
【答案】1,2-二溴乙烷 氢氧化钠水溶液 羧基、醛基 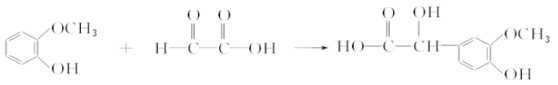 加成反应 ad
加成反应 ad 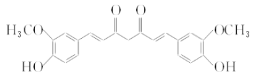
【解析】
乙烯与溴发生加成反应生成A为BrCH2CH2Br,A经反应生成B,根据C、D的分子式,可知A水解为B,B氧化为C,C氧化为D;由D→E的转化及E的结构简式,结合D的分子式可知,D是HOOCCHO;所以B是HOCH2CH2OH,C是OHCCHO;F发生信息①的反应生成G,G是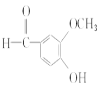 ,
, 与
与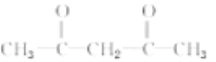 发生信息②的反应生成姜黄素的结构简式是
发生信息②的反应生成姜黄素的结构简式是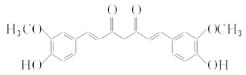 。
。
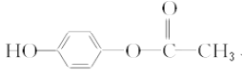
(1)乙烯与溴发生加成反应生成A为BrCH2CH2Br,A的名称为1,2-二溴乙烷;1,2-二溴乙烷水解生成HOCH2CH2OH,所以试剂X为氢氧化钠水溶液。
(2)D是HOOCCHO,含有的官能团名称为羧基、醛基。
(3)反应HOOCCHO与![]() 发生加成反应生成
发生加成反应生成 ,反应的化学方程式为
,反应的化学方程式为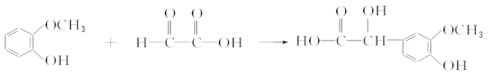 ,其反应类型是加成反应。
,其反应类型是加成反应。
(4)a. 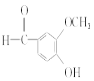 不含羧基,不能与NaHCO3溶液反应,故a错误;
不含羧基,不能与NaHCO3溶液反应,故a错误;
b. 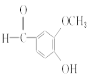 酚羟基的邻位可与浓溴水发生取代反应,故b正确;
酚羟基的邻位可与浓溴水发生取代反应,故b正确;
c. 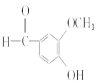 含有酚羟基,能与FeCl3溶液发生显色反应,故c正确;
含有酚羟基,能与FeCl3溶液发生显色反应,故c正确;
d.  中的苯环、醛基可与氢气发生加成反应,l mol G最多能与4 mol H2发生加成反应,故d错误;故选ad;
中的苯环、醛基可与氢气发生加成反应,l mol G最多能与4 mol H2发生加成反应,故d错误;故选ad;
(5)姜黄素的结构简式为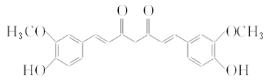 。
。
(6)①苯环上的一取代物只有2种;②核磁共振氢谱中有4组吸收峰;③l mol该物质与烧碱溶液反应,最多消耗3 mol NaOH,同时符合条件的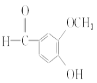 同分异构体是
同分异构体是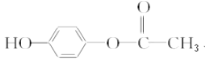 。
。


科目:高中化学 来源: 题型:
【题目】二氧化碳减排和再利用技术是促进工业可持续发展和社会环保的重要措施。
(1)将工业废气中的二氧化碳转化为甲醇,其原理是:CO2(g)+3H2(g)![]() H2O(g)+CH3OH(g) △H=-53.7kJ/mol。308K时,向2L密闭容器中通入0.04 mol CO2和0.08 mol H2,测得其压强(p)随时间(t)变化如图1中曲线I所示。
H2O(g)+CH3OH(g) △H=-53.7kJ/mol。308K时,向2L密闭容器中通入0.04 mol CO2和0.08 mol H2,测得其压强(p)随时间(t)变化如图1中曲线I所示。
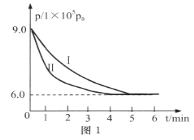

①反应开始至达平衡时,υ(H2)=________;该温度下反应的平衡常数为______。
②若其他条件相同时,只改变某一条件,曲线变化为II,则改变的条件是_____。
(2)还可以通过以下途径实现CO2向CH3OH的转化:
反应I:CO2(g)+H2(g)![]() H2O(g)+CO(g) △H<0
H2O(g)+CO(g) △H<0
反应Ⅱ:2H2(g)+CO(g)![]() CH3OH(g) △H<0
CH3OH(g) △H<0
反应I和反应Ⅱ的平衡常数K随温度T的变化如图2所示。
①根据图中数据分析可知,T1____T2(填“>”、“<”或“=”);T2时,CO2(g)+3H2(g)![]() H2O(g)+CH3OH(g)的平衡常数K=_____。
H2O(g)+CH3OH(g)的平衡常数K=_____。
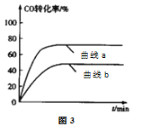
②某科研小组采用反应Ⅱ来合成甲醇,在450℃时,研究了n(H2):n(CO)分别为2:1、3:1时CO转化率的变化情况(如图3),则图中表示n(H2):n(CO)=3:1的变化曲线为______ (填“曲线a"或“曲线b”)。
(3)某同学将H2、CO2的混合气体充入一个密闭容器中,控制其他条件不变,改变起始物中H2、CO2的物质的量之比(用n表示)进行反应2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(g)△H=QkJ/mol,实验结果如图4所示(图中T表示温度):
CH3CH2OH(g)+3H2O(g)△H=QkJ/mol,实验结果如图4所示(图中T表示温度):
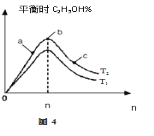
①若图像中T1>T2,则Q______0
②比较a、b、c三点所处的平衡状态中,反应物CO2的转化率最高的是____________,n=______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烷烃A只可能有三种一氯取代物B、C和D,C的结构简式是如图:  ,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下所示。
,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下所示。
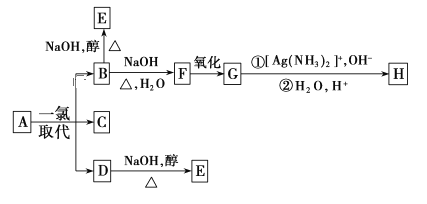
请回答下列问题:
(1)A的结构简式是_________。
(2)H的结构简式是________。
(3)B转化为F的反应属于____反应(填反应类型名称)。
(4)B转化为E的反应属于_____反应(填反应类型名称)。
(5)写出下列物质间转化的化学方程式①B→F:________,②F→G:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:![]() 不同温度下,在三个容器中发生上述反应,相关信息如下表及图所示,下列说法正确的是
不同温度下,在三个容器中发生上述反应,相关信息如下表及图所示,下列说法正确的是
容器 | 甲 | 乙 | 丙 |
容积 | 1 | 1 | 2 |
反应物起始量 | 2mol | 2mol | 2mol |
温度 |
|
|
|
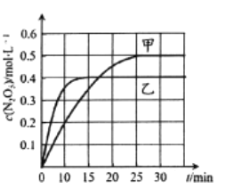
A.![]() 内甲容器中反应的平均速率:
内甲容器中反应的平均速率:![]()
B.![]() ,
,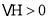
C.平衡时![]() 浓度:
浓度:![]()
D.![]() 时,若起始时间向容器甲中充入
时,若起始时间向容器甲中充入![]() 、
、![]() 、
、![]() 和
和![]() ,则脱硝反应达到平衡前,
,则脱硝反应达到平衡前,![]() 正
正![]() 逆
逆![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验事实的方程式正确的是
A.氯气能使湿润的有色布条褪色:Cl2+H2O![]() 2H+ + Cl + ClO
2H+ + Cl + ClO
B.Na2S 溶液显碱性:S2- + 2H2O![]() H2S↑+ 2OH-
H2S↑+ 2OH-
C.用氨水吸收烟气中的二氧化硫:SO2 + 2OH- = SO![]() + H2O
+ H2O
D.铜片溶解在NaNO3 和稀盐酸的混合液中:3Cu + 8H+ + 2NO![]() =3Cu2+ + 2NO↑ + 4H2O
=3Cu2+ + 2NO↑ + 4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰是重要的微量元素肥料之一,易溶于水,难溶于乙醇。工业上用软锰矿(主要成分是MnO2,含有少量Fe2O3、Al2O3、MgO、SiO2)通过如下简化流程既可脱除燃煤尾气中的SO2,又能制备硫酸锰晶体,实现了资源的综合利用:
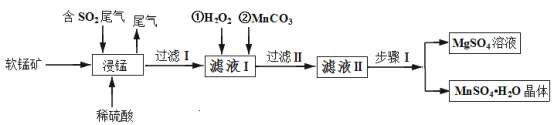
请回答下列问题:
(1)上述流程中第一步浸锰脱硫的好处是_________(答出一点即可)。
(2)写出浸锰过程中软锰矿中的MnO2发生的化学方程式_________。
(3)通过实验如何判定滤液Ⅰ中已加入足量H2O2 __________;加MnCO3的目的是调节溶液的pH,使滤液Ⅰ中的相关离子形成沉淀而除去,请写出 “过滤 Ⅱ”中所得滤渣的主要成分有________。
(4)已知硫酸锰晶体和硫酸镁晶体的溶解度曲线如图所示。
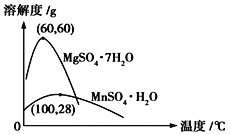
请写出步骤Ⅰ操作_________、趁热过滤;为了保证产品的纯度,同时又减少产品的损失,应选择下列溶液中的________(填选项字母)进行洗涤,实验效果最佳。
A 乙醇 B 饱和K2SO4溶液 C 蒸馏水 D 乙醇水溶液
(5)滤液Ⅱ还可通过加入过量NH4HCO3进行“50℃碳化”得到高纯碳酸锰,反应的离子方程式为_________。“50℃碳化”可能的原因是:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

(1) 腐蚀过程中,负极是 (填图中字母“a”或“b”或“c”);
(2) 环境中的Cl- 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为 ;
(3)若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为 L(标况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下反应N2(g)+3H2(g)2NH3(g)达到化学平衡状态的标志是( )
A.c(N2) :c(H2):c(NH3)=1 :3 :2
B.当![]() 不随时间而变化
不随时间而变化
C.N2与H2的物质的量之和是NH3物质的量的2倍
D.单位时间里每增加1molN2,同时减少2mol NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol/L的NaOH溶液滴定某浓度的二元弱酸(![]() )溶液,所得溶液中各种含X的微粒的物质的量分数(
)溶液,所得溶液中各种含X的微粒的物质的量分数(![]() )与pH的变化曲线如图所示。下列说法正确的是
)与pH的变化曲线如图所示。下列说法正确的是

A. ![]() 的电离常数
的电离常数![]() ,
, ![]() 的水解常数
的水解常数![]()
B. 由水电离出的c(![]() ):a>b
):a>b
C. 曲线![]() 分别表示
分别表示![]() (
(![]() )和
)和![]() (HX-)的变化
(HX-)的变化
D. b点所示溶液中:c(![]() >3c(
>3c(![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com