
【题目】下列反应属于取代反应的是( )
A.由乙烯制取氯乙烷
B.乙烷在光照下与氯气反应
C.苯与H2反应
D.乙醇与O2制取乙醛
科目:高中化学 来源: 题型:
【题目】已知在常温常压下: ①2CH3OH(l)+2O2(g)═2CO(g)+4H2O(g)△H=﹣a kJmol﹣1
②2CO(g)+O2(g)═2CO2(g)△H=﹣b kJmol﹣1
③H2O(g)═H2O(l)△H=﹣c kJmol﹣1
则表示CH3OH(l)燃烧热的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)为了探究Cl2、SO2同时通入H2O发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。
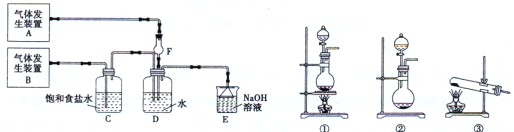
试填空:
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是 ;气体发生装置B应选择①、②、③三种装置中的 (选填序号)。
(2)D装置中主要反应的离子方程式为: 。
(3)为验证通入D装置中气体是Cl2过量还是SO2过量,兴趣小组的同!学准备了以下试剂:氯化铁溶液;氯化亚铁溶液;硫氰化钾溶液;苯酚溶液;品红溶液;酸性高锰酸钾溶液。
若Cl2量:取适量D中溶液滴加至盛有 (试剂名称,下同)的试管中,再加入产生的现象是 ,说明Cl2过量;
若SO2过量:取适量D中溶液滴加至盛有 的试管内,产生的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲配制6.0mol/L的H2SO4溶液1000mL,实验室有三种不同浓度的硫酸:①480mL0.5mol/L的硫酸;②150mL25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的硫酸。有三种规格的容量瓶:250mL、500mL、1000mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为 mol/L (保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为 mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部注入烧杯中混合均匀;
B.用量筒准确量取所需的18mol/L的浓硫酸 mL,注入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D. ;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果省略操作D,对所配溶液浓度有何影响? (填“偏大”、“偏小”或“无影响”)。
(5)进行操作C前还需注意 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,根据所给的10 种元素,回答下列间题.
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | C | N | F | Na | ||||
3 | Na | Mg | Al | Si | S | Cl |
(1)非金属性最强的元素是;
(2)Ne 原子结构示意图为;
(3)C 与N 中,原子半径较小的是;
(4)氯水具有漂白作用,是由于其中含有(填“HCl”或“HClO”)
(5)元素最高价氧化物对应的水化物中,碱性最强的是(填化学式),呈两性的是(填化学式);
(6)元素硅的氧化物常用于制造(填一种高性能的现代通讯材料的名称);
(7)如图为某有机物的球棍模型(其中 ![]() 代表氢原子代表
代表氢原子代表 ![]() 碳原子),
碳原子), 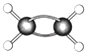 该有机物中碳元素与氢元素的质量比m(C):m(H)= . (相对原子质量C﹣12、H﹣1)
该有机物中碳元素与氢元素的质量比m(C):m(H)= . (相对原子质量C﹣12、H﹣1)
(8)镁是制造汽车、飞机、火箭的重要材料.写出工业上电解熔融氯化镁获得金属镁的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图: 
(1)连接上述仪器的正确顺序是:E接 , 接 , 接 , 接F.
(2)气体发生装置中进行的反应化学方程式是;当0.5mol MnO2参与反应时,被氧化的HCl的质量为 , 生成的Cl2在标准状况下的体积约为 .
(3)在装置中:①饱和食盐水的作用是 , ②浓硫酸的作用是 .
(4)化学实验中检验是否有Cl2产生常用湿润的淀粉﹣KI试纸.如果有Cl2产生,可观察到的现象是 , 写出反应方程式 .
(5)写出尾气吸收装置中进行的反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,则下列说法正确的是( )
A. 0.1mol·L-1的NaHSO4溶液中含有阳离子的物质的量为0.2mol
B. 在标准状态下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
C. 含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目为NA
D. 106 g Na2CO3固体中的阴离子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关浓硝酸的说法中错误的是( )
A.浓HNO3能溶解金属铜,说明其具有强酸性
B.浓HNO3能与碳反应,说明其具有强氧化性
C.浓HNO3不稳定易分解,需要避光保存
D.常温下浓HNO3能使金属铝钝化,可以用铝槽车运输浓HNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com