
【题目】某学生用0.1000mol·L-1标准NaOH溶液滴定未知浓度的盐酸,其操作为以下几步:
A.用标准NaOH溶液润洗碱式滴定管2~3次
B.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
C.把盛有标准NaOH溶液的碱式滴定管固定好,挤压玻璃珠,使滴定管尖嘴充满溶液
D.调节液面至“0”或“0”刻度以下,记下读数
E.移取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定到终点,并记下滴定管液面的读数
(1)下图中属于碱式滴定管的_____(选填:“甲”、“乙”)。

(2)判断到达滴定终点的实验现象是_____。
(3)上述E步操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是_____(填“偏大”或“偏小”或“无影响”)。
(4)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
试计算待测盐酸的物质的量浓度(写出计算过程)________。
【答案】乙 溶液由无色变为浅红色,且半分钟内不褪色 偏大 0.0800 mol·L-1
【解析】
(1) 酸式滴定管下端为玻璃活塞,碱式滴定管下端用橡皮管连接一支带有尖嘴的小玻璃管;
(2)如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)根据![]() ,判断不当操作对相关物理量的影响;
,判断不当操作对相关物理量的影响;
(4)根据关系式HCl~NaOH,来计算出盐酸的浓度。
(1)滴定管下端是橡皮管的为碱式滴定管,故答案为:乙;
(2)本实验是用NaOH滴定盐酸溶液,用酚酞作指示剂,所以终点时的现象为当溶液由无色变为浅红色,且在半分钟内不褪色,故答案为:溶液由无色变为浅红色,且半分钟内不褪色;
(3)锥形瓶用蒸馏水洗涤后,如果再用待测液润洗,会使锥形瓶内溶质的物质的量增大,会造成V(标准)偏大,根据![]() 分析可知,会造成c(待测)偏大,故答案为:偏大;
分析可知,会造成c(待测)偏大,故答案为:偏大;
(4)消耗NaOH溶液的体积为![]() ,则n(HCl)=n(NaOH), c(HCl)×25.00mL=0.1000molL-1×20.00mL;
,则n(HCl)=n(NaOH), c(HCl)×25.00mL=0.1000molL-1×20.00mL;
c(HCl)=0.0800molL-1,故答案为:0.0800 mol·L-1。


科目:高中化学 来源: 题型:
【题目】根据能量变化示意图,下列热化学方程式正确的是( )

A. N2(g)+3H2(g)===2NH3(g) ΔH=-(b-a) kJ·mol-1
B. N2(g)+3H2(g)===2NH3(g) ΔH=-(a-b) kJ·mol-1
C. 2NH3(l)===N2(g)+3H2(g) ΔH=2(a+b-c) kJ·mol-1
D. 2NH3(l)===N2(g)+3H2(g) ΔH=2(b+c-a) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡![]() 是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
I.(查阅资料)
物质 | 熔点 | 沸点 | 化学性质 |
Sn | 231 | 227 | 加热时与 |
| 246 | 652 |
|
|
| 114 | 极易水解 |
Ⅱ![]() (制备产品)
(制备产品)
实验装置如图所示![]() 省略夹持和加热装置
省略夹持和加热装置![]()
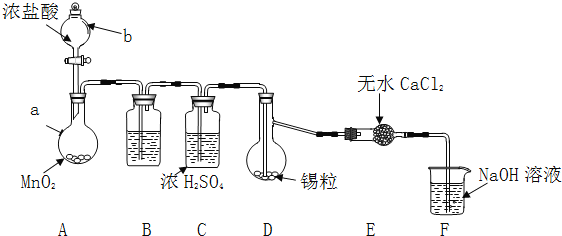
实验步骤:
(1)检查装置气密性后,按图示加入试剂.仪器b的名称是 ______ ,其中无水![]() 的作用是 ______ ,B中的试剂是 ______
的作用是 ______ ,B中的试剂是 ______ ![]() 选填下列字母编号
选填下列字母编号![]() 。
。
A.![]() 溶液
溶液 ![]() 溶液
溶液
![]() 饱和NaCl溶液
饱和NaCl溶液 ![]() 溶液
溶液
(2)先向A中烧瓶内加入盐酸并加热a,当整个装置 ______ 后![]() 填实验现象
填实验现象![]() ,再加热熔化锡粒,反应完后,停止加热。
,再加热熔化锡粒,反应完后,停止加热。
(3)待反应结束后,经 ______ ![]() 填写操作名称
填写操作名称![]() 、洗涤、干燥,可回收利用装置A中未反应完的
、洗涤、干燥,可回收利用装置A中未反应完的![]() 。
。
Ⅲ![]() 探究与反思
探究与反思![]()
(1)装置F中吸收![]() 发生反应的离子方程式是 ______ 。
发生反应的离子方程式是 ______ 。
(2)实验在D中得到的产品很少,经分析装置设计有缺陷,应在D和E之间补充 ______ ![]() 填装置名称
填装置名称![]() 。
。
(3)为验证产品中是否含有![]() ,该小组设计了以下实验方案:
,该小组设计了以下实验方案:![]() 所需试剂从稀
所需试剂从稀![]() 、稀HCl、
、稀HCl、![]() 溶液、
溶液、![]() 溶液、KSCN溶液、蒸馏水中选择
溶液、KSCN溶液、蒸馏水中选择![]()
取适量![]() 产品溶入20mL蒸馏水中,加入 ______ ,若 ______
产品溶入20mL蒸馏水中,加入 ______ ,若 ______ ![]() 填实验现象
填实验现象![]() ,则含有
,则含有![]() ,否则无
,否则无![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物在催化、药物等方面用途广泛。某种席夫碱的合成路线①如下:
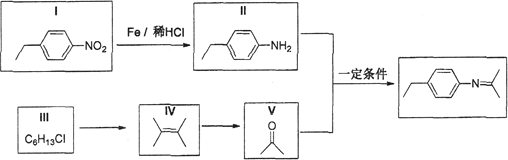
(1)Ⅰ的分子式为__________,1molV完全燃烧至少需要消耗__________mol O2;
(2)III与NaOH水溶液共热反应,化学方程式为___________________________;
(3)IV发生聚合反应生成的高分子化合物的结构简式为_____________________;
(4)结合合成路线①,分析以下合成路线②:
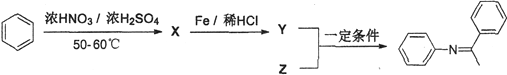
X的结构简式为__________,Z的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
H2O(g)=H2(g)+![]() O2(g)△H=+241.8kJ·mol-1
O2(g)△H=+241.8kJ·mol-1
H2(g)+![]() O2(g)=H2O(1)△H=-285.8kJ·mol-1
O2(g)=H2O(1)△H=-285.8kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88kJ B.吸热44 kJ C.放热44kJ D.吸热2.44 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为了探究SO2的实验室制法和有关化学性质,设计了如下的实验。
实验I:
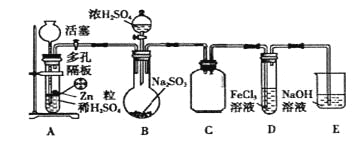
(1)实验基本操作
①多孔隔板与活塞相配合,能起到的作用是_____________________________________.
②该实验制H2时需用浓硫酸配制480mL 3 mol/L的稀硫酸,配制中所需的玻璃仪器有250 mL烧杯、l 00mL量筒、玻璃棒、胶头滴管等,还需_______________________.
③该实验过程中H2所起的作用是_____________________________.
(2)实验时先打开活塞,让装置A内试剂反应一段时间后,关闭活塞,再往装置B中滴入适量浓硫酸反应片刻后,甲、乙两学生分别取装置D中少量溶液,甲学生往其中加入酸性KMnO4溶液,观察到酸性KMnO4溶液紫红色褪去;乙学生往其中加入盐酸酸化的BaCl2溶液,观察到有白色沉淀生成。根据各自实验现象甲、乙学生得出SO2被Fe3+氧化。
①试判断甲、乙学生的结论是否严谨________________(填写选项)。
A.甲学生严谨 B.乙学生严谨 C.甲、乙学生都不严谨
②写出SO2被Fe3+氧化的离子反应方程式_____________________________________.
实验II:
(3)该研究小组为测定SO2催化氧化为SO3的转化率,又设计了如下实验:已知SO3熔点为16.8℃,且忽略空气中CO2的影响).
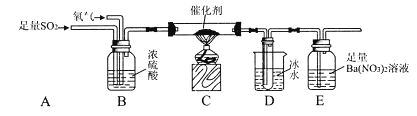
①当停止通入SO2,熄灭酒精灯后,需要继续通入氧气,其目的是:____________________.
②实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是_______________(用含字母的代数式表示,不用化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水溶液中电离的方程式:
HNO3__;
HClO__;
NaHCO3__、___。
(2)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 2CH3OH(g)![]() C2H4(g)+2H2O(g)。 某研究小组将甲醇蒸气以一定的流速持续通过相同量的同种催化剂, 不同温度得到如下图像, 则下列结论不正确的是
C2H4(g)+2H2O(g)。 某研究小组将甲醇蒸气以一定的流速持续通过相同量的同种催化剂, 不同温度得到如下图像, 则下列结论不正确的是
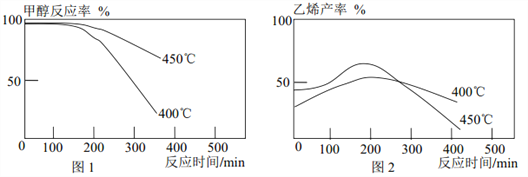
A. 一段时间后甲醇反应率下降可能是催化剂活性下降
B. 综合图 1、 图 2 可知, 甲醇还发生了其他反应
C. 若改变甲醇蒸气的流速, 不会影响甲醇反应率和乙烯产率
D. 制乙烯比较适宜的温度是 450℃左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氮及其化合物的研究具有重要意义。
(1)对于2NO(g)+O2(g) ![]() 2NO2(g)反应包含以下两个基元反应:
2NO2(g)反应包含以下两个基元反应:
① 2NO(g) ![]() N2O2(g)(快) ΔH1<0 ,υ1正=k1正c2(NO)、υ1逆=k1逆c(N2O2);
N2O2(g)(快) ΔH1<0 ,υ1正=k1正c2(NO)、υ1逆=k1逆c(N2O2);
② N2O2(g)+O2(g) ![]() 2NO2(g)(慢) ΔH2<0,υ2正=k2正c(N2O2)c(O2)、υ2逆=k2逆c2(NO2);决定2NO(g)+O2(g)
2NO2(g)(慢) ΔH2<0,υ2正=k2正c(N2O2)c(O2)、υ2逆=k2逆c2(NO2);决定2NO(g)+O2(g) ![]() 2NO2(g)反应速率快慢的基元反应是________(填标号)。一定条件下,反应2NO(g)+O2(g)
2NO2(g)反应速率快慢的基元反应是________(填标号)。一定条件下,反应2NO(g)+O2(g) ![]() 2NO2(g)达到平衡状态,平衡常数K=_______(用含有k1正、k1逆、k2正、k2逆 的代数式表示)
2NO2(g)达到平衡状态,平衡常数K=_______(用含有k1正、k1逆、k2正、k2逆 的代数式表示)
(2)使用SNCR脱硝技术的主反应为:
4NH3(g)+4NO(g)+O2(g) ![]() 4N2(g)+6H2O(g) △H<0
4N2(g)+6H2O(g) △H<0
副反应:4NH3(g)+4O2 (g) ![]() 2N2O (g)+6H2O (g) △H<0
2N2O (g)+6H2O (g) △H<0
下表在密闭体系中进行实验,起始投入一定量NH3、NO、O2,测定不同温度下,在相同时间内各组分的浓度。
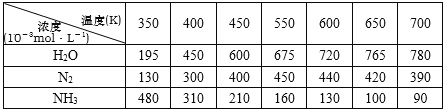
N2浓度变化趋势___________________,试解释原因______________________,
根据表中数据推测,副反应开始发生的温度区间是_____________________。
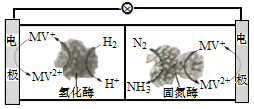
(3)利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。请写出氮气在固氮酶作用下发生的化学反应_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com