
����Ŀ����ҵ�Ͽ������ﴦ���� KCN �ķ�ˮ����һ������������������������£��� KCN ת���� KHCO3�� NH3����� pH��6.7��7.2�����ڶ����ǰѰ�ת��Ϊ���NH3+2O2 ![]() HNO3+H2O�� �����������գ�
HNO3+H2O�� �����������գ�
(1) д����һ����Ӧ�Ļ�ѧ��Ӧ����ʽ_____���ڶ�����Ӧ�Ļ�ԭ������________________����д��ѧʽ����
(2) N ԭ�ӡ�H ԭ�ӡ�O ԭ�ӵİ뾶�ɴ�С��˳����____________________��
(3) ̼ԭ�ӵĽṹʾ��ͼΪ________________��ˮ���ӵĵ���ʽΪ_______________________��
(4) �����£�0.1mol/LK2CO3��KCN��KHCO3 ��Һ���ʼ����� pH ���μ�С���� 0.1mol/L �� KCN��KHCO3��K2CO3 ��Һ�У�CN-��HCO3-��CO32-�����ʵ���Ũ���ɴ�С��˳����_____��
(5) ��ҵ�ϻ������������������� KCN �ķ�ˮ��KCN+2KOH+Cl2=KOCN+2KCl+H2O��2KOCN+4KOH+3Cl2=N2+6KCl+2CO2+2H2O��������ȣ����ﴦ�������ŵ���ȱ���ǣ���дһ������ �ŵ㣺__________________��ȱ�㣺__________________��
���𰸡�2KCN+O2+4H2O =2KHCO3+2NH3 HNO3��H2O N>O>H ![]()
![]() c(HCO3-)>c(CN-)>c(CO32-) ������Һ��й¶ ������Ӧ�Բ�
c(HCO3-)>c(CN-)>c(CO32-) ������Һ��й¶ ������Ӧ�Բ�
��������
����Ϊһ�ۺ���ϰ�⣬�漰��������ԭ��Ӧ����ʽ��д�������жϣ����ʽṹ��ԭ�Ӱ뾶�Ƚϡ�ԭ�ӽṹʾ��ͼ�͵���ʽ��д������ˮ�⣬��ҵ�����Ƚϣ�֪ʶ��϶ࡣ
��1����������������������£��� KCN ת���� KHCO3�� NH3�����������غ�͵����غ�ɵ÷���ʽΪ��2KCN+O2+4H2O =2KHCO3+2NH3���ݻ��ϼ۱仯��Ԫ����0�۱�Ϊ-2�ۿ�֪�ڶ�����Ӧ����������������ԭ������HNO3��H2O��
��2����N��O��H��Ԫ�������ڱ���λֵȷ��ԭ�Ӱ뾶��С��ϵ�� N>O>H��
��3���ݺ�������Ų�����̼��ԭ�ӽṹʾ��ͼΪ��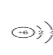 ����ԭ�ӳɼ�����ˮ�ĵ���ʽΪ��
����ԭ�ӳɼ�����ˮ�ĵ���ʽΪ��![]()
(4). �����ζ��������Σ�������ˮ����Һ�Լ��ԣ���Ũ�ȵ��ε�PHֵԽС�������ӵ�ˮ��̶�ԽС������������Ũ��Խ�����������ӵ�Ũ�ȴ�С˳��Ϊ��c(HCO3-)>c(CN-)>c(CO32-)��
��5�������ַ�������ԭ��ȷ���ŵ㣺������Һ��й¶��ȱ�㣺������Ӧ�Բ


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������ʴ�̷�Һ����![]() �ȣ��ͼ���ʴ�̷�Һ[NH4+��Cu��NH3��42+ ��NH3��H2O��]�Ʊ�CuI����ɫ���壩��ʵ����������:
�ȣ��ͼ���ʴ�̷�Һ[NH4+��Cu��NH3��42+ ��NH3��H2O��]�Ʊ�CuI����ɫ���壩��ʵ����������:
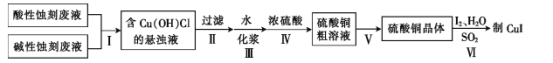
��1��������з����˶����Ӧ,����![]() �����ᷴӦ����Cu��OH��Cl�����ӷ���ʽΪ____��
�����ᷴӦ����Cu��OH��Cl�����ӷ���ʽΪ____��
��2������������pHΪ1~2,80 ���½���,���ʵļ��ȷ�ʽ��____��
��3��������ľ��岽��������Ũ����______��____��
��4�������������װ�ã��гּ�����װ����ʡ�ԣ��н��С�

��װ��a��ʢװŨ�����������������___,Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ___��
��װ��c�з�Ӧ��ɵ�������_____��
����װ��d�е���Һϴ���Ƶõ�CuI��Ŀ����____,Ȼ��������ˮ�Ҵ�ϴ�ӵ�Ŀ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����CaCl2��HCl�Ļ����Һ����μ���Ũ��Ϊ1 mol��L��1��Na2CO3��Һ����Ӧ�����м����Na2CO3��Һ���������������������������ϵ��ͼ��ʾ��
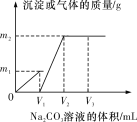
��֪ͼ��V1��V2��1��2��������V2 mL Na2CO3��Һʱ��������Һ��Ũ��Ϊ1 mol��L��1�����Ϊ200 mL����
(1)����V2 mL Na2CO3��Һʱ��������Һ��������________��
(2)ԭ�����Һ��CaCl2��HCl�����ʵ���֮��n(CaCl2)��n(HCl)��________��
(3)m1��________g��m2��________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�ij�����Ŷ������һ�����������洢/ת��װ�ã���ͼ��ʾ�����պ�K2���Ͽ�K1ʱ�����Ⲣ���ܣ��Ͽ�K2���պ�K1ʱ�����硣����˵��������ǣ� ��
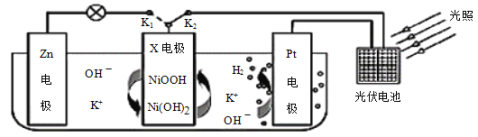
A.����ʱ����Һ��K+��Pt�缫�ƶ�
B.����ʱ��Zn�缫������Һ��pH����
C.����ʱ��X�缫������ԭ��Ӧ
D.����ʱ��X�缫��ӦʽΪNi(OH)2-e-+OH-=NiOOH+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣�����������10��Ԫ�أ�������¸�С�⡣
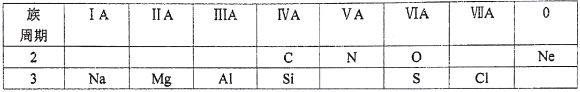
��1��þ��ԭ�ӽṹʾ��ͼΪ____��
��2��H2SO4��HClO4�У����Խ�ǿ����____��
��3��NaOH��Al (OH)3�У��������������������____��������������θ�ᣨ�����ᣩ�����ҩ��÷�Ӧ�����ӷ���ʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�������NO2��O2���Թܵ�����ˮ���У���ַ�Ӧ��ʣ����������Ϊԭ������������![]() ����ԭ���������NO2��O2�����֮����
����ԭ���������NO2��O2�����֮����
A.8��1B.7��3C.1��7D.4��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ������н������·�Ӧ��N2+3H2![]() 2NH3��5min�ڰ������ʵ���������0.1mol����Ӧ����Ϊ
2NH3��5min�ڰ������ʵ���������0.1mol����Ӧ����Ϊ
A.v(H2)=0.02 mol/(L��min)
B.v(N2)=0.01 mol/(L��min)
C.v(NH3)=0.01 mol/(L��min)
D.v(N2)=0.03 mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������80mL0.1mol/L��̼������Һ����ղ��ش��������⣺
��1������80mL1.0mol/L��Na2CO3��Һ��
ʵ��Ӧ��Na2CO3����/g | Ӧѡ������ƿ�Ĺ��/mL |
___ | ___ |
��2������ʱ������ȷ�IJ���˳��Ϊ___������ĸ��ʾ��ÿ����ĸֻ����һ�Σ���
A.��ȷ������Na2CO3���嵹���ձ��У��ټ�����ˮ�ܽ�
B.������ƿ�ǽ������µߵ���ҡ��
C.������ȴ����Һ�ز�����ע������ƿ��
D.��30 mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
E������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���1~2cm��
F����Ϊ��ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶�������
��3�������������������������ҺŨ�Ƚ��к�Ӱ�죿(�ƫ�ߡ���ƫ�͡�����Ӱ�족)
������ʱ���ӿ̶��ߣ������___��
������ƿ������������ˮ�������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.013��105 Pa�£���õ�ijЩ�����ķе���±����ݱ�����������˵����ȷ����(����)
�������� | �е�/�� |
������CH3(CH2)2CH3 | ��0.5 |
������CH3(CH2)3CH3 | 36.1 |
������ | 27.8 |
������ | 9.5 |
������CH3(CH2)4CH3 | 69.0 |
A. �ڱ�״��ʱ��������������
B. ��1.013��105 Pa��20 ��ʱ��C5H12����Һ��
C. ������̼ԭ�������ӣ��е㽵��
D. C5H12��֧�����ӣ��е㽵��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com