
【题目】下列溶液中的氯离子物质的量浓度与 100 mL 1 mol·L-1 的 AlCl3 溶液中氯离子物质的量浓度相等的是
A.200 mL 1 mol·L-1 的 NaClB.200 mL 2 mol·L-1 的NH4Cl
C.100 mL 3 mol·L-1 的 KClD.100 mL 2 mol·L-1 的BaCl2
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】金刚烷(C10H16)的结构如图1所示,它可以看成四个等同的六元环组成的空间构型。立方烷(C8H8)的结构如图2所示。其中金刚烷的二氯代物和立方烷的六氯代物的同分异构体分别是 ( )
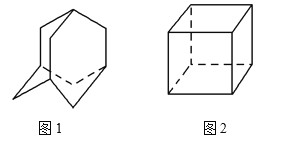
A. 4种和1种 B. 5种和3种
C. 6种和3种 D. 6种和4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡(BaTiO3)主要用于电子陶瓷、PTC热敏电阻、电容器等多种电子元器件的配制中。某工厂以重晶石(主要含BaSO4)为原料生产钛酸钡的工艺流程如图:

回答下列问题:
(1)利用焰色反应的原理可定性鉴别某些金属盐。灼烧钛酸钡样品时,钡的焰色为______(填标号)。
A.砖红色 B.黄绿色 C.紫色 D.黄色
(2)用Na2CO3溶液浸泡重晶石(杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=_________。(已知Kap(BaSO4)=1.2×10-10、Kap(BaCO3)=2.4×10-9)。
(3)流程中“混合”溶液中的钛元素在不同pH时主要以Ti(OH)+、TiOC2O4、TiO(C2O4)23-这三种形式存在(变化曲线如图所示)。实际制备工艺中,先用氨水调节混合溶液的pH在______,再进行“沉淀”,写出该条件下生成草酸氧钛钡晶体的离子方程式:__________。
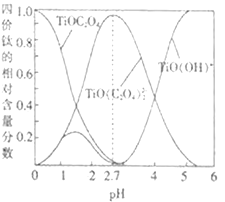
(4)检验草酸氧钛钡晶体是否洗涤干净的操作是_________。
(5)隔绝空气煅烧草酸氧钛钡晶体得到BaTiO3的同时,还能得到气体产物有H2O(g)、________;
(6)BaTiO3成品中C2O42-的含量可以用“氧化还原滴定法”测得。称取m g样品,置于烧杯中,加入50mL0.2 mol·L-1酸性高锰酸钾溶液充分反应后配制成100mL溶液,取20mL该溶液于锥形瓶中用0.1 mol·L-1的硫酸亚铁溶液进行滴定,滴定达到终点的标志是__________,重复滴定3次,平均每次消耗硫酸亚铁溶液的体积为20mL,则BaTiO3成品中C2O42-的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.Fe(OH)3胶体可使水中悬浮物凝聚沉淀,是城市饮用水处理新技术。
(1)实验室如何制取Fe(OH)3胶体,请简述操作___,相应的化学方程式是____。
(2)向Fe(OH)3胶体中逐滴加入硅酸胶体,逐渐出现红褐色沉淀,出现该现象的原因是____。
(3)除去胶体中混有的FeCl3和HCl的方法是___,如何验证胶体已净化完全,请简述方法___。
Ⅱ.已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为____mol·L-1(保留小数点后一位)。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=____mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下面操作造成所配溶液浓度偏高的是___(填序号)。
A.容量瓶用蒸馏水洗涤后未进行干燥处理,底部有少量水残留
B.向容量瓶加水定容时眼睛俯视液面
C.烧杯溶解固体后,用蒸馏水润洗2-3次,将部分洗涤液转入容量瓶中
D.定容摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 室温下,23g NO2气体中含有的分子数目为0.5 NA
B. 0.1mol/L醋酸溶液中含有醋酸分子的数目为0.1NA
C. 常温下,20L pH=12的Na2CO3溶液中含有OH 数目为0.2NA
D. 某密闭容器盛有0.1mol N2和0.3mol H2,一定条件下充分反应,转移电子数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,纵坐标表示导电能力,横坐标表示所加溶液的量,以下各组反应,符合该图的是( )
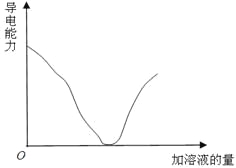
A.Ba(OH)2溶液中滴加稀H2SO4B.NaOH溶液中滴加稀HCl
C.CH3COOH溶液中滴加KOH溶液D.Cu(OH)2悬浊液中滴加HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)该反应的氧化剂是___(填化学式);氧化产物与还原产物的物质的量比是___;如果反应生成0.3mol的单质碘,则转移的电子数目是___。
(2)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,静置,这时候,观察到的现象是___;
(3)若采用如图实验装置将四氯化碳和I2的混合溶液分离。

写出图中仪器的名称:①___;该装置还缺少的仪器是___;
(4)上面实验中用到一定物质的量浓度的稀硫酸,在配制稀硫酸溶液的过程中,下面操作造成所配稀硫酸溶液浓度偏高的是___。
A.溶解的时候溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合液中含有Ba2+,Mg2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如图所示(写出最佳答案)
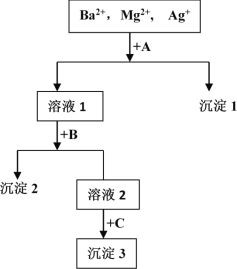
(1)沉淀的化学式:沉淀1______________,沉淀2______________,沉淀3______________;
(2)写出混合液 + A的离子方程式_____溶液1 + B的离子方程式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com