
【题目】钛酸钡(BaTiO3)主要用于电子陶瓷、PTC热敏电阻、电容器等多种电子元器件的配制中。某工厂以重晶石(主要含BaSO4)为原料生产钛酸钡的工艺流程如图:

回答下列问题:
(1)利用焰色反应的原理可定性鉴别某些金属盐。灼烧钛酸钡样品时,钡的焰色为______(填标号)。
A.砖红色 B.黄绿色 C.紫色 D.黄色
(2)用Na2CO3溶液浸泡重晶石(杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=_________。(已知Kap(BaSO4)=1.2×10-10、Kap(BaCO3)=2.4×10-9)。
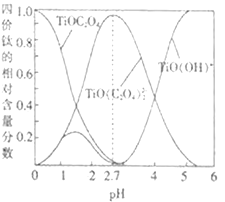
(3)流程中“混合”溶液中的钛元素在不同pH时主要以Ti(OH)+、TiOC2O4、TiO(C2O4)23-这三种形式存在(变化曲线如图所示)。实际制备工艺中,先用氨水调节混合溶液的pH在______,再进行“沉淀”,写出该条件下生成草酸氧钛钡晶体的离子方程式:__________。
(4)检验草酸氧钛钡晶体是否洗涤干净的操作是_________。
(5)隔绝空气煅烧草酸氧钛钡晶体得到BaTiO3的同时,还能得到气体产物有H2O(g)、________;
(6)BaTiO3成品中C2O42-的含量可以用“氧化还原滴定法”测得。称取m g样品,置于烧杯中,加入50mL0.2 mol·L-1酸性高锰酸钾溶液充分反应后配制成100mL溶液,取20mL该溶液于锥形瓶中用0.1 mol·L-1的硫酸亚铁溶液进行滴定,滴定达到终点的标志是__________,重复滴定3次,平均每次消耗硫酸亚铁溶液的体积为20mL,则BaTiO3成品中C2O42-的质量分数为_________。
【答案】B 0.05 2.7 TiO(C2O4)22-+Ba2++nH2O=BaTiO(C2O4)2nH2O↓ 取最后一次洗涤流出液于试管,加入少量硝酸酸化的AgNO3溶液,若试管中无白色浑浊出现,则证明已洗涤干净 CO、CO2 滴入最后一滴硫酸亚铁溶液,溶液由紫红色变为浅绿色,且半分钟不变色 ![]() %
%
【解析】
由制备流程可知,用饱和Na2CO3溶液处理重晶石,将BaSO4转化为易溶于酸的BaCO3,碳酸钡与盐酸反应生成氯化钡,然后氯化钡与四氯化钛、草酸和氨水反应生成BaTiO(C2O4)2nH2O沉淀,过滤、洗涤、干燥、煅烧得到BaTiO3,据此分析解答。
(1)Ba元素的焰色为绿色,Na元素焰色为黄色、K元素焰色为紫色、Ca元素焰色为砖红色,故选B;
(2)将BaSO4转化为易溶于酸的BaCO3的离子方程式为:BaSO4(s)+CO32-(aq)![]() BaCO3(s)+SO42-(aq),该反应的平衡常数K=
BaCO3(s)+SO42-(aq),该反应的平衡常数K=![]() =
=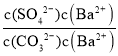 =
=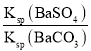 =
=![]() =0.05,故答案为:0.05;
=0.05,故答案为:0.05;
(3)根据“沉淀”时生成草酸氧钛钡晶体中含有TiO(C2O4)22-,因此实际制备工艺中,先用氨水调节混合溶液的pH在2.7,使得钛元素主要以TiO(C2O4)22-存在;根据沉淀的化学式可知,反应的离子方程式:TiO(C2O4)22-+Ba2++nH2O=BaTiO(C2O4)2nH2O↓,故答案为:2.7;TiO(C2O4)22-+Ba2++nH2O=BaTiO(C2O4)2nH2O↓;
(4)BaTiO(C2O4)2nH2O沉淀表面附着氯离子,检验洗涤液中是否存在氯离子即可,故方法为:取最后一次洗涤流出液于试管,加入少量硝酸酸化的AgNO3溶液,若试管中无白色浑浊出现,则证明已洗涤干净,故答案为:取最后一次洗涤流出液于试管,加入少量硝酸酸化的AgNO3溶液,若试管中无白色浑浊出现,则证明已洗涤干净;
(5)煅烧草酸氧钛钡晶体得到BaTiO3的同时,失去结晶水生成水蒸气,草酸根离子生成二氧化碳、CO,所以生成高温下的气体产物有CO、CO2和H2O(g),故答案为:CO、CO2;
(6)高锰酸根离子是紫红色,当滴入最后一滴硫酸亚铁溶液,溶液由紫红色变为浅绿色,且半分钟不变色,证明达到滴定终点;称取m g样品,置于烧杯中,加入50mL0.2 mol·L-1酸性高锰酸钾溶液充分反应后配制成100mL溶液,取20mL该溶液于锥形瓶中用0.1 mol·L-1的硫酸亚铁溶液进行滴定,根据2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,5Fe2++MnO4-+8H+=5Fe3+ +Mn2++4H2O,与亚铁离子反应的高锰酸根离子的物质的量为![]() ×0.1 mol·L-
×0.1 mol·L-![]() =0.002mol,则与C2O42-反应的高锰酸根离子为0.05L×0.2 mol·L-1-0.002mol=0.008mol,则C2O42-为
=0.002mol,则与C2O42-反应的高锰酸根离子为0.05L×0.2 mol·L-1-0.002mol=0.008mol,则C2O42-为![]() ×0.008mol=0.02mol,则m g样品中C2O42-的质量分数为
×0.008mol=0.02mol,则m g样品中C2O42-的质量分数为![]() ×100%=
×100%=![]() %,故答案为:滴入最后一滴硫酸亚铁溶液,溶液由紫红色变为浅绿色,且半分钟不变色;
%,故答案为:滴入最后一滴硫酸亚铁溶液,溶液由紫红色变为浅绿色,且半分钟不变色;![]() %。
%。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】明矾在日常生活中用途非常广泛。用废铝灰(含Al、Al2O3、Fe、Fe2O3、FeO 等)为原料制取明矾的工艺流程如下图。回答下列问题:
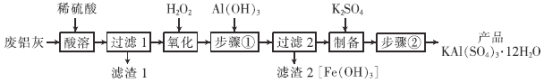
已知:Fe3+开始沉淀到沉淀完全时溶液的pH 为1.9~3.7。
(1)明矾净水的原理是_______________________(用离子方程式表示)。
(2)“酸溶”时,Al2O3溶解的化学方程式为______________________。
(3)“氧化”时,发生反应的离子方程式为_______________。
(4)“步骤①”的目的是______;“滤渣2”经碱洗、水洗、干燥和煅烧,得到的产品的名称是_____(填俗称)。
(5)“步骤②”包含的操作有_________、__________、过滤及干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)某工厂排放出有毒物质NOCl,它遇水就会生成NO3-。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_____。水源中的NO3-对人类健康会产生危害。为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为____
(二)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为:2FeCl3+Cu==2FeCl2+CuCl2。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:
①取少量废液,滴加KSCN溶液显红色。
②取100mL废液,加入足量的AgNO3溶液,析出沉淀43.05g。
③另取100mL废液,加入一定质量的铜片,充分反应后,测得铜片的质量减少了2.56g,再向反应后的溶液中滴加KSCN溶液不变色。
根据探究实验得出结论:
(1)废液中含有的金属离子是______。
(2)100mL废液中Cl-的物质的量是______。
(3)原100mL废液中铜离子的物质的量浓度是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三个反应:①2FeCl3+2KI===2FeCl2+2KCl+I2,②2Fe+3Cl2![]() 2FeCl3,③2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,若某溶液中有Fe2+、I和Cl,要氧化除去I而不除去Fe2+和Cl,可加入的试剂是
2FeCl3,③2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,若某溶液中有Fe2+、I和Cl,要氧化除去I而不除去Fe2+和Cl,可加入的试剂是
A. Cl2B. KMnO4C. FeCl3D. HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某校回收的含银悬浊废水中含有AgCl、Ag(NH3)2NO3、AgNO3、CH3COONH4、NaCl等,设计从废水中回收硝酸银的具体流程如下:
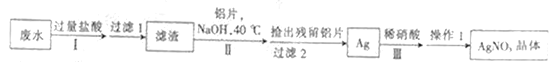
下列说法不正确的是
A. 步骤Ⅱ中发生的主要反应的离子方程:3AgCl+Al+4OH-=3Ag+AlO2-+3Cl-+2H2O
B. 实验中用铝粉代替铝片可以加快反应速率并简化实验操作
C. 步骤Ⅲ中若先将Ag氧化为Ag2O,再加入稀硝酸反应有利于环保
D. 操作Ⅰ包括蒸发浓缩、冷却结晶、过滤、洗涤等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用SCR技术可有效降低柴油发动机NOx排放。SCR工作原理为尿素[CO(NH2)2]水溶液热分解为NH3和CO2,再利用NH3转化NOx,装置如图所示,下列说法不正确的是( )

A.转化NO2过程的化学方程式为:8NH3+6NO2![]() 7N2+12H2O
7N2+12H2O
B.转化器工作过程中,当转移0.6mol电子时,会消耗4.48LNH3
C.尿素水溶液热分解反应不属于氧化还原反应
D.该装置转化NO时,还原剂与氧化剂物质的量之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中的氯离子物质的量浓度与 100 mL 1 mol·L-1 的 AlCl3 溶液中氯离子物质的量浓度相等的是
A.200 mL 1 mol·L-1 的 NaClB.200 mL 2 mol·L-1 的NH4Cl
C.100 mL 3 mol·L-1 的 KClD.100 mL 2 mol·L-1 的BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生反应,化学方程式如下(已配平),Cu+2H2SO4(浓) ![]() CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:
(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为_________。A物质可以与强碱反应生成盐和水。则A应该属于_________(用字母代号填写)。
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(2)一定量的铜片与含1.8mol H2SO4的浓H2SO4充分反应(浓H2SO4过量),如果该反应过程中转移了0.2 mol电子,生成的A气体在标准状况下体积为 _________L(假设气体全部逸出)。
(3)将(2)中反应后所得到的溶液稀释后与足量Ba(OH)2溶液反应,所得沉淀的质量为________________g。写出此过程中发生反应的化学方程式:_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融)![]() 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是____。
A.放在棕色瓶中 B.放在细沙中
C.放在水中 D.放在煤油中
(2)钠长时间放在空气中,最后的产物主要成分是____。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应(如图Ⅰ所示),请写出该反应的化学方程式____________,生成物的颜色为____。将该试管冷却后直立,滴加几滴水(如图Ⅱ所示),发生反应的化学方程式为____________,检验该反应产生的气体的方法是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com