
����Ŀ���������ճ���������;�dz��㷺���÷����ң���Al��Al2O3��Fe��Fe2O3��FeO �ȣ�Ϊԭ����ȡ�����Ĺ�����������ͼ���ش��������⣺
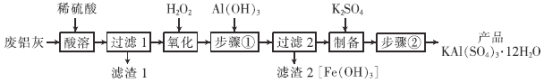
��֪��Fe3����ʼ������������ȫʱ��Һ��pH Ϊ1.9��3.7��
��1��������ˮ��ԭ����_______________________�������ӷ���ʽ��ʾ����
��2����������ʱ��Al2O3�ܽ�Ļ�ѧ����ʽΪ______________________��
��3����������ʱ��������Ӧ�����ӷ���ʽΪ_______________��
��4�������������Ŀ����______��������2������ϴ��ˮϴ����������գ��õ��IJ�Ʒ��������_____�����׳ƣ���
��5����������������IJ�����_________��__________�����˼����
���𰸡�Al3++3H2OAl(OH)3(����)+3H+ Al2O3+3H2SO4=Al2(SO4)3+3H2O 2Fe2++H2O2+2H+=2Fe3++2H2O ������ҺpH��ʹ������ȫ ���� ����Ũ�� ��ȴ�ᾧ
��������
������(��Al��Al2O3��Fe��Fe2O3��FeO ��)��������ϡ�����������ܽⲢ���ˣ��õ�����Al3+��Fe2+��Fe3+��SO42-��������Һ������1Ϊ�������ᷴӦ�����ʣ�����Һ�м���˫��ˮ����Һ�е�Fe2+����ΪFe3+������Fe(OH)3��Al(OH)3�����ܣ������������Һ�м���Al(OH)3��Fe3+ת��Ϊ�����ܵ�Fe(OH)3���������˺�õ�����Al3+��SO42-����Һ������2ΪFe(OH)3������Һ�м���K2SO4�Ƶò�Ʒ��Һ������Һ��������Ũ������ȴ�ᾧ�����ˡ��������յõ���Ʒ�������صľ��壬�ݴ˷������
(1)������ǿ�������Σ����������Al3+ˮ����������������壬�ܹ�����ˮ�������������γɳ�������ȥ���Ӷ��ﵽ�ﵽ��ˮ��Ŀ�ġ��䷴Ӧԭ���÷���ʽ��ʾΪ��Al3++3H2OAl(OH)3(����)+3H+��
(2)��������ʱ��Al2O3�����ᷴӦ������������ˮ����ѧ����ʽΪAl2O3+3H2SO4=Al2(SO4)3+3H2O��
(3)��������ʱ�������������������⣬����Һ�е�Fe2+����ΪFe3+��������Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H+=2Fe3++2H2O��
(4)���������������Һ�м���Al(OH)3�������ǵ�����Һ��pHֵ������Fe(OH)3��Al(OH)3�����ܣ�ʹFe3+��ȫת��ΪFe(OH)3��������ȥ��������2���ijɷ���Fe(OH)3������ʱ�ֽ�����������������һ�ֺ���ɫ��ĩ�����������ϣ����������죻
(5) ����������Ǵ���Һ�л�ò�Ʒ�����������IJ���������Ũ������ȴ�ᾧ�����˼����


 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����£���0.1000 mol/L������ζ�25 mL 0.1000 mol/L Na2CO3��Һ�����õζ���������ͼ��ʾ�������йصζ���������Һ�����Ũ�ȼ�Ĺ�ϵ����ȷ����
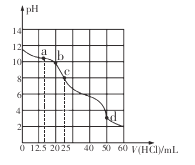
A. a�㣺c( HCO3-)>c(Cl-)>c(C032-)
B. b�㣺c(Na+)+c(H+)=c(Clһ)+c(HCO3-)+c��CO32-��+c��OH-��
C. c�㣺c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
D. d�㣺c��Cl-��=c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�����˵��CO2���������������(����)
A.Na2CO3+H2SO4�TCO2��+H2O+Na2SO4
B.CO2+2NaOH�TNa2CO3+H2O
C.CO2+2Mg![]() 2MgO+C
2MgO+C
D.CO2+Na2O=Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧԭ�����о���ѧϰ��ѧ����Ҫ���ݡ��ش��������⣺
��1����֪������ȼ���ȡ�H����285.5kJmol��1������ˮ���Ȼ�ѧ����ʽΪ_____
��2����298K��101kPa�£�2SO2��g��+O2��g��2SO3��g����H����198kJmol��1������ͬ�����£�2mol SO2�� 1 mol O2��ַ�Ӧ�����շų�������_____198kJ������ڡ���С�ڻ��ڡ������÷�Ӧ��ƽ�ⳣ������ʽK��_____��
��3��25��ʱ���±�ΪһЩ���ܵ���ʵ�������ݣ�
���� | Fe��OH��2 | Cu��OH��2 | Fe��OH��3 |
��ʼ����ʱ��pH | 5.8 | 4.1 | 2.0 |
��ȫ����ʱ��pH | 8.3 | 6.4 | 3.2 |
�����£���ȥ����CuCl2��Һ�к��е�����FeCl2�����������Ϊ��
��Ӧ�ȼ���_____�����Լ����ƣ������������ӷ�Ӧ����ʽΪ_____
���ټ���CuO��������Һ��pH��_____��Χ�ڣ�ʹ��Һ�е�Fe3+ת��ΪFe��OH��3���������ˡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
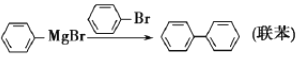
����Ŀ�������״����л��ϳ��м��塣ʵ�����ø����Լ�![]() )�����ͪ��Ӧ�Ʊ������״�����֪:�������Լ��dz����ã�����ˮ��������������̼�����ʷ�Ӧ��
)�����ͪ��Ӧ�Ʊ������״�����֪:�������Լ��dz����ã�����ˮ��������������̼�����ʷ�Ӧ��
��![]()
��
��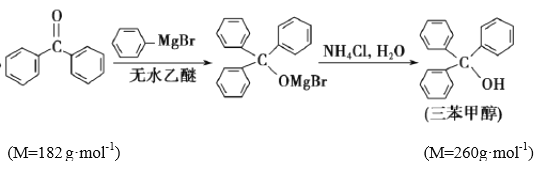
ʵ���������
��ʵ��װ����ͼ1��ʾ��
a.�ϳɸ����Լ�:��������ƿ�м���0.75gþм��������(������)�����Ӻ�װ�ã��ں�ѹ©���м���3.20mL(0.03mol)�屽��15.00mL���ѻ��ȣ���ʼ�����μӻ��Һ���������á�
b.�Ʊ������״�:��5.50g������15.00mL�����ں�ѹ©���л��ȣ�����������ƿ��40������ˮ�ܻ���0.5h������20.00mL�����Ȼ����Һ��ʹ����������
���ᴿ:ͼ2�Ǽ���ˮ��������װ�ã��ø�װ�ý����ᴿ�������ȴ����
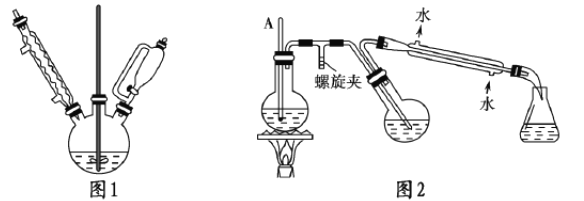
��1��ͼ1ʵ���У�ʵ��װ����ȱ�ݣ�Ӧ������������������____________װ��
��2�����ϳɸ����Լ������У��ͷе����ѵ�������____________________��
���ϳɸ����Լ������У�������Һ�μӹ��콫���¸����Լ������½�����ԭ����______��
��3���ᴿ�����з���A��Һ����������ʱӦ�������еIJ�����_______��
��4���ٷ�Ӧ�������������״�����IJ���Ϊ_______�����ˡ�ϴ��______��
A.�����ᾧ B.��ȴ�ᾧ C.���º�� D.��ֽ����
�����г��˲�����˵����ȷ����_______
A.������ˮ��ʪ��ֽ����ˮ��ͷ������ʹ��ֽ������©���ɰ���
B.��������ת����Һ������ˮ��ͷ������Һ������ʱ��ת�Ƴ���
C.ע������ƿ��Һ��߶ȣ����ӽ�֧�ܿ�λ��ʱ��������Ƥ�ܣ���Һ��֧�ܿڵ���
D.�ó���ϴ�ӳ���ʱ��Ӧ����ˮ��ͷ��ʹϴ�Ӽ�����ͨ��������Լ��ٳ�������ʧ
E.���˲������ڹ��˽�״�ɾ���̫С�ij���
��5������Һ����ȡ20.00mL�����Ȼ�����Һ����ȡҺ��ʱ������______�����ֳ���Һ�ܣ�
��6��ͨ�������õ�����4.00g����ʵ�����Ϊ__________(��ȷ��0.1��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ャҺ��Al(OH)3��MnO2������Na2CrO4�����ǵ��������������ʹNa2CrO4������ȫ��ˮ������ij�о�С��������Ƶĵ�����װ�ã���ͼ2����ʹ��Һ����ɹ�������ͺ���Ԫ����Һ�����������á��ش��͢��е����⡣

��������ķ�������ã�����ͼ�еIJ��ַ�������ͷ�Ӧ����δ������
��1����Ӧ�������Լ�NaOH�ĵ���ʽΪ_________��B��C�ķ�Ӧ����Ϊ__________��C��Al���Ʊ�������Ϊ______________��
��2����С��̽����Ӧ�ڷ�����������D��Ũ�����ϣ������ȣ��ޱ仯��������Cl2���ɣ�����Ӧֹͣ������ʣ�࣬��ʱ�μ����ᣬ�ֲ���Cl2���ɴ��ж�Ӱ��÷�Ӧ��Ч���е������У�����ţ�___________��
a���¶� b��Cl-��Ũ�� c����Һ�����
��3��0.1 mol Cl2�뽹̿��TiO2��ȫ��Ӧ������һ�ֻ�ԭ�������һ����ˮ���TiO2��xH2O��Һ̬���������4.28 kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ__________��
����Ԫ����Һ�ķ��������
��4���ö��Ե缫���ʱ��CrO42-�ܴӽ�Һ�з��������ԭ����__________�������Ԫ�ص�������_________�����������ɵ�����Ϊ___________��д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ũ��Ϊ0.1mol��L��1HF��Һ��ˮ����ϡ�ͣ����и���ʼ�ձ����������
A��c(H+) B��Ka(HF) C��![]() D��
D��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������½�0.01 molCH3COONa��0.005molHCl ����ˮ�����0.5 L�����Һ��
��1����Һ�й���________������
��2����Һ���������������ʵ���֮��һ������0.01 mol ��������____________��
��3����Һ��n ( CH3COO- ) + n ( OH- ) - n( H+ ) =_________mol��
�����������£�ȡŨ����ȵ�NaOH��HCl��Һ����3��2��������ͣ�������Һ��pH����12����ԭ��Һ��Ũ��Ϊ_________________ mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᱵ(BaTiO3)��Ҫ���ڵ����մɡ�PTC�������衢�������ȶ��ֵ���Ԫ�����������С�ij�������ؾ�ʯ(��Ҫ��BaSO4)Ϊԭ���������ᱵ�Ĺ���������ͼ��

�ش��������⣺
(1)������ɫ��Ӧ��ԭ���ɶ��Լ���ijЩ�����Ρ��������ᱵ��Ʒʱ��������ɫΪ______(����)��
A.ש��ɫ B.����ɫ C.��ɫ D.��ɫ
(2)��Na2CO3��Һ�����ؾ�ʯ(���ʲ���Na2CO3��Ӧ)���ܽ�BaSO4ת��ΪBaCO3���˷�Ӧ��ƽ�ⳣ��K��_________��(��֪Kap(BaSO4)��1.2��10��10��Kap(BaCO3)��2.4��10��9)��
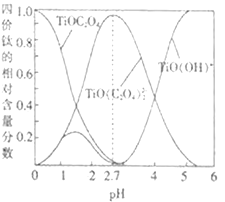
(3)�����С���ϡ���Һ�е���Ԫ���ڲ�ͬpHʱ��Ҫ��Ti(OH)����TiOC2O4��TiO(C2O4)23����������ʽ����(�仯������ͼ��ʾ)��ʵ���Ʊ������У����ð�ˮ���ڻ����Һ��pH��______���ٽ��С���������д�������������ɲ������ѱ���������ӷ���ʽ��__________��
(4)����������ѱ������Ƿ�ϴ�Ӹɾ��IJ�����_________��
(5)�����������ղ������ѱ�����õ�BaTiO3��ͬʱ�����ܵõ����������H2O(g)��________��
(6)BaTiO3��Ʒ��C2O42���ĺ��������á�������ԭ�ζ�������á���ȡm g��Ʒ�������ձ��У�����50mL0.2 mol��L��1���Ը��������Һ��ַ�Ӧ�����Ƴ�100mL��Һ��ȡ20mL����Һ����ƿ����0.1 mol��L��1������������Һ���еζ����ζ��ﵽ�յ�ı�־��__________���ظ��ζ�3�Σ�ƽ��ÿ����������������Һ�����Ϊ20mL����BaTiO3��Ʒ��C2O42������������Ϊ_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com