
����Ŀ����һ��ij�����ŷų��ж�����NOCl������ˮ�ͻ�����NO3-��NOCl�����и�ԭ�Ӿ�����8�����ȶ��ṹ����NOCl�ĵ���ʽΪ_____��ˮԴ�е�NO3-�����ཡ�������Σ����Ϊ�˽���ˮԴ��NO3-��Ũ�ȣ����о���Ա�����ڼ��������������۽�NO3-��ԭΪN2���÷�Ӧ�����ӷ���ʽΪ____
������ij������FeCl3��Һ��ʴ����ͭ�ľ�Ե������ӡˢ��·��������Ӧ�Ļ�ѧ����ʽΪ��2FeCl3+Cu==2FeCl2+CuCl2��ʵ��С���ͬѧ������ӡˢ��·��ķ�Һ�ɷֽ���������̽����
��ȡ������Һ���μ�KSCN��Һ�Ժ�ɫ��
��ȡ100mL��Һ������������AgNO3��Һ����������43.05g��
����ȡ100mL��Һ������һ��������ͭƬ����ַ�Ӧ���ͭƬ������������2.56g������Ӧ�����Һ�еμ�KSCN��Һ����ɫ��
����̽��ʵ��ó����ۣ�
��1����Һ�к��еĽ���������______��
��2��100mL��Һ��Cl-�����ʵ�����______��
��3��ԭ100mL��Һ��ͭ���ӵ����ʵ���Ũ����____��
���𰸡�![]() 10Al+6NO3-+4OH��==3N2+10AlO2-+2H2O Cu2+��Fe2+��Fe3+ 0.3mol 0.1mol/L
10Al+6NO3-+4OH��==3N2+10AlO2-+2H2O Cu2+��Fe2+��Fe3+ 0.3mol 0.1mol/L
��������
��һ��NOCl�����и�ԭ�Ӿ�����8�����ȶ��ṹ����NOCl�ĵ���ʽΪ![]() �����������Ϣ����Ӧ��Ϊ������NO3-��OH-��������Ϊ��N2��H2O���������������μӷ�Ӧ�����ﻹ��AlO2-����Ӧ��Al��AlO2-��AlԪ�ػ��ϼ���0������Ϊ+3�ۣ�������3�ۣ�NO3-��N2������Ԫ�ػ��ϼ���+5�۽���Ϊ0�ۣ�������10�ۣ����ϼ�������С������Ϊ30������ԭ�Ӹ����غ㡢����غ㷴Ӧ�����ӷ���ʽ��10Al+6NO3-+4OH-=10AlO2-+3N2��+2H2O���ʴ�Ϊ��
�����������Ϣ����Ӧ��Ϊ������NO3-��OH-��������Ϊ��N2��H2O���������������μӷ�Ӧ�����ﻹ��AlO2-����Ӧ��Al��AlO2-��AlԪ�ػ��ϼ���0������Ϊ+3�ۣ�������3�ۣ�NO3-��N2������Ԫ�ػ��ϼ���+5�۽���Ϊ0�ۣ�������10�ۣ����ϼ�������С������Ϊ30������ԭ�Ӹ����غ㡢����غ㷴Ӧ�����ӷ���ʽ��10Al+6NO3-+4OH-=10AlO2-+3N2��+2H2O���ʴ�Ϊ��![]() ��10Al+6NO3-+4OH-=10AlO2-+3N2��+2H2O��
��10Al+6NO3-+4OH-=10AlO2-+3N2��+2H2O��
��������ȡ������Һ���μ�KSCN��Һ�Ժ�ɫ��֤����Һ�д���Fe3+��
��ȡ100mL��Һ��������������������Һ����������43.05 g����������43.05 g���Ȼ��������ʵ�����43.05g��143.5g.mol��0.3mol��
����ȡ100mL��Һ������һ��������ͭƬ����ַ�Ӧ���ͭƬ������������2.56g������Ӧ�����Һ�еμ�KSCN��Һ����ɫ��˵����������ȫ�����ģ������˷�Ӧ��2Fe3++Cu��Cu2++2Fe2+���μӷ�Ӧ��ͭ�����ʵ�����2.56g��64g/mol��0.04mol������n��Fe3+����0.08mol��
��1�����ݢٵ�����ͷ�Ӧ2Fe3++Cu��Cu2++2Fe2+��֪��Һ�к��еĽ��������ǣ�Fe3+��Cu2+��Fe2+���ʴ�Ϊ��Fe3+��Cu2+��Fe2+��
��2�������������غ㣬n��Cl-��=n��AgCl��=0.3mol���ʴ�Ϊ��0.3mol��
��3��ԭ��Һ�к��е��Ȼ��������ʵ����ǣ�n(Cl)/3��0.1mol�����ݷ�Ӧ2Fe3++Cu��Cu2++2Fe2+���Ȼ����ܹ�����0.05molCu�����ڢ���ֻ������0.04molCu����100mL��Һ��Cu2+�����ʵ����ǣ�0.05mol-0.04mol��0.01mol��Ũ����0.01mol��0.1L��0.1mol/L���ʴ�Ϊ��0.1mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�����˵��CO2���������������(����)
A.Na2CO3+H2SO4�TCO2��+H2O+Na2SO4
B.CO2+2NaOH�TNa2CO3+H2O
C.CO2+2Mg![]() 2MgO+C
2MgO+C
D.CO2+Na2O=Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ũ��Ϊ0.1mol��L��1HF��Һ��ˮ����ϡ�ͣ����и���ʼ�ձ����������
A��c(H+) B��Ka(HF) C��![]() D��
D��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������½�0.01 molCH3COONa��0.005molHCl ����ˮ�����0.5 L�����Һ��
��1����Һ�й���________������
��2����Һ���������������ʵ���֮��һ������0.01 mol ��������____________��
��3����Һ��n ( CH3COO- ) + n ( OH- ) - n( H+ ) =_________mol��
�����������£�ȡŨ����ȵ�NaOH��HCl��Һ����3��2��������ͣ�������Һ��pH����12����ԭ��Һ��Ũ��Ϊ_________________ mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���
A. ʵ�����г����ű���ʳ��ˮ�ķ����ռ�Cl2
B. ��CO(g)+NO2(g)![]() CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ����
CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ����
C. �����¶��ܹ��ٽ�ˮ�ĵ���
D. �ں���Fe(SCN)3�ĺ�ɫ��Һ�м��������ۣ����ã���Һ��ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��pAg=��lgc(Ag+)��Ksp(AgCl)=1��10��12��Ksp (AgI)=1��10��16����ͼ����10mLAgNO3��Һ����ε���0.1mo1��L��1��NaCl��Һʱ��pAg���ż���NaCl��Һ������仯��ͼ��(ʵ��)������������ȷ����
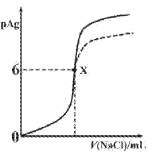
A. ԭAgNO3��Һ�����ʵ���Ũ��Ϊ0.1mol��L��1
B. ͼ��x���ʾ��Һ��Ag+ǡ����ȫ����
C. ͼ��x�������Ϊ(10��6)
D. ����NaCl��Һ����0.1mol��L��1NaI��Һ����ͼ�����յ���Ϊ���߲���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������(C10H16)�Ľṹ��ͼ1��ʾ�������Կ����ĸ���ͬ����Ԫ����ɵĿռ乹�͡�������(C8H8)�Ľṹ��ͼ2��ʾ�����н����Ķ��ȴ��������������ȴ����ͬ���칹��ֱ��� (����)
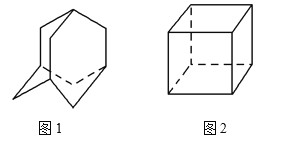
A. 4�ֺ�1�� B. 5�ֺ�3��
C. 6�ֺ�3�� D. 6�ֺ�4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᱵ(BaTiO3)��Ҫ���ڵ����մɡ�PTC�������衢�������ȶ��ֵ���Ԫ�����������С�ij�������ؾ�ʯ(��Ҫ��BaSO4)Ϊԭ���������ᱵ�Ĺ���������ͼ��

�ش��������⣺
(1)������ɫ��Ӧ��ԭ���ɶ��Լ���ijЩ�����Ρ��������ᱵ��Ʒʱ��������ɫΪ______(����)��
A.ש��ɫ B.����ɫ C.��ɫ D.��ɫ
(2)��Na2CO3��Һ�����ؾ�ʯ(���ʲ���Na2CO3��Ӧ)���ܽ�BaSO4ת��ΪBaCO3���˷�Ӧ��ƽ�ⳣ��K��_________��(��֪Kap(BaSO4)��1.2��10��10��Kap(BaCO3)��2.4��10��9)��
(3)�����С���ϡ���Һ�е���Ԫ���ڲ�ͬpHʱ��Ҫ��Ti(OH)����TiOC2O4��TiO(C2O4)23����������ʽ����(�仯������ͼ��ʾ)��ʵ���Ʊ������У����ð�ˮ���ڻ����Һ��pH��______���ٽ��С���������д�������������ɲ������ѱ���������ӷ���ʽ��__________��
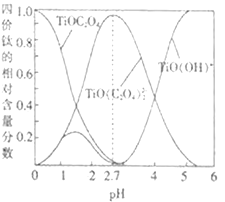
(4)����������ѱ������Ƿ�ϴ�Ӹɾ��IJ�����_________��
(5)�����������ղ������ѱ�����õ�BaTiO3��ͬʱ�����ܵõ����������H2O(g)��________��
(6)BaTiO3��Ʒ��C2O42���ĺ��������á�������ԭ�ζ�������á���ȡm g��Ʒ�������ձ��У�����50mL0.2 mol��L��1���Ը��������Һ��ַ�Ӧ�����Ƴ�100mL��Һ��ȡ20mL����Һ����ƿ����0.1 mol��L��1������������Һ���еζ����ζ��ﵽ�յ�ı�־��__________���ظ��ζ�3�Σ�ƽ��ÿ����������������Һ�����Ϊ20mL����BaTiO3��Ʒ��C2O42������������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������岻��ȱ����Ԫ�أ�Ϊ�˷�ֹ��ȱ���������г�������һ�ּӵ��Σ������ھ���������һ������KIO3��ȥ��ij�о�С��Ϊ�˼��ij�ӵ������Ƿ��е⣬�������йص����ϣ���������ԭ���ǣ�KIO3+5KI+3H2SO4��3I2+3H2O+3K2SO4
��1���÷�Ӧ����������___���ѧʽ�������������뻹ԭ��������ʵ�������___�������Ӧ����0.3mol�ĵ��ʵ⣬��ת�Ƶĵ�����Ŀ��___��
��2����ȡ�����ļӵ��μ�����ˮ�ܽ⣬Ȼ�����ϡ�����KI��Һ��������һ������CCl4�������ã���ʱ�۲쵽��������___��
��3����������ͼʵ��װ�ý����Ȼ�̼��I2�Ļ����Һ���롣

д��ͼ�����������ƣ���___����װ�û�ȱ�ٵ�������___��
��4������ʵ�����õ�һ�����ʵ���Ũ�ȵ�ϡ���ᣬ������ϡ������Һ�Ĺ����У���������������ϡ������ҺŨ��ƫ�ߵ���___��
A���ܽ��ʱ����Һû����ȴ�����¾�ת��
B��ת��ʱû��ϴ���ձ���������
C������Ͳ��ȡŨ�����ϴ����Ͳ����ϴ��Һת�Ƶ�����ƿ
D��ҡ�Ⱥ���Һ����ڿ̶��ߣ��ּ�����ˮ���̶���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com