
【题目】下图是元素周期表的一部分
① | |||||||||||||||||
② | ③ | ④ | ⑤ | ||||||||||||||
⑥ | ⑦ | ⑧ | |||||||||||||||
⑨ | ⑩ |
(1)元素⑨的外围电子的电子排布图为________,元素⑩原子结构示意图为____________
(2)元素③④⑤的电负性由大到小的顺序为____________(填化学用语,下同),其第一电离能由大到小的顺序为_______________,其简单离子半径由大到小的顺序为_______________。
(3)如果在温度接近373K(100℃)时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是_________________。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。写出元素②的最高价氧化物的水化物与NaOH溶液反应的离子方程式________________。
(5)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一主族的是____________。(填元素代号)
②T元素最可能是______(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为________。
【答案】 ![]()
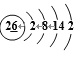 F>O>N F>N>O N3->O2->F- 分子间存在氢键,H2O分子发生缔合 2OH— + Be(OH)2 =BeO2 2—+ 2H2O R 和U p 120°
F>O>N F>N>O N3->O2->F- 分子间存在氢键,H2O分子发生缔合 2OH— + Be(OH)2 =BeO2 2—+ 2H2O R 和U p 120°
【解析】本题分析:本题主要考查元素周期表和元素的性质。
(1)元素⑨是钛,其外围电子排布图为![]() ,元素⑩为铁,其原子结构示意图为
,元素⑩为铁,其原子结构示意图为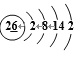 。
。
(2)元素③④⑤分别为碳、氮、氧,因为同周期元素从左到右,电负性逐渐增大,所以它们的电负性由大到小的顺序为F>O>N,因为同周期元素从左到右,第一电离能趋于增大,但是N的2p原子轨道处于半充满的较稳定状态,因而N的第一电离能大于氧,所以它们的第一电离能由大到小的顺序为F>N>O ,其简单离子半径的电子层结构相同,随着核电荷数的增大,离子半径逐渐减小,所以由大到小的顺序为N3->O2->F-。
(3)测定结果比理论值高,其原因是水分子间存在氢键,使得水分子发生缔合。
(4)元素②是铍,它的最高价氧化物的水化物Be(OH)2与NaOH溶液反应的离子方程式2OH-+Be(OH)2=BeO22-+2H2O。
(5)①Q的电离能较大,而且没有突跃,所以Q不易失去电子;R的第二电离能突跃,所以其化合价易呈+1;S的第三电离能突跃,所以其化合价易呈+2;T的第四电离能突跃,所以其化合价易呈+3;U的第二电离能突跃,所以其化合价易呈+1。同一主族元素的主要化合价相同。因此,在周期表中,最可能处于同一主族的是R 和U。
②T原子易失去3个电子,最可能是最外层有3个电子,其中2个s电子,1个p电子,所以T元素最可能是p区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z分别为硼、氯,它们形成的化合物BCl3分子中的中心原子B的价层电子对为3,分子呈平面正三角形,键角为120°。


科目:高中化学 来源: 题型:
【题目】对于可逆反应4NH3+5O2![]() 4NO+6H2O(g),下列叙述不正确的是 ( )
4NO+6H2O(g),下列叙述不正确的是 ( )
A.达到平衡时,4v(O2)正=5v(NO)逆
B.达到平衡状态后,NH3 、O2 、NO 、H2O(g)的物质的量保持不变。
C.达到平衡状态时,若增加容器体积,则反应速率增大
D.若单位时间生成xmolNO的同时,生成xmolNH3,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.在反应中,金属单质只表现还原性,非金属单质只表现氧化性
B.失去电子的物质做氧化剂
C.元素的单质可由氧化或还原含该元素的化合物来制得
D.金属阳离子被还原一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)积极保护生态环境可实现人与自然的和谐共处。
①下列做法会加剧温室效应的是__________(填字母)。
a.植树造林 b.燃煤供暖 c.风力发电
②下列防治“白色污染”的正确方法是_____________(填字母)。
a.使用可降解塑料 b.露天焚烧废旧塑料 c.直接填埋废旧塑料
③为减轻大气污染,多个城市已禁止燃放烟花爆竹。“禁止燃放烟花爆竹”的标识是_____(填字母)。

(2)合理使用化学知识可提高人们的生活质量。
某品牌牙膏的成分有甘油、山梨酸钾、氟化钠等。
①在上述牙膏成分中,属于防腐剂的是_______________。
②甘油的结构简式为____________;油脂水解可生成甘油和_____________。
③氟化钠(NaF)可与牙齿中的羟基磷酸钙[Ca5(PO4)3OH]反应,生成更难溶的氟磷酸钙[Ca5(PO4)3F],从而达到防治龋齿的目的。写出该反应的化学方程式:____________________。
(3)创新发展材料技术科推动人类社会的进步。
①石墨烯(见下图)可用作太阳能电池的电极,这里主要利用了石墨烯的______________性。

②基础工程建设中常用到水泥、玻璃、钢材等。生成水泥和玻璃都用到的原料是__________;在钢材中添加铬、镍等元素的目的是___________。
③新型战斗机常用纳米SiC粉体作为吸波材料。高温下焦炭和石英反应可制得SiC,石英的化学式为________________;高温分解Si(CH3)2Cl2也可制得SiC,同时还生成CH4和一种常见酸性气体,写出该反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有溴苯、乙醇、甲苯、己烯四种液体,只用一种试剂就可以将它们区别开,这种试剂是( )
A.溴水 B.食盐水 C.NaOH溶液 D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)丙烯腈可用“丙烯氨氧化法”生产,生成丙烯腈的热化学方程式为:
CH2=CHCH3(g)+NH3(g)+3/2O2(g)= CH2=CHCN (g)+3H2O(g) △H=-515kJ/mol。该法在生产中有多种副产物生成,其中丙烯醛是主要副产物之一。若气态丙烯与氧气反应生成22.4g气态丙烯醛和水蒸汽,同时放出141.2kJ热量,则反应的热化学方程式为:______,该反应在任何温度下都能自发进行,其原因是______。
(2)图(a)为在某一时间段一密闭体系中生成丙烯腈的反应速率与反应进程的曲线关系。由图可知,t1时刻表示体系改变的反应条件为______;t2时刻表示体系改变的另一反应条件为______,此时平衡______移动(填“正向”、“逆向”或“不”)。

(3)图(b)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为460℃ 。在相同的反应时间内,高于460℃时丙烯腈产率降低的可能原因是______(填序号)。
A.平衡常数变大
B.平衡常数变小
C.副反应增多
D.反应活化能增大
在相同的反应时间内.低于460℃时丙烯腈的产率______(填“是”或“不是”)对应温度下的平衡转化率,判断理由是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com