
【题目】化合物F是一种有机香精的调香剂。实验室由A制备F的一种合成路线如下:
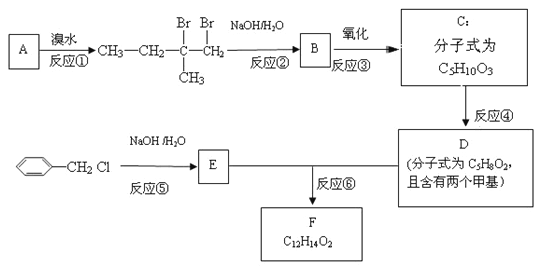
回答下列问题:
(1)化合物A的化学名称是________________________________;
(2)由C生成D和D、E生成F的反应类型分别是_____________、_______________;
(3)C的结构简式为________________________________________________________;
(4)反应⑥的化学方程式为_________________________________________________;
(5)芳香化合物G是E的同分异构体,且G能与金属钠反应放出H2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为3:2:2:1,写出一种符合要求的G的结构简式:_____________
(6)写出用正丙醇(CH3CH2CH2OH)为原料制备化合物CH3COCOOCH2CH2CH3的合成路线_____________________________(其它试剂任选)。
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列各图与表述一致的是( )

A. 图①表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液分别升温至t2℃时,溶质的质量分数B>A
B. 用图②所示装置蒸发FeCl3溶液制备无水FeCl3
C. 图③可以表示向一定量的明矾溶液中逐滴摘加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化
D. 图④电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳是导致温室效应的主要气体,其对应的水溶液碳酸是可乐饮料的主要成分之一。回答下列问题:
(1)下列事实中,能证明碳酸是弱酸的是________
A.碳酸不稳定,易分解为二氧化碳和水
B.用氢氧化钠溶液中和等浓度的碳酸溶液,需要氢氧化钠溶液的体积是碳酸体积的2倍
C.相同条件下,碳酸的导电能力低于相同浓度的硫酸溶液
D.常温下,5.0×10-6mol/L的碳酸溶液pH值为6
(2)煤的燃烧也是导致温室效应的原因之一,其燃烧有下列两种途径:
途径I:C(s)+O2(g)=CO2(g) ΔH=Q1kJ/mol
途径II:先制水煤气:C(s)+H2O(g)=CO(g)+H2(g) ΔH=Q2kJ/mol
再燃烧水煤气:CO(g)+1/2O2(g)=CO2(g) ΔH=Q3kJ/mol
H2(g)+1/2O2(g)=H2O(g) ΔH=Q4kJ/mol
则Q1、Q2、Q3、Q4的数学关系式是___________________________________;
(3)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.6,c(H2CO3)=1.5×10-5 mol/L。
①若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3-+H+的平衡常数K1=_______,该步电离的电离度α=______(已知:10-5.6=2.5×10-6,保留一位小数);
HCO3-+H+的平衡常数K1=_______,该步电离的电离度α=______(已知:10-5.6=2.5×10-6,保留一位小数);
②常温下,0.10 mol/L NaHCO3溶液的pH等于8.0,则此时溶液中c(H2CO3)_____c(CO32-)(填“>”“=”或“<”),原因是__________________________________________________;(用离子方程式和必要的文字说明);
③向饱和碳酸溶液中分别加入下列物质,能使碳酸的第一步电离平衡向右移动的是_________
A.HCl气体 B.NaOH固体 C.Na单质 D.苯酚钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸是重要的一元酸,在有机和无机反应中都有应用。现有25 ℃时,pH=3的醋酸。请回答以下问题:
(1)若向醋酸中加入少量醋酸钠固体,此时溶液中![]() ________(填“增大”“减小”或“不变”)。
________(填“增大”“减小”或“不变”)。
(2)若向醋酸中加入稀NaOH溶液,使其恰好完全反应,所得溶液的pH________(填“>”“<”或“=”)7,用离子方程式表示其原因_____________________________________。
(3)若向醋酸中加入pH=11的NaOH溶液,且二者的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是___________________________________________。
(4)若向醋酸中加入NaOH溶液至溶液恰好呈中性,此时c(Na+)______c(CH3COO-)(填“>”、“<”或“=”)。
(5)若向醋酸中加入一定量NaOH溶液,所得混合液pH=6,则此溶液中c(CH3COO-)-C(Na+)=________mol/L(填写准确数据)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明化学反应有一定的限度,进行了如下探究活动:
探究活动一:取5mL 0.Imol.L-1的KI溶液于试管,滴加0.Imol.L-1的FeCl3溶液5—6滴,振荡;
探究活动二:在上述试管中加入2mL CC14,充分振荡、静置;
探究活动三:取上述静置分层后的上层水溶液于试管,滴加0. Imol.L-1的KSCN溶液5—6滴,振荡。
(1)写出探究活动一中反应的离子方程式____。
(2)探究活动二的实验现象为____。
A.溶液分层,上层呈紫色
B.溶液分层,下层呈紫色
C.溶液分层,均为无色
(3)在探究活动三中,可以证明该化学反应有一定的限度的实验现象是____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由N、B等元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅的制造;由第二周期元素组成的与BCl3互为等电子体的阴离子为_______(填离子符号,填一个)。
(2)氨硼烷(H3N→BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料.
①H3N→BH3中B原子的外围电子排布图_________。
②Ti(BH4)3由TiCl3和LiBH4反应制得,写出该制备反应的化学方程式____;基态Ti3+的成对电子有___对,BH4-的立体构型是____;Ti(BH4)3所含化学键的类型有____;
③氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3;与上述化学方程式有关的叙述不正确的是 _____________
A.氨硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2都是非极性分子
(3)磷化硼(BP)是受到高度关注的耐磨材料,如图1为磷化硼晶胞;
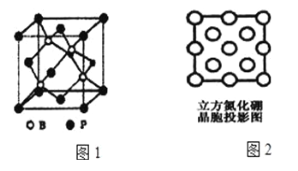
①晶体中P原子填在B原子所围成的____空隙中。
②晶体中B原子周围最近且相等的B原子有____个。
(4)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是__________。图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置______。其中“●”代表B原子,“×”代表N原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是

A. 逐滴加入饱和食盐水可控制生成乙炔的速率
B. 用溴水验证乙炔的性质,不需要除杂
C. KMnO4酸性溶液褪色,说明乙炔具有还原性
D. 将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com