
【题目】由N、B等元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅的制造;由第二周期元素组成的与BCl3互为等电子体的阴离子为_______(填离子符号,填一个)。
(2)氨硼烷(H3N→BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料.
①H3N→BH3中B原子的外围电子排布图_________。
②Ti(BH4)3由TiCl3和LiBH4反应制得,写出该制备反应的化学方程式____;基态Ti3+的成对电子有___对,BH4-的立体构型是____;Ti(BH4)3所含化学键的类型有____;
③氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3;与上述化学方程式有关的叙述不正确的是 _____________
A.氨硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2都是非极性分子
(3)磷化硼(BP)是受到高度关注的耐磨材料,如图1为磷化硼晶胞;
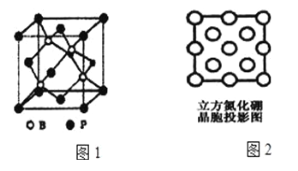
①晶体中P原子填在B原子所围成的____空隙中。
②晶体中B原子周围最近且相等的B原子有____个。
(4)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是__________。图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置______。其中“●”代表B原子,“×”代表N原子。
【答案】NO3-/CO32-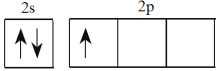 TiCl3+3LiBH4
TiCl3+3LiBH4![]() Ti(BH4)3 + 3LiCl9正四面体配位键、共价键、离子键CD正四面体12氮化硼中硼的原子半径比C大,故其N-B键的键能小于金刚石中的C-C键,所以氮化硼的熔点就越低
Ti(BH4)3 + 3LiCl9正四面体配位键、共价键、离子键CD正四面体12氮化硼中硼的原子半径比C大,故其N-B键的键能小于金刚石中的C-C键,所以氮化硼的熔点就越低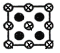
【解析】
(1)根据等电子体原理,原子数相同,价电子数也相同的粒子互为等电子体,所以由第2周期元素组成的与BCl3互为等电子体的阴离子为CO32-或NO3-,故答案为CO32-或NO3-;(2)①B原子的外围电子排布图为![]() ;TiCl3和LiBH4发生复分解反应得到Ti(BH4)3,反应方程式为:TiCl3+3LiBH4
;TiCl3和LiBH4发生复分解反应得到Ti(BH4)3,反应方程式为:TiCl3+3LiBH4![]() Ti(BH4)3 + 3LiCl;基态Ti3+的核外电子排布式为1s22s22p63s23p63d1,故其成对电子数为9;BH4-中B原子的价层电子数为(3+1+4)÷2=4,则其杂化方式为sp3,立体构型为正四面体;BH4-中B原子存在空轨道,与
Ti(BH4)3 + 3LiCl;基态Ti3+的核外电子排布式为1s22s22p63s23p63d1,故其成对电子数为9;BH4-中B原子的价层电子数为(3+1+4)÷2=4,则其杂化方式为sp3,立体构型为正四面体;BH4-中B原子存在空轨道,与
H-能形成配位键,故Ti(BH4)3中所含化学键有离子键、共价键、配位键;③A.氨硼烷N与B间形成的是配位键,故A说法正确;B.在同周期元素中元素的第一电离能随原子序数的增大而增大,而VA族元素的第一电离能要大于相邻元素,则第一电离能:N>O>C>B,故B说法正确;C.反应前CH4中碳原子的轨道杂化类型为sp3,反应后生成的CO2中碳原子的轨道杂化类型为sp;故C说法错误;D.CH4、CO2都是非极性分子,但H2O是极性分子,故D说法错误;答案为CD。(3)①由晶胞结构分析可每个B原子与周围四个P原子成键,同时每个P原子与周围四个B原子成键,P原子位于四个B原子形的正四面体中心,故答案为正四面体;②由晶胞结构可知晶体中B原子周围最近且相等的B原子和P原子周围最近且相等的P原子,以晶胞某个面心的P原子为中心,同一个平面内与之最近且相等的P原子为4个,三个面共12个,故答案为12;(4)氮化硼中硼的原子半径比C大,故其N-B键的键能小于金刚石中的C-C键,所以氮化硼的熔点就越低;立方氮化硼晶胞沿z轴的投影图相当于该晶胞的正视图,其晶胞结构与磷化硼相似,则参照图1可得B与N的相对位置为![]() 。
。


科目:高中化学 来源: 题型:
【题目】甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
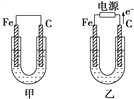
(1)若两池中电解质溶液均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒。
②乙池中阳极的电极反应式是_________________________________________。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式:______________________________________
②甲池中碳极上电极反应式是_______________________________________,
乙池中碳极上电极反应属于________(填“氧化反应”或“还原反应”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种有机香精的调香剂。实验室由A制备F的一种合成路线如下:
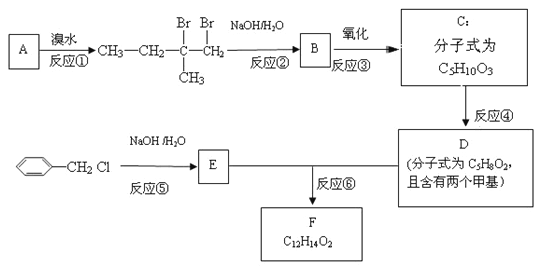
回答下列问题:
(1)化合物A的化学名称是________________________________;
(2)由C生成D和D、E生成F的反应类型分别是_____________、_______________;
(3)C的结构简式为________________________________________________________;
(4)反应⑥的化学方程式为_________________________________________________;
(5)芳香化合物G是E的同分异构体,且G能与金属钠反应放出H2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为3:2:2:1,写出一种符合要求的G的结构简式:_____________
(6)写出用正丙醇(CH3CH2CH2OH)为原料制备化合物CH3COCOOCH2CH2CH3的合成路线_____________________________(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CO和H2S反应可制得羰基硫(COS)。在恒容的密闭容器中发生反应并达到平衡:CO(g)+H2S(g) ![]() COS(g)+H2(g),数据如下表所示:
COS(g)+H2(g),数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
下列说法正确的是( )
A. 上述反应是吸热反应
B. 实验1达平衡时,CO的转化率为70%
C. 实验2达平衡时,a<7.0
D. 实验3达平平衡后,再充入1.0molH2,平衡逆向移动,平衡常数值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式正确的是( )
A. 将NO2通入水中,红棕色消失:3NO2+H2O=2HNO3+O2
B. 漂白粉实现漂白性:CO2+2ClO-+H2O=CO32-+2HClO
C. Na与水反应产生气体:Na+H2O=Na++OH-+H2↑
D. 燃煤时加入石灰石可减少SO2的排放:2CaCO3+O2+2SO2![]() 2CaSO4+2CO2
2CaSO4+2CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硅晶体是信息技术的重要材料。
(1)工业上用石英和焦炭可以制得粗硅。已知反应过程的能量变化如下图


写出用石英和焦炭制取粗硅的热化学方程式______________________________。
(2)某同学设计下列流程制备高纯硅:

①Y的化学式为____________________。
②写出反应I的离子方程式________________________________________。
③写出反应IV的化学方程式________________________________________。
④甲烷分解的温度远远高于硅烷(SiH4),用原子结构解释其原因______________________。
(3)将粗硅转化成三氯硅烷(SiHCl3),进一步反应也可以制得粗硅。其反应:SiHCl3(g)+H2(g)![]() Si(s)+3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比的变化关系如图所示。下列说法正确的是__________(填字母)。
Si(s)+3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比的变化关系如图所示。下列说法正确的是__________(填字母)。

A.该反应是放热反应
B.横坐标表示的投料比可以是![]()
C.该反应的平衡常数随温度升高而增大
D.实际生产中为提高SiHCl3的利用率,可以适当增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 氯化铵溶液,加水稀释时,c(NH4+)/c(Cl-)的值一定减小
B. 0.1 mol·L-1的盐酸和0.1 mol·L-1的弱酸HA溶液分别加水稀释10倍:pH(HA) > pH(盐酸)
C. 已知25℃时,HA的Ka=6.25×10—5,当pH为5.0时,HA溶液中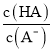 = 0.16
= 0.16
D. 某二元酸的酸式盐NaHA溶液中必然存在:c(H+)+c(A2—)=c(OH—)+c(H2A)
【答案】D
【解析】A、加水稀释时,促进铵根离子水解,所以铵根离子浓度减小的程度大,c(NH4+)/c(Cl-)的值一定减小,选项A正确;B、0.1 mol·L-1的盐酸(pH=1)和0.1 mol·L-1的弱酸HA(pH>1)溶液分别加水稀释10倍后,盐酸的pH=2,HA的pH>2,pH(HA) > pH(盐酸),选项B正确;C、根据HA![]() H++A-,Ka=
H++A-,Ka=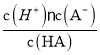 =6.25×10-5,故当溶液的pH为5.0时,c(H+)=10-5 mol·L-1,HA溶液中
=6.25×10-5,故当溶液的pH为5.0时,c(H+)=10-5 mol·L-1,HA溶液中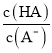 =
=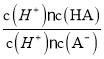 =
=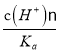 =
=![]() =0.16,选项C正确;D、依据溶液中电荷守恒和物料守恒计算分析,某二元弱酸的酸式盐NaHA溶液中电荷守恒c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),物料守恒c(Na+)=c(H2A)+c(HA-)+c(A2-),计算得到c(OH-)+c(A2-)=c(H+)+c(H2A),选项D错误。答案选D。
=0.16,选项C正确;D、依据溶液中电荷守恒和物料守恒计算分析,某二元弱酸的酸式盐NaHA溶液中电荷守恒c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),物料守恒c(Na+)=c(H2A)+c(HA-)+c(A2-),计算得到c(OH-)+c(A2-)=c(H+)+c(H2A),选项D错误。答案选D。
【题型】单选题
【结束】
24
【题目】有关锌-稀硫酸-铜构成的原电池的一些说法中,正确的是( )
A. 锌片为正极,且锌片逐渐溶解
B. 铜片为负极,且铜片上有气泡
C. 溶液中的H+移向铜极
D. 该电池工作的过程中溶液的酸性始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是常见化合物或单质,有如下转化关系(略去条件和副产品)。

(1)若D为氧气,C为NaAlO2,E为NaOH,则B转化为C的离子方程式为_____________。
(2)若A、B、C均为钠盐溶液且A为Na2CO3,D、E均为卤素单质且有一种为黄绿色气体,则E的化学式为_______________。
(3)若B、D均为质子数小于18的元素原子形成的单质,A、C、E均为氧化物,其中E为SiO2,且D所含元素原子的质子数是B的2倍,A转化为B、B转化为C两个反应均属于置换反应,请写出A的电子式:______________,A转化为B的化学方程式为_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com