
【题目】为了证明化学反应有一定的限度,进行了如下探究活动:
探究活动一:取5mL 0.Imol.L-1的KI溶液于试管,滴加0.Imol.L-1的FeCl3溶液5—6滴,振荡;
探究活动二:在上述试管中加入2mL CC14,充分振荡、静置;
探究活动三:取上述静置分层后的上层水溶液于试管,滴加0. Imol.L-1的KSCN溶液5—6滴,振荡。
(1)写出探究活动一中反应的离子方程式____。
(2)探究活动二的实验现象为____。
A.溶液分层,上层呈紫色
B.溶液分层,下层呈紫色
C.溶液分层,均为无色
(3)在探究活动三中,可以证明该化学反应有一定的限度的实验现象是____________________
科目:高中化学 来源: 题型:
【题目】取Fe和Fe2O3 的混合物 15 g,加入150 mL 2 mol/L 的稀硫酸,固体混合物完全溶解,放出气体 1.68 L(标准状况下),向所得溶液中滴入硫氰化钾溶液,未见颜色变化。若要使该溶液中的铁元素完全转化为沉淀,需加入3 mol/L 的NaOH溶液的体积为( )
A. 150 mL B. 200 mL C. 225 mL D. 250 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对实验仪器特点的描述正确的或实验能达到预期目的的是( )
A.用10mL量筒去量取5.35mL浓硫酸
B.用托盘天平称量6.25g硝酸钾固体
C.量筒的“0”刻度在下面
D.容量瓶上的标识有温度、容量和刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种有机香精的调香剂。实验室由A制备F的一种合成路线如下:
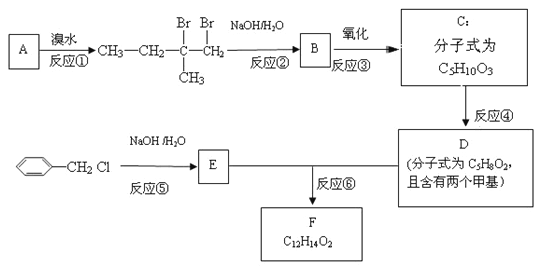
回答下列问题:
(1)化合物A的化学名称是________________________________;
(2)由C生成D和D、E生成F的反应类型分别是_____________、_______________;
(3)C的结构简式为________________________________________________________;
(4)反应⑥的化学方程式为_________________________________________________;
(5)芳香化合物G是E的同分异构体,且G能与金属钠反应放出H2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为3:2:2:1,写出一种符合要求的G的结构简式:_____________
(6)写出用正丙醇(CH3CH2CH2OH)为原料制备化合物CH3COCOOCH2CH2CH3的合成路线_____________________________(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:A+3B![]() 2C+2D在4种不同的情况下的反应速率分别为
2C+2D在4种不同的情况下的反应速率分别为
①v(A )=0.15mol/(L·s) ②v(B )=0.6mol/(L·s) ③v(C )=0.4mol/(L·s) ④v(D )=0.45mol/(L·s)
该反应进行速率最快的是
A. .① B. ②和③ C. ④ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CO和H2S反应可制得羰基硫(COS)。在恒容的密闭容器中发生反应并达到平衡:CO(g)+H2S(g) ![]() COS(g)+H2(g),数据如下表所示:
COS(g)+H2(g),数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
下列说法正确的是( )
A. 上述反应是吸热反应
B. 实验1达平衡时,CO的转化率为70%
C. 实验2达平衡时,a<7.0
D. 实验3达平平衡后,再充入1.0molH2,平衡逆向移动,平衡常数值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式正确的是( )
A. 将NO2通入水中,红棕色消失:3NO2+H2O=2HNO3+O2
B. 漂白粉实现漂白性:CO2+2ClO-+H2O=CO32-+2HClO
C. Na与水反应产生气体:Na+H2O=Na++OH-+H2↑
D. 燃煤时加入石灰石可减少SO2的排放:2CaCO3+O2+2SO2![]() 2CaSO4+2CO2
2CaSO4+2CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 氯化铵溶液,加水稀释时,c(NH4+)/c(Cl-)的值一定减小
B. 0.1 mol·L-1的盐酸和0.1 mol·L-1的弱酸HA溶液分别加水稀释10倍:pH(HA) > pH(盐酸)
C. 已知25℃时,HA的Ka=6.25×10—5,当pH为5.0时,HA溶液中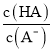 = 0.16
= 0.16
D. 某二元酸的酸式盐NaHA溶液中必然存在:c(H+)+c(A2—)=c(OH—)+c(H2A)
【答案】D
【解析】A、加水稀释时,促进铵根离子水解,所以铵根离子浓度减小的程度大,c(NH4+)/c(Cl-)的值一定减小,选项A正确;B、0.1 mol·L-1的盐酸(pH=1)和0.1 mol·L-1的弱酸HA(pH>1)溶液分别加水稀释10倍后,盐酸的pH=2,HA的pH>2,pH(HA) > pH(盐酸),选项B正确;C、根据HA![]() H++A-,Ka=
H++A-,Ka=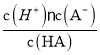 =6.25×10-5,故当溶液的pH为5.0时,c(H+)=10-5 mol·L-1,HA溶液中
=6.25×10-5,故当溶液的pH为5.0时,c(H+)=10-5 mol·L-1,HA溶液中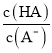 =
=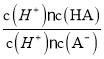 =
=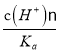 =
=![]() =0.16,选项C正确;D、依据溶液中电荷守恒和物料守恒计算分析,某二元弱酸的酸式盐NaHA溶液中电荷守恒c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),物料守恒c(Na+)=c(H2A)+c(HA-)+c(A2-),计算得到c(OH-)+c(A2-)=c(H+)+c(H2A),选项D错误。答案选D。
=0.16,选项C正确;D、依据溶液中电荷守恒和物料守恒计算分析,某二元弱酸的酸式盐NaHA溶液中电荷守恒c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),物料守恒c(Na+)=c(H2A)+c(HA-)+c(A2-),计算得到c(OH-)+c(A2-)=c(H+)+c(H2A),选项D错误。答案选D。
【题型】单选题
【结束】
24
【题目】有关锌-稀硫酸-铜构成的原电池的一些说法中,正确的是( )
A. 锌片为正极,且锌片逐渐溶解
B. 铜片为负极,且铜片上有气泡
C. 溶液中的H+移向铜极
D. 该电池工作的过程中溶液的酸性始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是形成光化学烟雾和酸雨的重要原因。回答下列问题:
(1)光化学烟雾的产生机理(R为烃基)及烟雾箱(添加有NO和丙烯的空气,并用紫外光照射)中部分物质的浓度随照射时间的变化如图所示。

①80min后NO2浓度减小,是由于发生了反应______(填“I”“Ⅱ”“Ⅲ”或“Ⅳ”,下同),O3开始产生并明显增多,是由于发生了反应_______。
②0~50 min内,v(NO)=______mL·m-3·min-l。
③烟雾箱中丙烯与O2、NO反应会生成甲醛、乙醛及NO2,总反应的化学方程式为_______。
(2)处理含氮氧化物(NO和NO2)烟气的常用方法是碱液吸收法,用质量分数为2%的NaOH溶液吸收不同氧化度[氧化度![]() ,NO氧化度可看作0,NO2氧化度可看作100%]的氮氧化物,其吸收率随时间的变化如图所示。
,NO氧化度可看作0,NO2氧化度可看作100%]的氮氧化物,其吸收率随时间的变化如图所示。

①从反应速率与吸收率得出的结论是___________。
②a=50%时,碱液吸收的离子方程式为___________。
③a=70%时,吸收得到的盐是___________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com