
【题目】钾在氧气中燃烧时得到一种钾的氧化物晶体其结构如图所示,下列有关说法正确的是
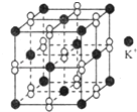
A.该氧化物属于离子晶体,其中只含离子键
B.1mol该晶体中含有的离子数目为3NA
C.晶体中与每个K+距离相等且最近的K+共有8个
D.晶体中每个K+同时吸引着6个阴离子
【答案】D
【解析】
A、晶体中K+离子位于晶胞的顶点和面心,晶体中K+离子个数为8×1/8+6×1/2=4。阴离子位于晶胞的边上和体心处,则阴离子个数是12×1/4+1=4,所以晶胞中阴阳离子的个数之比为1:1,因此氧化物是KO2,该氧化物属于离子晶体,既含有离子键又含有共价键,A错误;
B、1molKO2中含有1mol K+,1molO2-,含有的离子数目是2NA,B错误;
C、晶体中与每个K+距离相等且最近的K+位于晶胞的顶点和面心处,共有8×3×1/2=12个,C错误;
D、根据晶胞结构可知晶体中每个K+同时吸引着6个阴离子,即以顶点为中心6个阴离子分别位于上下前后左右各2个,D正确;
答案选D。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪组原子均可产生NMR现象( )
A.18O 31P 119Sn
B.27Al 19F 12C
C.元素周期表中第一周期所有元素的原子
D.元素周期表中第ⅤA族所有元素的原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年,嫦娥四号成功在月球着陆。探测器上的五星红旗由一类特殊的聚酰亚胺(化合物H)制成。以下是H的合成路线:
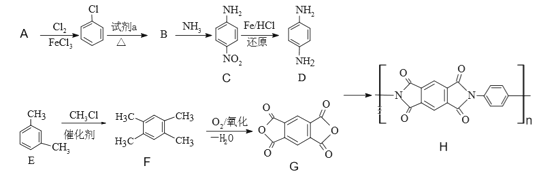
已知: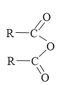 +R’-NH2→
+R’-NH2→![]() +RCOOH
+RCOOH
(1)A 结构简式是________________,E的名称___________。
(2)试剂a是_____________,其化学方程式___________________。
(3)B→C的反应类型________;C中含有的官能团名称为___________。
(4)写出 D+G→H 的化学反应方程式_____________。
(5)写出一种苯环上一氯代物有三种,核磁共振氢谱为6:4:2:1:1的F的同分异构体的结构简式_______________。(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了监测某烟道气中的NOx的含量,选用如下采样和检测方法。

I.采样步骤
①检验系统气密性;②加热器将烟道气加热至140℃;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
(1)A中装有无碱玻璃棉,其作用是___。采样步骤②加热烟道气的目的是___。
C中填充的干燥剂最好的选择是___(选填编号)。
a.碱石灰 b.无水CuSO4 c.P2O5
(2)用实验室常用仪器组装一套装置,其作用与D(装有碱液)相同,在虚线框中画出该装置的示意图,标明气体的流向及试剂___。

Ⅱ.NOx含量的测定
将一定量的气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3-,然后加入过量的FeSO4标准溶液,充分反应后,再用K2Cr2O7标准溶液滴定剩余的Fe2+。
(3)NO被H2O2氧化为NO3-的离子方程式是___。滴定操作使用的玻璃仪器主要有___。
(4)滴定过程中发生下列反应:3Fe2++NO3+4H+=NO↑+3Fe3++2H2O、Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O。判断下列情况对NOx含量测定结果的影响(填“偏高”、“偏低”或“无影响”):若缺少采样步骤③,会使测试结果___;若FeSO4标准溶液部分变质,会使测定结果___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)物质的分离与提纯是化学的重点,请根据下列实验目的,分别选择相应的操作和实验装置。下列为操作:
a.蒸馏 b.结晶法 c.加适量水,过滤 d.加热(或灼烧) e.加适量盐酸,蒸发 f.萃取分液 g.分液 h.升华
下列为实验装置:
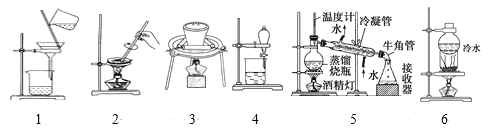
(1)从碘水中提取碘:___、__。(分别填操作序号及实验装置图编号,下同)。
(2)除去氧化钙中的碳酸钙:___、___。
(3)除去硫酸钡中的硝酸钾:___、___。
(4)分离固体细沙和碘的方法:___、___。
(5)除去氯化钠晶体中的碳酸钠:___、__。
(6)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合液(两者互溶):__、_。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的CaCl2、MgCl2、硫酸钠以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
![]()
(1)第⑤步中,操作B是___(填操作名称),第④步中,试剂Y是___。
(2)判断试剂X过量的方法是___。
(3)写出第②步中涉及反应的化学方程式___。
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、___(填化学式)。
(5)此实验方案尚需完善,具体步骤是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]()
![]() (R、R'可表示烃基或官能团)。A可发生如图转化(方框内物质均为有机物,部分无机产物已略去):
(R、R'可表示烃基或官能团)。A可发生如图转化(方框内物质均为有机物,部分无机产物已略去):
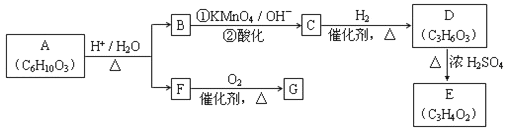
请回答:
(1)F的蒸气密度是相同条件下H2密度的31倍,且分子中无甲基。已知1mol F与足量金属钠作用产生H2 22.4L(标准状况),则F的分子式是_____,名称是__________.
(2)G与F的相对分子质量之差为4,则G具有的性质是______(填字母)
a.可与银氨溶液反应 b.可与乙酸发生酯化反应
c.可与氢气发生加成反应 d.1mol G最多可与2mol新制Cu(OH)2发生反应
(3)D能与NaHCO3溶液发生反应,且两分子D可以反应得到含有六元环的酯类化合物,E可使溴的四氯化碳溶液褪色,则D→E的化学方程式是______________,该反应类型是_____反应
(4)H与B互为同分异构体,且所含官能团与B相同,则H的结构简式可能是:_________.
(5)A转化为B和F的化学方程式是__________.
(6)A的同分异构体含有两种官能团,该化合物能发生水解,且1mol该化合物能与4mol银氨溶液反应,符合该条件的同分异构体一共有__________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,正确的是( )

A.用如图装置进行实验,将装置①中的AlCl3滴入装置②浓氢氧化钠溶液中可观察到有大量白色沉淀产生
B.利用装置③可制备氢氧化亚铁并长时间观察其颜色
C.装置④不能验证Na2CO3和NaHCO3两种固体的热稳定性
D.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来说明金属铝的熔点较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)中国古代四大发明之一——黑火药,它的爆炸反应为2KNO3+3C+S![]() A+N2↑+3CO2↑。
A+N2↑+3CO2↑。
①除S外,上列元素的电负性从大到小依次为____。
②在生成物中,含极性共价键的分子的中心原子轨道杂化类型为____。
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为____。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为____,Q2+的未成对电子数是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com