
【题目】下列物质中不含硅酸盐的是( )
A.陶瓷B.玻璃C.水泥D.生石灰
科目:高中化学 来源: 题型:
【题目】下列有关化学用语使用正确的是
A. 次氯酸的结构式:H—Cl—O B. 乙醇的结构简式: C2H6O
C. 硫离子的结构示意图:![]() D. 丙烷分子的球棍模型:
D. 丙烷分子的球棍模型:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 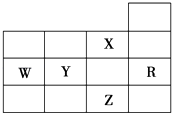
A.W元素的第一电离能小于Y元素的第一电离能
B.Y、Z的阴离子电子层结构都与R原子的相同
C.p能级未成对电子最多的是Z元素
D.X元素是电负性最大的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】RNA 水解后,得到的化学物质是
A .氨基酸、葡萄糖、碱基
B .氨基酸、核糖、核苷酸
C .核糖、碱基、磷酸
D .脱氧核糖、碱基、磷酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
A. C14H10O5 B. C14H16O4 C. C14H18O5 D. C14H22O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以天然气为原料合成甲醇。有关热化学方程式如下:
①2CH4(g)+O2(g)![]() 2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
③2CH4(g)+O2(g)![]() 2CH3OH(g) ΔH3=-251.0 kJ·mol-1
2CH3OH(g) ΔH3=-251.0 kJ·mol-1
(1)ΔH2=____kJ·mol-1。
(2)在体积可变的密闭容器中投入1 mol CO和2 mol H2,在不同条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。
CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。

①M点时,H2的转化率为____;压强:p1____(填“>”“<”或“=”)p2。
②反应速率:N点v正(CO)____(填“>”“<”或“=”)M点v逆(CO)。
③若压强为p1、在1 L恒容密闭容器中进行上述反应(起始投料不变),在不同温度下上述反应的平衡常数的对数(lg K)如图2所示。则温度为506 K时,平衡常数K=____(保留三位小数),B、C、D、E四点中能正确表示该反应的lg K与T的关系的点为____。
④在2 L恒容密闭容器中充入a(a>0) mol H2、2 mol CO和7.4 mol CH3OH(g),在506 K下进行上述反应。为了使该反应逆向进行,a的范围为________。
(3)某甲醇-空气燃料电池以KOH溶液为电解质溶液。当KOH全部转化成KHCO3时停止放电,写出此时负极的电极反应式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用X表示原子:
(1)中性原子的中子数:N=________。
(2)阴离子的中子数:AXn-共有x个电子,则N=________。
(3)中性分子中子数:12C18O2分子中,N=________。
(4)A2-原子核内有x个中子,其质量数为m,则n gA2-所含电子的物质的量为________mol。
(5)某元素的同位素X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:X元素在周期表中的位置_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
B.0.5mol C2H6分子中所含C﹣H共价键数为2NA
C.标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA
D.1mol甲基﹣CH3所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,11.2 LCH2Cl2含极性共价健数目为2NA
B. 0.1 mol Cu与40mL10 mol.L-1浓硝酸作用能生成NO2的分子数为02NA
C. 将0.2 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+的数目小于0.2NA
D. 30g葡萄糖和乙酸的混合物中含碳原子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com