
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 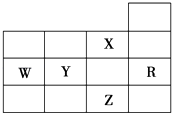
A.W元素的第一电离能小于Y元素的第一电离能
B.Y、Z的阴离子电子层结构都与R原子的相同
C.p能级未成对电子最多的是Z元素
D.X元素是电负性最大的元素
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】氰基烯酸酯在碱性条件下能快速聚合为 ,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(H)的合成路线如下:

已知:①A的相对分子量为58,氧元素质量分数为0. 276,核磁共振氢谱显示为单峰;

回答下列问题:
(1)A的化学名称为____________。
(2)G的结构简式为________________,G中的含氧官能团是________________。(填官能团名称)
(3)由B生成C的反应类型为_______________,由C生成D的反应类型为_____________。
(4)由E生成F的化学方程式为________________________________。
(5)H的同分异构体中,含有酯基,能发生银镜反应、核磁共振氢谱之比是1:1:3的同分异构体结构简式_____________________________________________。(写两种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食醋的总酸量即一定体积的食醋原液所含醋酸的质量,单位是gL﹣1或g/100mL.国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.
(1)用酸碱滴定法测定某食醋样品中的总酸量时,下列说法中正确的是(双选).
A.用NaOH溶液滴定时反应的离子方程式为H++OH﹣=H2O
B.食醋样品通常需要预先稀释一定倍数后再进行滴定
C.用NaOH溶液滴定时,可使用酚酞或甲基橙作指示剂
D.若测得样品的物质的量浓度为0.75molL﹣1 , 则其总酸量为45gL﹣1
(2)某同学仔细观察该食醋样品的标签,发现其中还含有作为食品添加剂的苯甲酸钠(C6H5COONa),他想用理论验证醋酸与苯甲酸钠不会发生离子互换反应,需查找在一定温度下醋酸与苯甲酸的 .
A.pH
B.电离度
C.电离常数
D.溶解度
(3)常温下,用0.1000molL﹣1 NaOH溶液分别滴定20.00mL 0.1000molL﹣1 HCl溶液和20.00mL 0.1000molL﹣1 CH3COOH溶液,得到两条滴定曲线,如图所示. 
①滴定醋酸溶液的曲线是(填“图1”或“图2”);滴定曲线中a= mL;
②E点pH>8的原因是(用离子方程式表示): .
(4)测定食醋的总酸量实验中,配制NaOH溶液和稀释食醋所用的蒸馏水必须煮沸,目的是 .
(5)实验时,吸取食醋样品10mL于100mL容量瓶中定容.移取定容后的溶液20mL于锥形瓶中,加入1~2滴指示剂,用浓度为c molL﹣1的NaOH标准溶液滴定,平行测定三次,消耗NaOH溶液的平均体积为V mL.则原食醋样品的总酸量= g/100mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 都为短周期元素,A 原子失去一个电子后成为一个质子;C 的-1 价阴离子与氖原子具有相同的电子层结构;D在C 的下一周期,D可与同周期的B形成 BD2型离子化含物;E 和 C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题。
(1)B元素在元素周期表中的位置是____________。
(2)A与 E 形成的最简单化合物的电子式为____________。
(3)C的氢化物与 D的氢化物的沸点相比较: ____________(用化学式表示,且用>符号连接)。 解释原因______________。
(4)E 的氢化物与 E 的最高价氧化物对应水化物反应的生成物中含有的的化学键有____________。
(5)E 的最高价氧化物对应的水化物的稀溶液与过量铁粉发生反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学电源的说法不正确的是( )
A.我们可以根据硫酸密度的大小来判断铅蓄电池是否需要充电
B.燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的化学电源
C.普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,就不能再使用了
D.由Ag2O和Zn形成的碱性银锌纽扣电池,发生电化学反应时,Zn作为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al、Fe、Cu 是重要的材料元素,在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe2+的核外电子排布式为[Ar]______,有__个未成对电子。
(2)氯化铝熔点为194℃,而氧化铝熔点为2050℃,二者熔点相差很大的原因是_____。
(3)已知Al 的第一电离能为578kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因________。
(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是____;SiO2中Si原子采取____杂化。
(5)一种铜的溴化物晶胞结构如图所示:该晶胞中铜的配位数是___,与溴紧邻的溴原子数目是________,由图中P点和Q点的原子坐标参数可确定R点的原子坐标参数为________;已知晶胞参数为apm,其密度为_______g/cm3 (列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)是一种重要的化工试剂,氯化法是合成硫酰氯(SO2Cl2)的常用方法。实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出);

已知:①SO2(g)+Cl2(g)=SO2Cl2 △H=-97.3kJ/mol。
②常溫下硫酰氯为无色液体,熔点-54.1℃,沸点69.1℃,在潮湿空气中“发烟”。
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氧气。
回答下列问题:
(1)硫酰氯在潮湿空气中“发烟”的原因___________(用化学方程式表示)。
(2)装置B中盛放的试剂是________;仪器D的名称为________。
(3)装置E的作用是_____,E中冷凝水的入口是____(填“a”或“b”);整套装置存在的一处缺陷是_______。
(4)当装置A中生成氯气1.12L(已折算成标准状况)时,硫酰氯的产率为44%,则最终得到纯净的硫酰氯_______g。
(5)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为___________________,分离两种产物的方法是______________。
(6)硫酰氯的工业品中常含有少量硫酸,请你设计实验验证其中含有硫酸(写出实验方案及相关实验现象,不必写出具体实验操作________。可选试剂:稀盐酸、稀硫酸、BaCl2溶液、蒸馏水、石蕊试液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】压强变化不会使下列化学反应的平衡发生移动的是 ( )
A. H2(气)+I2(气) ![]() 2HI(气)
2HI(气)
B. 3H2(气)+N2(气) ![]() 2NH3(气)
2NH3(气)
C. 2SO2(气)+O2(气) ![]() 2SO3(气)
2SO3(气)
D. C(固)+CO2(气) ![]() 2CO(气)
2CO(气)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com