
【题目】铜是人类发现最早并广泛使用的一种金属。回答下列问题:
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为__________________。
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式____________。配制的FeCl3溶液应保持_______(填“酸性”“碱性”或“中性”),原因是_____________。
(3)溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I―=2CuI↓+I3- ②I3- +2S2O32-=3I―+2S2O62-
反应①中的氧化剂为_____________。现取20.00 mL含Cu2+的溶液,加入足量KI充分反应后,用0.1000 mol·L1 Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液25.00 mL,此溶液中Cu2+的浓度为_______mol·L1。
【答案】Cu+H2O2+H2SO4=CuSO4+2H2O Cu+2Fe3+=Cu2++2Fe2+ 酸性 防止Fe3+水解生成Fe(OH)3 Cu2+ 0.125
【解析】
(1)铜与稀硫酸不反应,稀硫酸的作用是提供酸性环境,增强过氧化氢的氧化性;
(2)由于Fe3+易水解,因此配制的FeCl3溶液要保持在酸性条件下,抑制水解;
(3)根据转移的电子数守恒可列关系式求解。
(1)H2O2在酸性条件下具有强氧化性,能跟铜反应,反应的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O。
(2)FeCl3溶液刻蚀印刷电路板铜箔,是铁离子把铜氧化成铜离子,反应的离子方程式为Cu+2Fe3+=Cu2++2Fe2+。由于Fe3+易水解,因此FeCl3溶液应保持酸性,目的是防止Fe3+水解生成Fe(OH)3。
故答案为:Cu+2Fe3+=Cu2++2Fe2+ ;酸性;防止Fe3+水解生成Fe(OH)3 。
(3)反应①中的铜的化合价由+2→+1价,化合价降低,因此,氧化剂为Cu2+。
根据反应关系:2S2O32- ![]() I3-
I3- ![]() 2Cu2+
2Cu2+
0.1mol/L![]() 0.025L x
0.025L x![]() 0.02L
0.02L
0.1mol/L![]() 0.025L= x
0.025L= x![]() 0.02L,解得x=0.125mol/L
0.02L,解得x=0.125mol/L
故答案为:Cu2+ ;0.125。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是

A. 整个反应过程中,氧化剂为O2
B. 放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-
C. 放电时,当电路中通过0.1 mol电子的电量时,有0.1 mol Li+透过固体电解质向Cu极移动,有标准状况下1.12 L氧气参与反应
D. 通空气时,铜被腐蚀,表面产生Cu2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是
A. 12 g金刚石中含有化学键的数目为4NA
B. 18 g的D2O中含有的质子数为10
C. 28 g的乙烯和环已烷混合气体中所含原子总数为6NA
D. 1 L 1mol·L1的NH4Cl溶液中NH4+和Cl―的数目均为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
A. 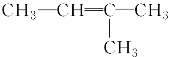 ―→
―→
B. CH2===CH—CH2—CH3+HCl![]()
C. CH3—CH===CH2+H2O![]()
D. nCH2===CH2+nCH2===CH—CH3![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种气体麻醉剂,可由“可燃冰”为原料合成。回答下列问题:
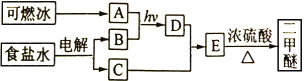
(1)B为黄绿色气体,其化学名称为____________。
(2)由A和B生成D的化学方程式为__________________。
(3)E的结构简式为____________。
(4)由E生成二甲醚的反应类型为______________________。
(5)二甲醚的同分异构体的结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃A在一定条件下可以按下图进行反应:

(已知:D是 、F1和F2互为同分异构体、G1和G2互为同分异构体)
、F1和F2互为同分异构体、G1和G2互为同分异构体)
请填空:
(1)A的结构简式是__________________。写出A发生加聚反应的化学方程式:_________________。
(2)框图中属于取代反应的是(填数字代号)________。
(3)框图中①③⑥属于(填反应类型)_________________。写出第⑤步反应的化学方程式:____________________。
(4)G1的结构简式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法正确的是( )
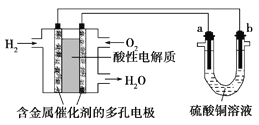
A. 燃料电池工作时,正极反应为O2+2H2O+4e-===4OH-
B. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
C. 电解过程中SO42— 移向b极
D. a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠是日常生活中人们常用的调味品。是下列事实中,可以证明NaCl中一定存在离子键的是
A.水溶液能导电B.易溶于水C.熔化时能导电D.有较高的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】指出下列变化能量是怎样转化的:
(1)学校燃烧煤煮饭____________,
(2)给手机的电池充电______________,
(3)用畜电池点亮灯泡_________,
(4)电解水得到O2和H2______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com