
【题目】叠氮化物是一类重要化合物,氢叠氮酸(HN3)是一种弱酸,如图为分子结构示意图1.肼(N2H4)被亚硝酸氧化时便可生成氢叠氮酸(HN3):N2H4+HNO2═2H2O+HN3 . 它的酸性类似于醋酸,可微弱电离出H+和N3﹣ . 
试回答下列问题:
(1)下列说法正确的是(选填序号).
A.酸性:HNO2>HNO3
B.N2H4中两个氮原子采用的都是sp2杂化
C.HN3、H2O都是极性分子
D.N2H4沸点高达113.5℃,说明肼分子间可形成氢键
(2)叠氮化物能与Fe3+、Cu2+及Co3+等形成配合物,如:[Co(N3)(NH3)5]SO4 , 在该配合物中钴显价,根据价层电子对互斥理论可知SO42﹣的立体构型为 , 写出钴原子在基态时的核外电子排布式: .
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)═2Na(l)+3N2(g),下列说法正确的是(选填序号).
A.NaN3与KN3结构类似,前者晶格能较小
B.钠晶胞结构如图2,晶胞中分摊2个钠原子
C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮元素的电负性小
(4)与N3﹣互为等电子体的分子有:(举两例).
【答案】
(1)CD
(2)+3;正四面体;1s22s22p63s23p63d74s2或[Ar]3d74s2
(3)BC
(4)CO2、BeCl2
【解析】解:(1.)A.HNO2为弱酸,而HNO3是强酸,故A错误;B.N2H4中氮原子最外层有5个电子,形成三对共用电子对,另外还有一对孤电子对,氮原子采用的都是sp3杂化,故B错误;C.HN3、H2O中都有孤电子对,所以都是极性分子,故C正确;D.氢键主要存在于N、F、O三种元素的氢化物分子之间,可使物质的熔沸点变大,N2H4沸点高达113.5℃,可以说明肼分子间可形成氢键,故D正确;所以答案是:CD;
(2.)在[Co(N3)(NH3)5]SO4中,根据化合价代数和为零,可以算得钴的化合价为:+3价,SO42﹣中S原子采用sp3杂化方式,可知SO42﹣的立体构型为正四面体;27号元素Co基态原子核外电子排布式为1s22s22p63s23p63d74s2或[Ar]3d74s2 , 所以答案是:+3;正四面体;1s22s22p63s23p63d74s2或[Ar]3d74s2;
(3.)A.NaN3与KN3结构类似,Na+半径小于K+ , 所以NaN3的晶格能比KN3大,故A错误;B.钠晶胞中,在8个顶点上各有一个原子,体心上还有一个,所以晶胞中钠原子的个数为:8× ![]() +1=2,故B正确;C.子的最外层P轨道有3个电子,处于半充满状态,是一种较稳定结构,所以它的第一电离能大于氧,故C正确;D.常温下很稳定,是因为氮气是双原子分子,两个氮原子之间存在N≡N键,不易断裂,与元素的电负性无关,故D错误; 所以答案是:BC;
+1=2,故B正确;C.子的最外层P轨道有3个电子,处于半充满状态,是一种较稳定结构,所以它的第一电离能大于氧,故C正确;D.常温下很稳定,是因为氮气是双原子分子,两个氮原子之间存在N≡N键,不易断裂,与元素的电负性无关,故D错误; 所以答案是:BC;
(4.)在N3﹣中,价电子数为16,根据等电子体原理,可以写出与N3﹣互为电子体的分子为CO2、BeCl2等,所以答案是:CO2、BeCl2 .


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0L恒容密闭容器中充入2mol SO2和1mol O2 , 发生反应: 2SO2(g)+O2(g)2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s | 0 | t1 | t2 | t3 | t4 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
A.反应在前t1 s 的平均速率v(O2)= ![]() ?mol?L﹣1?s﹣1
?mol?L﹣1?s﹣1
B.保持其他条件不变,体积压缩到1.0L,平衡常数将增大
C.相同温度下,起始时向容器中充入4mol SO3 , 达到平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2mol SO2、1mol O2 , 反应达到新平衡时 ![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质用途的说法不正确的是( )
A.二氧化硅是制作光导纤维的材料
B.氢氧化铁胶体可用作净水剂
C.碳酸氢钠可用于治疗胃酸过多
D.二氧化碳可用作镁燃烧的灭火剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X~W是元素周期表中的短周期元素,其性质或结构信息如下表:
元素 | X | Y | Z | V | W |
性质信息 | 单质为有色气体,有毒,可用于自来水消毒 | 日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着 | 其单质在空气中约占4/5左右 | 单质为淡黄色晶体,质脆,不溶于水,微溶于酒精 | 位于第ⅣA,是形成的化合物最多的元素之一 |
回答下列问题:
(1)X在元素周期表中的位置是____________,V2-离子结构示意图为______________。
(2)Z的单质特别稳定,原因在于_______________;X、Y和V三元素中原子半径最小的是_________。
(3)WV2常温下呈液态,是一种常见的溶剂。已知WV2在氧气中完全燃烧,生成VO2和WO2,若0.1 mol WV2在1 mol O2中完全燃烧,则所得气体混合物在标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种氧气吸收剂,为红棕色晶体,易被氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂)。其制备装置及步骤如下:
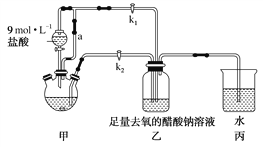
①检查装置气密性,往三颈烧瓶中依次加入过量锌粉、适量CrCl3溶液。
②关闭k2打开k1,旋开分液漏斗的旋塞并控制好滴速。
③待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,把溶液转移到装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞。
④将装置乙中混合物快速过滤、洗涤和干燥,称量得到2.76 g[Cr(CH3COO)2]2·2H2O。
(1)装置甲中连通管a的作用是______________________。
(2)三颈烧瓶中的Zn除了与盐酸生成H2外,发生的另一个反应的离子方程式为______________________。
(3)实验步骤③中溶液自动转移至装置乙中的实验操作为______________________。
(4)装置丙中导管口水封的目的是______________________。
(5)洗涤产品时,为了去除可溶性杂质和水分,下列试剂的正确使用顺序是________(填字母)。
a.乙醚 b.去氧冷的蒸馏水 c.无水乙醇
(6)若实验所取用的CrCl3溶液中含溶质3.17 g,则[Cr(CH3COO)2]2·2H2O(相对分子质量为376)的产率是______________________。
(7)一定条件下,[Cr(CH3COO)2]2·2H2O受热得到CO和CO2的混合气体,请设计实验检验这两种气体的存在________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或方法能达到目的是( )
A.用氨水除去试管内壁上的银镜
B.用通入氢气的方法除去乙烷中的乙烯
C.用点燃的方法鉴别乙醇、苯和四氯化碳
D.用溴水鉴别苯、甲苯和乙苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】李时珍在《本草纲目》中写到“烧酒非古法也,自元时始创其法。用浓酒精和糟入甑,蒸令气上,用器承取滴露。”文中涉及的操作方法是
A.分液B.萃取C.过滤D.蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜(甲醚具有可燃性,是一种常用的燃料).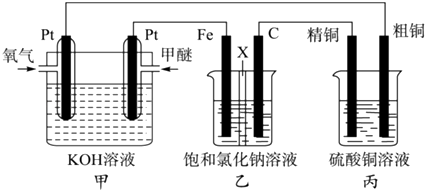
根据要求回答相关问题
(1)装置甲中通入燃料甲醚的一极是(填“正极”或“负极”),写出正极的电极反应式:
(2)装置乙中Fe为极(填“阳极”或“阴极”),石墨电极(C)的电极反应式为: .
(3)如果粗铜中含有锌、银等杂质,丙装置的阳极泥中含有 , 反应一段时间后,硫酸铜溶液浓度将(填“增大”、“减小”或“不变”.)
(4)当装置甲中消耗0.05molO2时,装置乙中溶液的pH为(溶液体积为200mL不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com