
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. pH=1的溶液中:Fe2+、NO![]() 、Na+、SO
、Na+、SO![]()
B. 水电离出的c(H+)=10-12 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO![]()
C. ![]() =1012的水溶液中:NH
=1012的水溶液中:NH![]() 、Al3+、NO
、Al3+、NO![]() 、Cl-
、Cl-
D. c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO![]() 、SCN-
、SCN-
科目:高中化学 来源: 题型:
【题目】t℃时,卤化银(AgX,X=Cl,Br)的2条溶解平衡曲线如图所示,已知AgCl,AgBr的Ksp依次减小,且p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-),利用pX-pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是
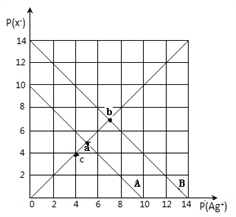
A. t℃时,c点可表示AgCl的不饱和溶液
B. B线表示的是AgBr
C. 取a、b两点处溶液等体积混合,维持t℃不变,混合溶液中一定无白色沉淀生成
D. 在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈104
AgBr(s)+Cl-(aq)平衡常数K≈104
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2和X气体分别通入BaCl2溶液,未见沉淀生成,若同时通入,有沉淀生成,则X气体不可能是
A.CO2 B.NH3 C.Cl2 D.H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
①油脂氢化的目的是提高油脂的熔点和稳定性②油脂是高级脂肪酸和甘油所生成的酯③油脂在酸性条件下的水解反应也叫皂化反应④油和脂肪属于同系物
A.①③B.①④C.①②D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 澄清石灰水中加盐酸:2H++Ca(OH)2===Ca2++2H2O
B. 向NaHCO3溶液中加入NaOH溶液:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. 氯气溶于水:Cl2+H2O![]() 2H++ClO-+Cl-
2H++ClO-+Cl-
D. 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO![]() ===BaSO4↓+H2O
===BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生将一氯丙烷和NaOH溶液共热煮沸几分钟后,冷却,滴入AgNO3溶液,结果未见到白色沉淀生成,其主要原因是( )
A.加热时间太短B.不应冷却后再滴入AgNO3溶液
C.加AgNO3溶液后未加稀HNO3D.加AgNO3溶液前未用稀HNO3酸化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 次氯酸钠溶液中通入过量的二氧化硫:ClO-+SO2+H2O===HSO![]() +HClO
+HClO
B. 等物质的量浓度、等体积的硫酸氢钠溶液和氢氧化钡溶液反应:H++SO![]() +Ba2++OH-===BaSO4↓+H2O
+Ba2++OH-===BaSO4↓+H2O
C. 氯气和水的反应:Cl2+H2O===2H++Cl-+ClO-
D. 向碳酸氢钾溶液中滴入过量澄清石灰水:2HCO![]() +Ca2++2OH-===CO
+Ca2++2OH-===CO![]() +2H2O+CaCO3↓
+2H2O+CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为冰晶石(化学式为Na3AlF6)的晶胞。己知冰晶石熔融时电离方程式为:Na3AlF6![]() 3Na++AlF63-。图中●位于大立方体顶点和面心,○位于大立方体的12 条棱的中点和8个小立方体的体心。则下列说法正确的是( )
3Na++AlF63-。图中●位于大立方体顶点和面心,○位于大立方体的12 条棱的中点和8个小立方体的体心。则下列说法正确的是( )
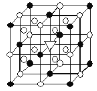
A. 冰晶石是原子晶体 B. 该物质中存在配位键
C. 大立方体的体心处△代表的是Al3+ D. 该物质是电解冶炼铝的还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知等体积的20%硫酸溶液其质量大于10%硫酸溶液,则将溶质的质量分数为a%、物质的量浓度为C1 mol·L-1的稀硫酸加热蒸发掉溶液总质量的一半的水,此时溶质的质量分数变为b%,物质的量浓度为C2 mol·L-1,下列关系正确的是
A. b﹤2 a B. C2﹤2 C1 C. C2﹥2 C1 D. C1=2C2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com