
【题目】课外活动时间玛丽同学制备Fe(OH)3胶体,具体操作如下:首先在烧杯中加入25mL蒸馏水,用酒精灯加热至沸腾,然后向烧杯中逐滴滴加6滴FeCl3饱和溶液,并继续煮沸至液体呈透明的红褐色,即得Fe(OH)3胶体。试回答下列问题:
(1)写出该反应的化学方程式:___。
(2)如何证明玛丽同学是否成功制得胶体_____?
(3)若玛丽同学在滴加FeCl3饱和溶液的同时用玻璃棒不断搅拌,结果没有得到胶体,为什么呢_____?
【答案】FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl 利用胶体的丁达尔效应,用一束可见光通过所得分散系,在入射光侧面若能看到光亮的通路,则证明已成功制得胶体 )搅拌会使胶体产生聚沉
Fe(OH)3(胶体)+3HCl 利用胶体的丁达尔效应,用一束可见光通过所得分散系,在入射光侧面若能看到光亮的通路,则证明已成功制得胶体 )搅拌会使胶体产生聚沉
【解析】
(1)氯化铁加入到沸水中水解生成氢氧化铁胶体;
(2)胶体具有丁达尔效应;
(3)依据胶体聚沉的性质和方法解答。
(1)该反应是利用FeCl3饱和溶液制取Fe(OH)3胶体,化学方程式为FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl;
Fe(OH)3(胶体)+3HCl;
(2)利用胶体的丁达尔效应,用一束可见光通过所得分散系,在入射光侧面若能看到光亮的通路,则证明已成功制得胶体;
(3)搅拌可加快胶体粒子的运动速率,增加了胶体粒子之间的碰撞机会, 使胶体发生聚沉。


科目:高中化学 来源: 题型:
【题目】化合物 Y 能用于高性能光学树脂的合成,可由化合物 X 与 2-甲基丙烯酰氯在一定条件下反应制得:

下列有关化合物 X、Y 的说法正确的是
A.X 分子中所有原子一定共平面B.Y 分子存在顺反异构
C.可以用酸性 KMnO4 溶液鉴别 X 和 YD.X→Y 的反应为取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物X的叙述正确的是( )

A.X分子能发生氧化、取代、消去反应B.X分子只存在2个手性碳原子
C.X分子中含有五种官能团D.1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素及其化合物的用途非常广泛。回答下列问题:
(1)基态氯原子价电子轨道表示式(电子排布图)为___;处于最高能级电子云轮廓图形状为____。
(2)![]() 和
和![]() 的中心原子相同且杂化方式也相同,它们的键长和键角如下图所示:
的中心原子相同且杂化方式也相同,它们的键长和键角如下图所示:
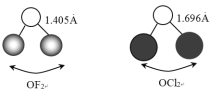
①O-F键的键长比O-Cl键的小,其原因是______。
②键角:∠FOF_____(填“>”、“<”或“=”)∠ClOCl。
(3)①试解释酸性HBrO4>HBrO3的原因_________。
②试解释酸性HClO3>HBrO3>HIO3的原因_________。
(4)![]() 的熔点为1040℃;
的熔点为1040℃;![]() 的熔点为194℃,沸点为181℃,前者的熔点比后者高得多,其原因是______。
的熔点为194℃,沸点为181℃,前者的熔点比后者高得多,其原因是______。
(5)氯化亚铜晶胞结构如图所示,晶胞参数a=0.542nm。
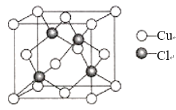
①Cu+的配位数为_____。
②氯化亚铜的密度为____![]() (用含NA的计算式表示)。
(用含NA的计算式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,将0.100mol的N2O4气体充入1L抽空密闭容器中,发生反应:N2O4(g)2NO2.现在隔一定时间对该容器内的物质进行分析,得到如下表格:
t/s c/(molL﹣1) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)/(molL﹣1) | 0.100 | c1 | 0.050 | c3 | a | b |
c(NO2)/(molL﹣1) | 0 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试回答下列问题:
(1)达到平衡时N2O4的转化率为_____%,表中c2_____c3,a_____b(后两空选填>、<、=)
(2)20 s的N2O4的浓度c1=_____mol/L在0~20s内N2O4的平均反应速率为_____mol/(Ls);
(3)若其他反应条件以及初始物质物质的量不变,将反应的温度降低到80℃时,达到平衡时NO2的物质的量为0.100 mol,那么正反应是_____反应(选填吸热或放热)
(4)若在相同初始情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度为_____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温,下列各组离子一定能在指定溶液中大量共存的是( )
A.![]() =10-12的溶液中:
=10-12的溶液中:![]() 、Cu2+、
、Cu2+、![]() 、
、![]()
B.滴加KSCN溶液显红色的溶液中:![]() 、K+、Cl-、I-
、K+、Cl-、I-
C.0.1mol·L-1的NaHCO3溶液中:Fe3+、K+、Cl-、![]()
D.水电离产生的c(OH-)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学概念在逻辑上存在如图关系,对下列概念的说法正确的是( )

A. 化合物与氧化物属于交叉关系
B. 单质与非电解质属于包含关系
C. 溶液与分散系属于并列关系
D. 化合物与电解质属于包含关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2CO3和NaHCO3的混合溶液,取该溶液50.00mL加水稀释到1L。
(1)从稀释后溶液中取出20.00mL.测量溶液体积的仪器事先进行洗涤的洗涤液依次为:自来水、_____、_____,对溶液体积读数的方法是读出_____对应的刻度值。
(2)稀释后溶液用标准盐酸(0.2000mol/L)进行滴定:
①取20.00mL溶液(酚酞做指示剂)消耗标准盐酸12.00mL。
②取10.00mL(甲基橙做指示剂)消耗标准盐酸15.00mL。
判断①滴定终点的现象是_____。则此次测定原样品溶液中碳酸氢钠的浓度_____。
(3)重复上述(2)滴定操作1﹣2次的目的是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在药物制剂中,抗氧剂与被保护的药物在与![]() 发生反应时具有竞争性,抗氧性强弱主要取决于其氧化反应的速率。
发生反应时具有竞争性,抗氧性强弱主要取决于其氧化反应的速率。![]() 、
、![]() 和
和![]() 是三种常用的抗氧剂。下列说法中,不正确的是
是三种常用的抗氧剂。下列说法中,不正确的是
已知:![]() 溶于水发生反应:
溶于水发生反应:![]()
实验用品 | 实验操作和现象 |
① ② ③ | 实验1:溶液①使紫色石蕊溶液变蓝,溶液②使之变红。 实验2:溶液①与 实验3:调溶液①②③的pH相同,保持体系中 |

A.![]() 溶液显碱性,原因是:
溶液显碱性,原因是:![]()
B.![]() 溶液中
溶液中![]() 的电离程度大于水解程度
的电离程度大于水解程度
C.实验2说明,![]() 在
在![]() 时抗氧性最强
时抗氧性最强
D.实验3中,三种溶液在pH相同时起抗氧作用的微粒种类和浓度相同,因此反应速率相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com