
【题目】“结晶玫瑰”具有强烈的玫瑰香气,属于结晶型固体香料,在香料和日用化工产品中具有广阔的应用价值。“结晶玫瑰”的化学名称为乙酸三氯甲基苯甲酯,通常用三氯甲基苯基甲醇和醋酸酐为原料制备。
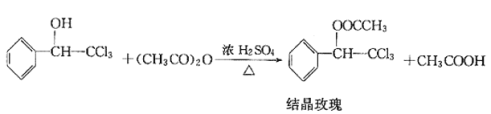
已知:
物质 | 在乙醇中的溶解性 | 在水中的溶解性 | 熔点℃ |
三氯甲基苯基甲醇 | 溶 | 不溶 | — |
醋酸酐 | 溶 | 溶 | -73 |
结晶玫瑰 | 溶 | 不溶 | 88 |
醋酸 | 易溶 | 易溶 | 16.6 |
部分实验装置以及操作步骤如下:
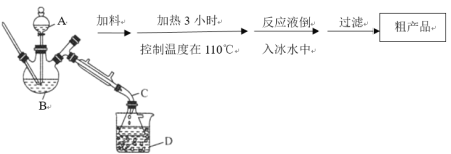
请根据以上信息,回答下列问题:
(1)装置中仪器B的名称是___________。
(2)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌。待混合均匀后,最适宜的加热方式为油浴加热,用油浴加热的理由是_______________。有同学认为装置中A仪器也可改为另一种漏斗,该漏斗的名称是___________,它的作用是____________。
现有同学设计如下方案把粗产品进行提纯。
(3)①将粗产品溶解在________(填“水”、“乙醇”或“粗产品滤液”)中均匀混合,用水浴加热到70℃,回流溶剂使粗产品充分溶解,得到无色溶液。然后将所得溶液经过__________(填操作方法)析出白色晶体,整个过程中不需要用到的仪器是_______(选择相应字母填空)。
A.冷凝管 B.烧杯 C.蒸发皿 D.玻璃棒
②将步骤①所得混合物过滤、洗涤、干燥得到白色晶体,请列举一种常见的实验室干燥的方法_______。可通过测定晶体的熔点判断所得晶体是否是结晶玫瑰,具体做法为:加热使其熔化测其熔点,实验现象为__________。
(4)ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰bg,则产率是_________。(用含a、b的式子表示)
【答案】三颈烧瓶 控制反应温度为110℃(大于100℃),且能使反应物均匀受热 恒压分液漏斗或恒压滴液漏斗 平衡气压,使液体顺利流下 乙醇 冷却结晶 C 空气中风干,空气中晾干,高温烘干,用滤纸吸干等 白色晶体在88℃左右完全熔化 ![]()
【解析】
三氯甲基苯基甲醇和醋酸酐放入三颈烧瓶,加入浓硫酸作催化剂,发生取代反应,为便于控制温度在110℃左右,需使用油浴加热;加热3小时后,反应基本完成,此时将反应混合液冷却,然后倒入冰水中,醋酸酐和醋酸溶解,而乙酸三氯甲基苯甲酯和少量三氯甲基苯基甲醇结晶析出;过滤后,得到粗产品。将粗产品溶于乙醇中均匀混合,用水浴加热到70℃,
再冷却结晶,过滤、洗涤、干燥,便可获得乙酸三氯甲基苯甲酯晶体。
(1)装置中,仪器B是具有三个颈的烧瓶,其名称是三颈烧瓶。答案为:三颈烧瓶;
(2)因为需加热温度为110℃,超出了水的沸点,所以最适宜的加热方式为油浴加热,用油浴加热的理由是控制反应温度为110℃(大于100℃),且能使反应物均匀受热。A仪器也可改为另一种漏斗,该漏斗应具有使液体容易滴下的作用,其名称是恒压分液漏斗或恒压滴液漏斗,它的作用是平衡气压,使液体顺利流下。答案为:控制反应温度为110℃(大于100℃),且能使反应物均匀受热;恒压分液漏斗或恒压滴液漏斗;平衡气压,使液体顺利流下;
(3)①因为粗产品中的成分难溶于水而易溶于乙醇,所以将粗产品溶解在乙醇中均匀混合,用水浴加热到70℃,回流溶剂使粗产品充分溶解得到无色溶液,然后将所得溶液经过冷却结晶析出白色晶体。溶解时应使用烧杯、玻璃棒,水浴加热、回流溶剂时需使用冷凝管,所以整个过程中不需要用到的仪器是蒸发皿,故选C。
②将步骤①所得混合物过滤、洗涤、干燥得到白色晶体,实验室干燥的方法可以是空气中风干、空气中晾干、高温烘干、用滤纸吸干等。可通过测定晶体的熔点判断所得晶体是否是结晶玫瑰,具体做法为:加热使其熔化测其熔点,因为结晶玫瑰是纯净物,所以温度在熔点附近时,晶体完全熔化,所以实验现象为白色晶体在88℃左右完全熔化。答案为:乙醇;冷却结晶;C;空气中风干,空气中晾干,高温烘干,用滤纸吸干等;白色晶体在88℃左右完全熔化;
(4)由反应方程式: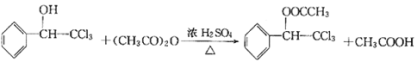 ,理论上,ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰的质量为
,理论上,ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰的质量为![]() =
=![]() g,则产率是
g,则产率是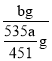 =
= ![]() 。答案为:
。答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。
回答下列问题:
(1)基态Ge原子价电子排布图为_______,Ge原子的电子发生跃迁时会吸收或发出不同的光,可用光谱分析仪获得______光谱(填“连续”或 “线状”),鉴定Ge元素的存在。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:Na2GeO3;二锗酸钠:Na2Ge2O5等),也能形成类似于烷烃的锗烷(GenH2n+2)。
①Na2GeO3中锗原子的杂化方式是______。
②推测 1molGenH2n+2中含有的σ键的数目是_____(用NA表示阿伏加德罗常数值)。
(3)利用离子液体[EMIM] [AlCl4]可电沉积还原金属Ge,其熔点只有7℃其中 EMIM+结构如图所示。
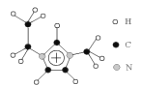
①该物质的晶体类型是_________。
②EMIM+ 离子中组成元素的电负性由小到大的顺序是________。
(4)独立的NH3分子中H-N-H 的键角为 107.3 ,[Zn(NH3)6]2+离子中H-N-H的键角________107.3° ( 填“大于”、“小于”或“等于” )。
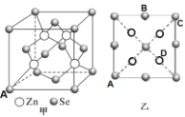
(5)硒化锌( ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是_____;已知晶胞边长为a pm,乙图为甲图的俯视图,A点坐标为( 0,0,0),B点坐标为(![]() ,a,
,a,![]() ) ,则 D点坐标为_______;若该晶胞密度为ρ g·cm-3,则阿伏加德罗常数NA为_______(列出计算式)。
) ,则 D点坐标为_______;若该晶胞密度为ρ g·cm-3,则阿伏加德罗常数NA为_______(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)回答下列问题:
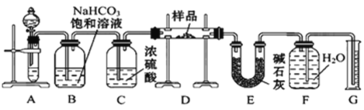
(1)装置B的作用是___________________; 装置E中碱石灰的作用是_________________________________。
(2)装置D中发生反应的化学方程式是_________________;______________________.
(3)超氧化钾(KO2)与过氧化钠一样能吸收CO2生成碳酸盐及O2,写出该反应的化学方程式_________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
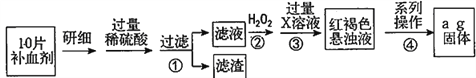
请回答下列问题:
(1)向操作①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有______(填离子符号)。
(2)操作②中反应的离子方程式:__________________________________。
(3)操作③中反应的离子方程式:__________________________________。
(4)操作④中一系列处理的操作步骤:过滤、______、灼烧、_______、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为______g。(用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图实验装置进行相关实验,能得出相应实验结论的是( )
a | b | c | 实验结论 |
| |
A | 浓醋酸 | CaCO3 | C6H5ONa溶液 | 酸性:碳酸>苯酚 | |
B | Br2的苯溶液 | 铁屑 | AgNO3溶液 | 苯和液溴发生取代反应 | |
C | 浓盐酸 | 酸性KMnO4溶液 | 碘化钾溶液 | 氧化性:Cl2>I2 | |
D | 饱和食盐水 | 电石 | 酸性KMnO4溶液 | 乙炔具有还原性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
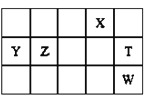
【题目】元素X、Y、Z、T、W在周期表中的位置如图所示,X原子最外层电子数是其内层电子数的3倍。下列说法正确的是
A.T元素的单质溶于水只需克服分子间作用力
B.TX2、T2或X3均可用于杀菌消毒
C.HT的酸性比HW的酸性强
D.Y与X形成碱性氧化物,能与酸和碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)

(1)写出下列物质的化学式:F____________,G________________。
(2)将混合物中两种金属分离开的最简单的方法是___________。
(3)D→E的转化中,加入过量的X可能是_____________________。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______________________________________________;
H→I:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是

A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com