
【题目】下列有关物质的量浓度关系中,正确的是( )
A.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO ![]() )>c(NH
)>c(NH ![]() )>c(H+)>c(OH﹣)
)>c(H+)>c(OH﹣)
B.室温下,pH=3的醋酸与pH=11的NaOH溶液等体积混合:c (Na+)>c (CH3COO﹣)>c(OH﹣)>c(H+)
C.浓度均为0.1 mol?L﹣1CH3COONa、NaHCO3、 ![]() ﹣ONa溶液中:若c(OH﹣)分别为c1、c2、c3 , 则c3>c2>c1
﹣ONa溶液中:若c(OH﹣)分别为c1、c2、c3 , 则c3>c2>c1
D.NaHCO3溶液中:c(Na+)=c(H2CO3)+c(HCO ![]() )+2c(CO
)+2c(CO ![]() )
)
【答案】AC
【解析】解:A.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合,反应后的溶液溶质为(NH4)2SO4和Na2SO4 , NH4+水解,溶液呈酸性,则c(Na+)=c(SO ![]() )>c(NH
)>c(NH ![]() ),c(H+)>c(OH﹣),一般来说,单水解的程度较弱,则有c(NH4+)>c(H+),应有c(Na+)=c(SO
),c(H+)>c(OH﹣),一般来说,单水解的程度较弱,则有c(NH4+)>c(H+),应有c(Na+)=c(SO ![]() )>c(NH
)>c(NH ![]() )>c(H+)>c(OH﹣),故A正确; B.醋酸为弱酸,室温下,pH=3的醋酸与pH=11的NaOH溶液等体积混合,醋酸过量,溶液呈酸性,则有c (CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣),故B错误;
)>c(H+)>c(OH﹣),故A正确; B.醋酸为弱酸,室温下,pH=3的醋酸与pH=11的NaOH溶液等体积混合,醋酸过量,溶液呈酸性,则有c (CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣),故B错误;
C.已知酸性:CH3COOH>H2CO3> ![]() ﹣OH,酸性越弱,对应的盐类水解程度越大,则浓度均为0.1 molL﹣1CH3COONa、NaHCO3、
﹣OH,酸性越弱,对应的盐类水解程度越大,则浓度均为0.1 molL﹣1CH3COONa、NaHCO3、 ![]() ﹣ONa溶液中:若c(OH﹣)分别为c1、c2、c3 , c3>c2>c1 , 故C正确;
﹣ONa溶液中:若c(OH﹣)分别为c1、c2、c3 , c3>c2>c1 , 故C正确;
D.根据物料守恒可知,NaHCO3溶液中存在c(Na+)=c(H2CO3)+c(HCO ![]() )+c(CO
)+c(CO ![]() ),故D错误.
),故D错误.
故选AC.


科目:高中化学 来源: 题型:
【题目】NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:Ⅰ.利用催化技术将尾气中的NO和CO转变成CO2和N2 , 化学方程式如下:
2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)△H=﹣748kJ/mol
2CO2(g)+N2(g)△H=﹣748kJ/mol
为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应.用气体传感器测得不同时间NO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | … |
c(NO)/molL﹣1 | 1.00×10﹣3 | 4.00×10﹣4 | 1.70×10﹣4 | 1.00×10﹣4 | 1.00×10﹣4 | … |
(1)前2s内的平均反应速率υ(N2)=(保留3位有效数字,下同);计算此温度下该反应的K= .
(2)达到平衡时,下列措施能提高NO转化率的是 . (填字母序号)
A.选用更有效的催化剂
B.降低反应体系的温度
C.充入氩气使容器内压强增大
D.充入CO使容器内压强增大
(3)已知N2(g)+O2(g)=2NO(g)△H=+180kJ/mol;则CO的燃烧热为 .
(4)Ⅱ.臭氧也可用于处理NO.O3氧化NO结合水洗可产生HNO3和O2 , 每生成1mol的HNO3转移mol电子.
(5)O3可由电解稀硫酸制得,原理如图.图中阴极为(填“A”或“B”),阳极(惰性电极)的电极反应式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证ⅦA族部分元素非金属性递变规律,设计如图进行实验,
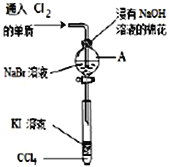
(1)仪器A的名称是______________,A中发生反应的离子方程式是______________________;
(2)为了验证溴和碘的非金属性强弱,通入C12单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象的___________________________;
(3)ⅦA族元素,非金属性随着原子序数的增加而逐渐减弱的原因:同主族元素从上到下,________________________,得电能力减弱。
(4)阅读上述实验操作步骤,为确保实验结论可靠,你认为做好本实验最关键的因素是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则下列叙述中正确的是
A. 原子序数:D>C>B>A B. 原子半径:B>A>C>D
C. 离子半径:C3->D->A2+>B+ D. 氧化性:A2+>B+,还原性:C3-<D-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D.E是短周期元素,周期表中A与B、C与E相邻;A与E的最外层电子数之比2:3,B的最外层电子数比C的最外层电子数少1个;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红。
(1)E的元素名称是_______,该己素在周期表中的位置为_______。
(2)A、B、C的氢化物稳定性又弱到强的顺序为(用分子式表示)_______;B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z中所含化学键的类型为________。
(3)写出D2C2的电子式________。用电子式表示只含D、E两种元素的化合物的形成过程________。
(4)写出D2C2与H2O反应的离子方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在VL密闭容器中,A、B、C三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析: 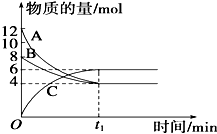
(1)反应的化学方程式为 .
(2)从开始到t1 min末时,用物质C表示的反应速率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe(OH)3胶体区别于FeCl3溶液最本质的特征是 ( )
A. Fe(OH)3胶体粒子的大小在1~100 nm之间 B. Fe(OH)3胶体具有丁达尔效应
C. Fe(OH)3胶体是均一、稳定的分散系 D. Fe(OH)3胶体的分散质能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 硫酸的摩尔质量是98gB. 18g水中含有水分子数为NA
C. O2的摩尔质量等于其相对分子质量D. 1molCO的质量为28g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
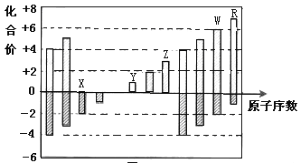
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:W>R
C. W最高价氧化物对应的水化物是强碱
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com