
【题目】连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图。常温下,下列各点所对应溶液中微粒物质的量浓度关系正确的是( )

A.a点:c(N2O22-)+c(HN2O2-)-c(Na+)=9.9×10-7mol·L-1
B.b点:c(Na+)>c(N2O22-)+c(HN2O2-)+c(H2N2O2)
C.c点:c(Na+)>c(HN2O2-)>c(N2O22-)>c(H2N2O2)
D.d点:2c(H2N2O2)+c(HN2O2-)+c(H+)=c(OH-)
【答案】D
【解析】
c点:10mL0.01mol·L-1的H2N2O2溶液滴加10mL 0.01mol·L-1的NaOH溶液二者发生反应,生成NaHN2O2溶液,此时pH大于7,则HN2O2水解大于电离,离子浓度大小比较:c(Na+)>c(HN2O2-)>c(H2N2O2) >c(N2O22-);d点:滴加20mL 0.01mol·L-1的NaOH溶液二者发生反应,生成Na2N2O2溶液,存在三大守恒;a和b点的溶质都含有NaHN2O2 和H2N2O2,但是比例不同,在没有明确的量比关系时,只能书写电荷守恒。
A.存在电荷守恒表示为2c(N2O22-)+c(HN2O2-)+ c(OH-)=c(Na+)+c(H+),a点pH=6,故2c(N2O22-)+c(HN2O2-)-c(Na+)=9.9×10-7mol·L-1,A项错误;
B. NaHN2O2的物料守恒表示为 c(Na+)=c(N2O22-)+c(HN2O2-)+c(H2N2O2),b点溶质含有NaHN2O2 和H2N2O2,故c(Na+)<c(N2O22-)+c(HN2O2-)+c(H2N2O2),B项错误;
C. 根据分析,c点:c(Na+)>c(HN2O2-)>c(H2N2O2) >c(N2O22-),C项错误;
D.根据分析, d点的质子守恒可以表示为:2c(H2N2O2)+c(HN2O2-)+c(H+)=c(OH-),D项正确;
答案选D。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。以含钴废料(主要成分为Co2O3,含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如下图所示:

已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
完全沉淀时的pH | 3.7 | 9.0 | 9.2 |
回答下列问题:
(1)“酸浸”含钴废料的温度不宜过高,原因是_____________。
(2) “酸浸”时发生的主要反应是___________________(写离子方程式)。
(3)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示:
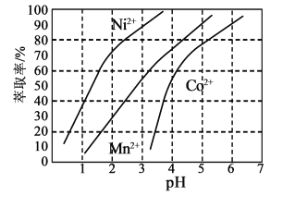
使用该萃取剂时应控制的pH约为____________,理由是_____________。
(4)写出高温煅烧时发生的化学反应方程式___________。
(5)操作1得到的副产品是__________(填名称);
已知该物质的溶液加热到100℃时会变质,该物质的溶解度见下表:
湿度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ |
溶解度 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 88.0 |
操作1是________(填字母)。
a.蒸发结晶 b.降温结晶 c.减压蒸发结晶
(6)有机相提取的Ni2+再生时可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH,则放电时负极的电极反应式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.为粗略测定质量为Wg的电石中CaC2的质量分数,利用电石与饱和食盐水反应,实验装置如图所示:
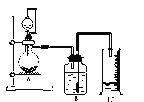
(1)烧瓶中发生反应的化学方程式是_____________
(2)产生的气体分子的中心原子的杂化轨道类型是____________
(3)实验测得量筒中水为VmL,该温度下气体摩尔体积为24.5 L/mol,则电石中CaC2质量分数为___________________
II.俄国化学家马尔柯夫尼柯夫因为提出碳碳双键的加成规则而闻名于世,该规则是指不对称的烯烃与HX或HCN加成时,氢总是加到含氢较多的双键碳原子上。
已知:![]()
以下是F的合成路线,请填写下列空白:
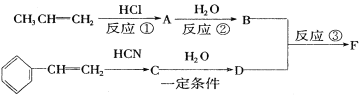
(1)写出C的结构简式______________
(2)B核磁共振氢谱共有__________________组氢
(3)写出③的化学方程式______________
(4)将F与含酚酞的NaOH溶液混合,加热一段时间后,可观察到的颜色变化是__________________
(5)若某有机物G是D的同系物,相对分子质量比D少14,则其分子式为:________;其同分异构体中含苯环且能使石蕊试液变红的物质共有______________种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对溴苯乙烯与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。完成下列填空:
(1)写出该共聚物的结构简式________。
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体![]() 。写出该两步反应所需的试剂及条件_______、__________。
。写出该两步反应所需的试剂及条件_______、__________。
(3)将![]() 与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。A的结构简式为_______。由上述反应可推知_________。由A生成对溴苯乙烯的反应条件为______。
与足量氢氧化钠溶液共热得到A,A在酸性条件下遇FeCl3溶液不显色。A的结构简式为_______。由上述反应可推知_________。由A生成对溴苯乙烯的反应条件为______。
(4)丙烯催化二聚得到2,3-二甲基-1-丁烯,B与2,3-二甲基-1-丁烯互为同分异构体,且所有碳原子处于同一平面,写出B的结构简式_______。设计一条由2,3-二甲基-1-丁烯制备B的合成路线_______。(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化硫(SCl2)熔点-78℃,沸点59℃,密度1.638g/mL,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2)。以下是氯气与硫合成二氯化硫的实验装置。
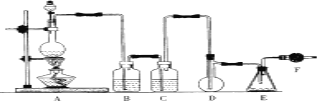
试回答下列问题:
(1)装置A中发生反应的化学方程式为______________________。
(2)装置B应盛放的药品是__________,C中是______________。
(3)实验时,D装置需加热至50—59℃.最好采用_____________方式加热。
(4)在配制一定物质的量浓度的盐酸溶液时,下列操作所配溶液浓度偏低的是__________;
A.配制溶液时,容量瓶中有少量水。
B.使用容量瓶配制溶液时,俯视观察溶液凹液面与容量瓶刻度线相切
C.配制溶液的过程中,容量瓶未塞好,洒出一些溶液。
D.发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是
选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子的立体构型 |
A | SO2 | sp | 直线形 | 直线形 |
B | HCHO | sp2 | 平面三角形 | 三角锥形 |
C | H3O+ | sp2 | 四面体形 | 平面三角形 |
D | NH4+ | sp3 | 正四面体形 | 正四面体形 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如图:
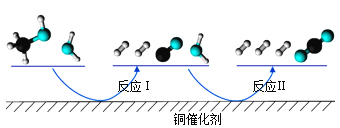

下列说法正确的是( )
A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) △H=+akJ/mol(a>0)
B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量
C.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗
D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com