
分析 (1)平衡后,通入2mol SO2,二氧化硫浓度增大,平衡正向移动;
(2)平衡后,通入2mol SO2,1mol O2,相当于在原来基础上增大压强,平衡正向移动;
(3)平衡后,通入a mol SO2,b mol O2,c mol SO3,相当于在原来基础上增大压强,平衡正向移动.
解答 解:(1)平衡后,通入2mol SO2,二氧化硫浓度增大,平衡正向移动,SO2的转化率减小,O2的转化率增大,故答案为:减小;增大;
(2)平衡后,通入2mol SO2,1mol O2,相当于在原来基础上增大压强,平衡正向移动,则SO2的转化率增大,O2的转化率 增大,SO2的百分含量 减小,O2的百分含量减小,SO3的百分含量增大,故答案为:增大;增大;减小;减小;增大;
(3)平衡后,通入a mol SO2,b mol O2,c mol SO3,相当于在原来基础上增大压强,平衡正向移动,则SO2的转化率 增大,O2的转化率 增大,SO2的百分含量减小,O2的百分含量减小,SO3的百分含量增大.故答案为:增大;增大;减小;减小;增大.
点评 本题考查化学平衡的移动,为高频考点,把握压强、浓度对平衡移动的影响为解答本题的关键,侧重分析与应用的考查,注意平衡移动原理的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 在化合物CaCl2中,除了有Ca2+与Cl-之间的离子键外,还有两个Cl-之间的共价键 | |
| B. | 碘受热升华时共价键被破坏 | |
| C. | 熔化状态下能导电的化合物中一定存在离子键 | |
| D. | 离子化合物中可能含有共价键,共价化合物中可能含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | CaO+H2O═Ca(OH)2 | ||
| C. | SO3+H2O═H2SO4 | D. | 2F2+2H2O═4HF+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{71b}{161(b+36a)}$×100% | B. | $\frac{71}{161}$×100% | ||
| C. | $\frac{b}{b+36a}$×100% | D. | $\frac{71b}{161(b+18a)}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
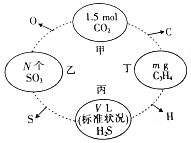 如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)
如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①③⑤ | C. | ②④⑥ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 待测液中一定存在SO42-、Fe3+、Cl-,可能存在Na+ | |
| B. | 待测液中:c(Cl-)≥0.2mol•L-1 | |
| C. | 另取100mL待测液加入足量Ba(OH)2溶液,可得6.8g沉淀 | |
| D. | 另取100mL待测液加入足量AgNO3溶液,可得2.87g沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有原子个数为0.3NA | B. | 分子个数约为6.02×1022 | ||
| C. | 物质的量是0.2mol | D. | 与质量相等的O2所含原子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com