
【题目】在合成氨过程中,进入合成塔的氮气和氢气的体积比为1∶3,压强为160 atm,从合成塔出来的混合气体中氨的体积分数为25%。求:
(1)从合成塔出来的气体中氮气和氢气的体积比是多少_______
(2)从合成塔出来的气体的压强是多少_______
【答案】从合成塔出来的气体中氮气和氢气的体积比为1∶3。 从合成塔出来的气体的压强是128 atm。
【解析】
(1)同温同压下,任何气体的体积比等于物质的量之比,据此分析;
(2)恒温恒容时,气体的压强比等于物质的量之比,据此分析。
(1)同温同压下,任何气体的体积比等于物质的量之比,
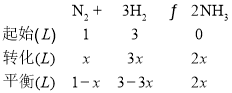 ,
,
则有:![]() =25%,x=0.4,则从合成塔出来的气体中氮气和氢气的体积比为 (1-x)∶(3-3x)=1∶3,故答案为:从合成塔出来的气体中氮气和氢气的体积比为1∶3;
=25%,x=0.4,则从合成塔出来的气体中氮气和氢气的体积比为 (1-x)∶(3-3x)=1∶3,故答案为:从合成塔出来的气体中氮气和氢气的体积比为1∶3;
(2)恒温恒容时,气体的压强比等于物质的量之比,则有:![]() =
=![]() ;
;![]() =
=![]() ,p后=128 atm,故答案为:从合成塔出来的气体的压强是128 atm。
,p后=128 atm,故答案为:从合成塔出来的气体的压强是128 atm。


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
A.6.0gSiO2晶体中含有共价键的个数为0.2NA
B.标准状况下,11.2LSO2与22.4LO2反应,生成的SO3分子个数小于0.5NA
C.MnO2与足量浓盐酸反应生成标准状况下11.2LCl2,转移电子数为NA
D.室温下,53.5gNH4Cl晶体溶于氨水中,所得溶液pH=7,NH4+的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰电池在生活巾应用广泛。工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下:
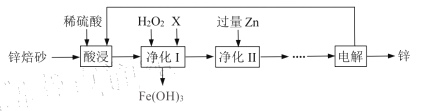
回答以下问题:
(1)ZnFe2O4中Fe的化合价是_______。
(2)为了提高酸浸效率,可采用的措施是_______(至少两条)。
(3)净化I的过程中温度不能太高,原因是________。
(4)X可以调节pH,则X为________。
(5)净化II中的离子反应方程式_______.
(6)本流程中可以循环利用的物质除锌外还有________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)![]() 2C(g)达到平衡标志的是
2C(g)达到平衡标志的是
①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④C的物质的量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a molA,同时生成3a mol B
⑧A、B、C的分子数之比为1:3:2
A. ⑤⑥B. ⑦④C. ①③D. ②⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取水煤气的反应为C(s)+H2O(g) ![]() CO(g)+H2(g) ΔH>0;在一定条件下达到化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是( )
CO(g)+H2(g) ΔH>0;在一定条件下达到化学平衡后,在时间为t时突然改变条件,反应速率的变化如图所示,在t时所改变的条件是( )

A.加压 B.升温 C.增大水蒸气浓度 D.增大碳的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+=I2+5SO42-+H2O,生成的I2可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
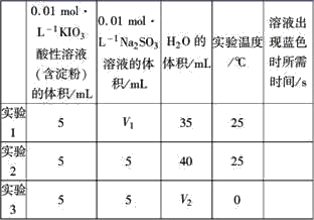
该实验的目的是_________;表中V2=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对某黄铁矿石(主要成分为FeS2)进行如下实验探究。
实验一:测定硫元素的含量
I.将m1 g该黄铁矿样品放入如图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全,得到红棕色固体和一种刺激性气味的气体。
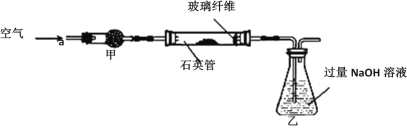
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:
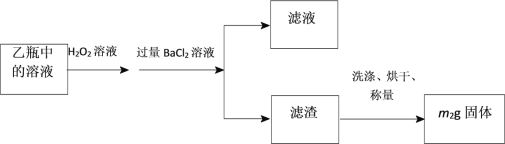
问题与讨论:
(1)石英管中发生反应的化学方程式为_________。
(2)I中,干燥管甲内所盛试剂是________,石英管中的玻璃纤维的作用为__________。
(3)该黄铁矿石中硫元素的质量分数为___________。
实验二:测定铁元素的含量

问题与讨论:
(4)步骤②中,若选用铁粉作还原剂,会使测量结果________(填“不影响”、“偏高”或“偏低”)。
(5)步骤③中,需要用到的玻璃仪器有烧杯、玻璃棒、_______、________。
(6)滴定终点的现象是___。
(7)用c mol/LKMnO4溶液滴定,终点时消耗KMnO4溶液V mL,则黄铁矿中铁元素的质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据能量变化示意图,下列说法正确的是( )

A. 状态1是液态,则状态3一定是气态
B. 状态3是液态,则状态4一定是气态
C. A(状态2)+B(g)═C(状态3)+D(g)△H=(d﹣a)kJmol﹣1
D. 断裂1molC(状态3)和1molD(g)中的化学键需要吸收的能量为(e﹣d)kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是( )


A.用乙醇萃取碘水中的碘B.用装置甲制取纯净的![]()
C.用装置乙除去![]() 中的少量
中的少量![]() D.中和滴定时,用待测液润洗锥形瓶,减小实验误差
D.中和滴定时,用待测液润洗锥形瓶,减小实验误差
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com