
【题目】下列有关叙述中正确的是( )
A.常温下,pH=4的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
B.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
C.已知25℃时NH4CN溶液显碱性,则25℃时的电离平衡常数K(NH3·H2O)<K(HCN)
D.0.1mol/L醋酸溶液加少量水稀释![]() 增大
增大
【答案】A
【解析】
A. 常温下,pH=4的CH3COOH与CH3COONa混合溶液呈酸性,则c(H+)>c(OH),根据电荷守恒c(H+)+ c(Na+)= c(OH)+ c(CHCOO),可知:c(Na+)<c(CHCOO),故A正确;
B. NaCl溶液和CH3COONH4溶液均显中性,氯化钠溶液对水的电离无影响,而醋酸根离子、铵根离子发生水解,促进了水的电离,故B错误;
C. 已知25℃时NH4CN溶液显碱性,说明CN离子水解程度大于NH4+离子,HCN酸性弱,电离程度小,则25℃时的电离常数:K(NH3H2O)>K(HCN),故C错误;
D. 醋酸中加入少量水后,醋酸的电离程度增大,则溶液中醋酸的物质的量减小,氢离子的物质的量增大,由于在同一溶液中,则![]() 的比值减小,故D错误;
的比值减小,故D错误;
答案选A。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法中正确的是( )
①标准状况下,4.48L NO 和2.24L O2 充分混合后所得混合物分子数为0.2NA
②含13g甲醛(HCHO)和17g乙酸(CH3COOH)的液体混合物中,氧原子数目为NA
③0.1 mol H2和 0.1 mol I2于密闭容器中充分反应后,其分子总数为 0.2NA
④1mol Na2O 和Na2O2混合物中含有的阴、阳离子总数是3NA
⑤常温常压下,30g的C2H6含有的共价键数为6NA
⑥标准状况下,22.4L HF中所含F原子数目为NA
⑦在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为5NA
A.②③④⑦B.①④⑤⑥C.①②③⑤⑥D.①②④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用还原沉淀法处理含铬废水(![]() 和
和![]() ),其流程为:
),其流程为:
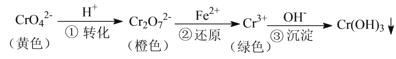
已知:步骤③生成的![]() 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:![]()
![]() ,
,![]()
下列有关说法不正确的是
A.步骤①中当![]() 时,说明反应:
时,说明反应:![]() 达到平衡状态
达到平衡状态
B.若向![]() 溶液中加NaOH浓溶液,溶液可由橙色变黄色
溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原![]() 离子,需要
离子,需要![]()
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽![]() 当溶液中
当溶液中![]() 时,可视作该离子沉淀完全
时,可视作该离子沉淀完全![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种氧气吸收剂,为红棕色晶体,易被氧化,不溶于水和乙醚(易挥发的有机溶剂),微溶于乙醇,易溶于盐酸,其制备装置如下(已知Cr3+水溶液颜色为绿色,Cr2+水溶液颜色为蓝色):

(1)装置甲中连通管a的作用是________________________。
(2)向三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液:关闭k2打开k1,旋开分液漏斗的旋塞并控制好滴速;当观察到三颈烧瓶中溶液颜色__________________时,打开k2关闭k1,当观察到装置乙中出现大量红棕色晶体时,关闭分液漏斗的旋塞。
(3)装置乙中反应的离子方程式为__________________________________。
(4)将装置乙中混合物快速过滤、洗涤和干燥,称量得到a g [Cr(CH3COO)2]2·2H2O。洗涤时依次用去氧的冷蒸馏水、无水乙醇、乙醚洗涤。其中乙醇洗涤的目的是___________。
(5)若实验所取用的CrCl3溶液中含溶质b g,则[Cr(CH3COO)2]2·2H2O (相对分子质量为376) 的产率是________________。
(6)该实验装置有一个明显的缺陷,解决此缺陷的措施为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
请回答下列问题:
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是_________。
(2) 0.1mo1/L的H2C2O4溶液与0.1mo1/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为________________。
(3)pH相同的NaC1O和CH3COOK溶液中,[c(Na+)-c(C1O-)]______[c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mo1/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图Ⅰ、Ⅱ分别是甲、乙两组同学根据反应“![]() +2I-+2H+=
+2I-+2H+=![]() +I2+H2O”设计成的原电池装置,其中 C1、C2 均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图Ⅱ的 B 烧杯中逐滴加入适量 40% NaOH 溶液。下列叙述中正确的是 ( )
+I2+H2O”设计成的原电池装置,其中 C1、C2 均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图Ⅱ的 B 烧杯中逐滴加入适量 40% NaOH 溶液。下列叙述中正确的是 ( )

A.甲组操作时,电流表(A)指针发生偏转
B.甲组操作时,溶液颜色变浅
C.乙组操作时,C1上发生的电极反应为I2+2e-=2I-
D.乙组操作时,C2作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生产和生活息息相关。下列说法不正确的是 ( )
A.硅太阳能电池与原电池的原理不同
B.铵态氮肥和草木灰混合使用可增加肥效
C.用可溶性的铝盐和铁盐处理水中的悬浮物
D.硫酸工业中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为![]() 的密闭容器中反应
的密闭容器中反应![]()
![]() 达到平衡,下列说法正确的是
达到平衡,下列说法正确的是
容器 | 温度 | 物质的起始浓度 | ||
|
|
| ||
Ⅰ | 400 |
|
| 0 |
Ⅱ | 400 |
|
|
|
Ⅲ | 300 | 0 | 0 | td style="width:88.2pt; border-top-style:solid; border-top-width:0.75pt; border-left-style:solid; border-left-width:0.75pt; padding:3.38pt 5.03pt; vertical-align:middle">|
A.达到平衡时,向容器Ⅰ中通入氦气,正、逆反应速率均增大,平衡不移动
B.达到平衡时,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C.达到平衡时,容器Ⅲ中![]() 小于容器Ⅰ中
小于容器Ⅰ中![]() 的两倍
的两倍
D.容器中混合气体的密度不再发生变化可作为反应达到平衡状态的标志
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com